Wann ist inhalatives Kortikoid (ICS) bei chronisch-obstruktiver Lungenerkrankung (COPD) sinnvoll? Im Gegensatz zum Asthma, bei dem ICS in aller Regel unverzichtbar sind, sollten sie bei der COPD mit Bedacht und gezielt eingesetzt werden. Denn diese Substanzen bergen in der Langzeittherapie bekanntlich auch Gefahren. Sie sollten möglichst nur dann zum Einsatz kommen, wenn rezidivierende akute Exazerbationen mittels LAMA und LABA nicht beherrschbar sind.
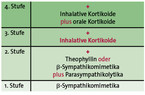
Eine Empfehlung zur Therapie chronisch-obstruktiver Atemwegserkrankungen gab die Deutsche Atemwegsliga erstmals 1984 heraus (Abb. 1) [1]. Die damaligen Therapiehinweise unterschieden aber noch nicht zwischen Asthma und chronisch-obstruktiver Bronchitis (COB, später COPD). Stufe 1 und 2 empfahl die anti-obstruktive Therapie. Eine Bronchodilatation rund um die Uhr erforderte – wegen der kurzen Wirkdauer der früheren Bronchodilatatoren SABA und SAMA (nur drei bis sechs Stunden) und zur Überbrückung der nächtlichen Pause – eine Kombination aus Inhalativum plus retardierter oraler Medikation. Stufe 3 und 4 sah eine Therapie mit einem inhalativen und/oder oralen Kortikoid vor. Über einen eventuellen Wirkmechanismus gab es zu diesem Zeitpunkt keinerlei Kenntnisse [1, 2].
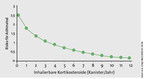
Seit Mitte der 1980er-Jahre haben Kortikoide ihren festen Platz in der Asthmatherapie. Mit der Entdeckung der beiden Entzündungsformen bei Asthma und COPD – einer überwiegend eosinophilen beim Asthma und einer neutrophilen bei chronisch-obstruktiver Lungenerkrankung – lässt sich Asthma semikausal therapieren: Endlich konnte man die Entzündung beim Asthma gezielt behandeln. Heute ist die semikausale Therapie mit einem Kortikoid zur Inhalation (ICS) derart erfolgreich, dass wir Asthmatikern praktisch Beschwerdefreiheit garantieren können. Einzige Voraussetzung: Der Patient muss die Therapie regelmäßig und korrekt vornehmen. Zahl und Dosis der Substanzen passt der Arzt individuell an. Hausbesuche in den frühen Morgenstunden bei Patienten, die einen Asthmaanfall erlitten haben, gehören heute der Vergangenheit an. Auch in der Klinik begegnet man kaum mehr solchen Fällen – damals gehörten sie zur nächtlichen Routine. Die Mortalität beim Asthma sank ebenfalls dramatisch (Abb. 2).
Unterschiedliche Therapieempfehlungen für Asthma und COPD wurden erstmals 1988 herausgegeben. Für die Asthmatherapie gelten seitdem drei Forderungen:- Die Basis ist eine anti-entzündliche Therapie mit einem ICS. Hier gibt es nur extrem seltene Ausnahmen wie die Unverträglichkeit für ICS oder eine Sonderform des Asthmas, das neutrophile Asthma.
- Alle anderen Substanzen werden, falls nötig, zusätzlich eingesetzt, nie aber als Ersatz des ICS.
- Für die Dosierung gilt: So viel wie nötig, so wenig wie möglich!
Der Arzt beurteilt die Entzündung und passt die ICS-Dosis an die aktuelle Intensität an. Im Gegensatz zur semikausalen Therapie beim Asthma ist es bei der COPD bis heute noch nicht möglich, die Entzündung gezielt anzugehen. Unsere Bemühungen sind deshalb auf eine rein symptomatische Therapie begrenzt. Mit der Einführung langwirkender Bronchodilatatoren wurde die Inhalation zum Goldstandard. Alle oral zu applizierenden Substanzen waren plötzlich fast überflüssig und wurden nur noch im Ausnahmefall eingesetzt. Durch weitere Neueinführungen (Tabelle 1) gestaltete sich die Therapie noch einfacher und effektiver. Bei einigen älteren Substanzen, wie dem Theophyllin, machten wir immer wieder positive Erfahrungen. Die Patienten beschrieben Effekte, die nach Absetzen wieder verschwanden, ohne dass wir diese objektivieren konnten. Im Ausnahmefall lohnt deshalb immer ein Versuch.
Kortikoide bei COPD
Kortikoide waren früher auch in weiteren Empfehlungen der höheren Stufen enthalten, behielten aber den Charakter einer "Ultima Ratio". Bei der COPD stellten sich hier immer wieder "Zufallserfolge" heraus, für die wir allerdings keine plausible Erklärung hatten – außer, dass wir in diesen Fällen ein gleichzeitig vorliegendes Asthma (COPD + Asthma) therapiert haben könnten. Erst mit der Erkenntnis, dass die Exazerbationen die Progredienz und die Prognose der COPD bestimmen, änderte sich unsere Zielsetzung. Exazerbationen intensivieren den Lungenfunktionsverlust und steigern die Mortalität während und auch noch viele Monate nach diesem Ereignis. Heute sind wir endlich in der Lage, die Kortikoide auch bei der reinen COPD gezielt einzusetzen oder auf sie wegen fehlender Effekte zu verzichten.
Systemische Kortikoide (OCS)
Die Therapie mit einem systemischen Kortikoid ist bei der akuten Exazerbation (AECOPD) ein Muss (30 – 50 mg für maximal zehn Tage; abruptes Absetzen). In der Langzeittherapie haben diese Medikamente nur negative Effekte wie eine erhöhte Infektneigung und häufigere Exazerbationen.
Inhalierbare Kortikoide (ICS)
Die ICS können die Zahl und wahrscheinlich auch die Intensität von Exazerbationen reduzieren. Sie sind jedoch nicht in der Lage, den Lungenfunktionsverlust oder die Mortalität zu reduzieren.
Dass die positiven Erkenntnisse zur Progressionshemmung von Exazerbationen unter ICS bei COPD häufig nicht berücksichtigt werden, hat die DACCORD-Studie bedauerlicherweise belegt [3]. Nur 45 % der Patienten mit Exazerbationen, also einer Indikation für ICS, erhielten eine solche Therapie. Mehr als die Hälfte blieb demnach ohne diese effektive Substanz. Hingegen erhielten fast 40 % der Patienten ohne Exazerbationen ein ICS. Bei ihnen bleibt diese Therapie jedoch ohne Effekt, ist aber mit einem erhöhten Risiko verbunden. Offenbar bestätigt sich hier die Befürchtung, dass eine Differenzierung zwischen Asthma und COPD und eine daraus folgende differenzierte Therapie mit ICS für nicht erforderlich gehalten wird – leider zum Nachteil der Patienten [4].
Inzwischen haben weitere Erkenntnisse den Einsatz für die ICS weiter eingeschränkt:- Alle Inhalativa, d. h. LAMA, LABA und ICS haben eine vergleichbare Potenz, Exazerbationen zu reduzieren. Keine der Substanzen ist besser als die andere [5]!
- Für die ICS konnte belegt werden, dass sich die Fähigkeit zur Reduktion von Exazerbationen auf Patienten mit fortgeschrittener COPD (FEV1 ≤ 40 %) beschränkt [5].
Der Einsatz dieser drei Substanzen, mit denen sich die akute Verschlechterung der COPD aufhalten lässt, kann jetzt bei vergleichbar positiven Effekten vom jeweiligen Nebenwirkungspotenzial abhängig gemacht werden. LAMA und LABA sind die risikoärmeren Alternativen.
Gegen die Gabe von ICS spricht einiges:- ein erhöhtes Pneumonierisiko
- - per se ein deutlich erhöhtes Risiko für Pneumokokkeninfekte haben,
- - ohnehin zu den älteren Patienten zählen, die ein zunehmend schwächeres Immunsystem mit Infektneigung entwickeln und
- - nach Pneumonien für viele Monate eine deutlich erhöhte Letalität aufweisen.
- Der Soor befällt dosisabhängig nicht nur den Mund, sondern auch den Ösophagus [6, 7, 8]. Die Soor-Ösophagitis wird in der Literatur bisher nicht erwähnt, obwohl sie vermutlich nicht selten ist. In einer Untersuchung liegt sie bei Patienten unter ICS bei 37 % von ihnen vor und nur zu 0,3 % in der Kontrollgruppe [9].
- Die Osteoporose ist seltener als befürchtet, wird bei COPD aber durch Inaktivität, eingeschränkte Belastbarkeit und die üblicherweise höheren ICS-Dosen begünstigt.
Das Nebenwirkungsrisiko der LAMA und LABA ist dagegen deutlich geringer zu bewerten. Für die ICS bei COPD muss die Forderung lauten: So oft wie nötig, so selten wie eben möglich! Es ist selbstverständlich, dass die inhalativen Kortikoide ihre Berechtigung bei der Kombination aus COPD plus Asthma (ACO) haben. Möglicherweise ist einer der entscheidenden Hinweise auf die asthmatische Komponente eine erhöhte Zahl von Eosinophilen im Blutbild. Bei COPD mit asthmatischer Komponente sollte man immer wie beim Asthma therapieren, d. h. mit ICS!
Die neuen Leitlinien von 2018 empfehlen für die Therapie der reinen COPD:- Beginn mit einem Bronchodilatator (wegen des geringeren Nebenwirkungspotenzials bevorzugt mit einem LAMA)
- LAMA + LABA bei unzureichender Besserung oder direkt bei intensiver Symptomatik. Die Empfehlungen gelten für Patienten mit und ohne Exazerbationen. Der Vorteil dieser Therapievariante ist eine Reduktion der Krankheitsschübe bei gleichzeitig intensiverer Bronchodilatation: Sie lindert die Symptome, steigert die Lebensqualität und führt zur Entblähung und Besserung der pulmonalen und kardialen Belastbarkeit. LABA + ICS sind die eindeutig schlechtere Alternative. Bei Patienten ohne Exazerbationen sind ICS überhaupt nicht indiziert.
- Nur wenn unter der dualen Bronchodilatation noch Exazerbationen auftreten, ist ein ICS zusätzlich (!) gerechtfertigt (LAMA + LABA + ICS = Triple-Therapie).
ICS sollten bei COPD aber nur verordnet werden, wenn unter dualer Bronchodilatation noch Exazerbationen auftreten! Nachweislich hat die Triple-Therapie im Vergleich zur dualen Bronchodilatation einen additiven Effekt, doch ist sie erst bei deren "Versagen" und nicht als Alternative im Sinne der Leitlinien indiziert.
Übertherapie mit der Triple-Therapie bei COPD in Deutschland!
Eine Indikation für die Triple-Therapie dürfte es deshalb nur bei wenigen COPD-Patienten mit Exazerbationen geben. Es ist völlig unverständlich, dass nicht nur in Deutschland (ein Drittel), sondern auch in den Niederlanden (ein Viertel) sowie in Spanien und England (laut persönlichen Angaben) – und vermutlich weltweit so viele Patienten mit COPD eine freie oder fixe Dreifachkombination erhalten. Rein rechnerisch bekommen in deutschen Praxen mehr Patienten eine Triple-Therapie, als es überhaupt Patienten mit Exazerbationen gibt (Tabelle 2). Die meisten von ihnen wären mit der dualen Bronchodilatation vollkommen ausreichend therapiert, benötigen demnach kein ICS.
Aus der DACCORD-Studie geht außerdem hervor, dass offenbar mehr oder weniger kritiklos aus der Kombination LABA + ICS eine Dreifach-Therapie gemacht wird, ohne dass noch vorhandene Exazerbationen dies unbedingt erforderten. Anders lässt sich diese Übertherapie nicht interpretieren. Der Verzicht auf ICS könnte meist effektiver, gefahrloser und preiswerter sein. Mit dem aktuellen Vorgehen werden die genannten Gefahren einfach billigend in Kauf genommen.
Korrektes Vorgehen bei COPD
- Patienten unter LABA + ICS ohne Exazerbationen = Absetzen des ICS
- Patienten unter LABA + ICS mit Exazerbationen = Absetzen des ICS – bei unzureichender Symptomlinderung und/oder Auftreten von Exazerbationen: Steigerung der Therapie mit einem zweiten Bronchodilatator (LAMA + LABA)
- Patienten unter LAMA + LABA mit Exazerbationen = Beginn einer Triple-Therapie
Diese Hinweise gelten auch vor dem Hintergrund, dass sich das Krankheitsbild durch Absetzen von ICS bei einigen wenigen Patienten verschlechtert. Komplikationen treten aber nur selten auf. Zur Sicherheit lässt man die Präparate am besten ausschleichen. Die Patienten sollten sich nach drei Monaten oder bei subjektiver Verschlechterung wieder bei ihrem Arzt vorstellen.
Dr. med. Thomas Hausen
Interessenkonflikte: Der Autor hat Honorare für Beratung und Vorträge von Aerocrine, Bayer, Berlin-Chemie und Novartis erhalten.
Erschienen in: Der Allgemeinarzt, 2018; 40 (10) Seite 16-19