Dem akuten Thoraxschmerz kann eine ganze Reihe schwerwiegender Erkrankungen zugrunde liegen. Die Differenzialdiagnostik des plötzlich auftretenden Brustschmerzes bleibt daher für Hausärzte eine große Herausforderung. Eine rasante Entwicklung hat durch die Einführung hoch-sensitiver Troponin-Tests der Nachweis bzw. Ausschluss eines akuten Koronarsyndroms genommen. Die in der ambulanten Versorgung mit zunehmender Häufigkeit verwendeten Troponin-Schnelltests sollten allerdings mit Vorsicht genutzt werden, denn ihre Sensitivität ist (noch) begrenzt.
Als akuten Brustschmerz bezeichnet man neu aufgetretene Schmerzen im Brustkorb mit Druckgefühl oder Missempfindungen. Häufig werden diese Beschwerden von vorübergehender oder anhaltender Schmerzausstrahlung in den linken oder rechten Arm, in Nacken oder Kiefer begleitet. Auch ist eine starke vegetative Symptomatik mit Schwitzen, Übelkeit, Erbrechen, Bauchschmerzen oder Dyspnoe zu beobachten.
Weltweit gehört der akute Brustschmerz zu den häufigsten Vorstellungsgründen in den Notaufnahmen (3 – 6 %) [1, 2]. Aufgrund unterschiedlicher akut lebensbedrohlicher Differenzialdiagnosen, die ein unverzügliches Handeln erfordern, ist die Priorisierung und Stratifizierung von Brustschmerzpatienten eine große klinische Herausforderung. In der Allgemeinarztpraxis machen Patienten mit Brustschmerzen zwar einen deutlich geringeren Anteil aus (0,7 %) [3], jedoch spielt der erstbehandelnde Arzt in vielen Fällen für die erfolgreiche und zeitgerechte Versorgung klinisch kritischer Patienten eine entscheidende Rolle.
Frau W., 67, stellt sich bei ihrem Hausarzt mit linksthorakalen Schmerzen ohne Ausstrahlung vor, die seit sechs Stunden andauern. Zudem klagt sie über bislang unbekannte Atemnot (NYHA II–III). Weitere Symptome verneint sie.
Folgende kardiovaskuläre Risikofaktoren sind bei ihr bekannt: langjähriger Hypertonus (Ramipril 2,5 mg 1 – 0 – 1), Ex-Raucherin (15 PY) – seit zehn Jahren abstinent – und eine Hypercholesterinämie (LDL-Cholesterin 119 mg/dl bei bestehender Therapie mit 20 mg Atorvastatin). Es existieren sonst keine relevanten Vorerkrankungen. Eine kardiologische Basisdiagnostik inklusive Belastungs-EKG und Echokardiographie vor zwei Jahren erbrachte keine auffälligen Befunde.
Die körperliche Untersuchung ist bis auf eine erhöhte Atemfrequenz (28/min) und eine erhöhte Herzfrequenz (105/min) unauffällig. Die EKG-Untersuchung zeigt einen tachykarden Sinusrhythmus, einen inkompletten Rechtsschenkelblock sowie diskrete T-Negativierungen in den Ableitungen V1 – V3. Aufgrund der anhaltenden klinischen Beschwerdesymptomatik und der erhobenen Befunde veranlasst der Kollege eine notfallmäßige Einweisung in die nächstgelegene Notaufnahme.Die gefährlichsten, weil lebensbedrohlichen Differenzialdiagnosen des akuten Brustschmerzes umfassen das akute Koronarsyndrom (ACS), die Lungenarterienembolie, das akute Aortensyndrom, den Pneumothorax sowie – sehr selten – das Boerhaave-Syndrom [4]. Das ACS verbirgt sich hinter 3,6 % der Patienten, die sich wegen Brustschmerzen beim Hausarzt vorstellen, und ist damit eine höchst relevante Differenzialdiagnose [3]. Die anderen hier genannten Erkrankungen müssen zwar immer in Betracht gezogen werden, sind beim Allgemeinarzt aber nur selten anzutreffen.
Risikostratifizierung in der Hausarztpraxis
Grundsätzlich muss bei jedem Patienten mit akuten Brustschmerzen zunächst von einer bedrohlichen, instabilen Situation ausgegangen werden. Sobald Anzeichen für akutes Kreislaufversagen, Bewusstseinseintrübung und/oder Verwirrtheit, für vorangegangene Synkope oder Kollaps, Kaltschweißigkeit, Ruhedyspnoe und/oder ausgeprägte Angst des Patienten vorliegen, sollte eine sofortige Stabilisierung und eine notfallmäßige stationäre Einweisung erfolgen [5]. Bei Verdacht auf ein ACS empfiehlt es sich, ein 12-Kanal-EKG zu schreiben, eine symptomatische Therapie zu beginnen (z. B. Nitroglycerin-Applikation, ggf. Morphin) sowie Acetylsalicylsäure (300 mg oral, oder > 250 mg i.v.) und Heparin (5000 IE i.v.) zu applizieren. Keine dieser Maßnahmen darf jedoch den Transport in die nächstgelegene Notaufnahme zur weiteren Versorgung des Patienten verzögern. Zeigen sich im 12-Kanal-EKG
ischämietypische Veränderungen, insbesondere ST-Hebungen, sollte in Abstimmung mit dem Notarzt der Transport in ein Zentrum mit interventioneller Kardiologie erfolgen.
Bestehen die Beschwerden schon länger (> 72 h), kann die Wahrscheinlichkeit einer koronaren Herzkrankheit (KHK) als Ursache der Beschwerden abgeschätzt werden. Der von Bösner et al. erarbeitete "Marburger Herz-Score" ermöglicht dies auf einfache Art (Tabelle 1). Der Score ist speziell auf die Prävalenz von Brustschmerzen in der hausärztlichen Versorgung abgestimmt [6]. Bei einer Summe von mindestens zwei Punkten (P) sollte man eine KHK als mögliche Ursache der Beschwerden abklären. Je nach Häufigkeit und Dauer der Symptomatik sowie nach Dynamik im Vorfeld der Vorstellung sollte man Troponin bestimmen, um ein akutes Geschehen auszuschließen.
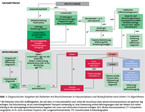
Bei den hierfür zunehmend in der ambulanten Versorgung verwendeten Troponin-Schnelltests ist aufgrund der aktuell noch begrenzten Sensitivität jedoch Vorsicht geboten. Bei unauffälligem Troponin-Ergebnis kann der niedergelassene Kardiologe die weitere Abklärung der KHK ambulant vornehmen, bei hinreichendem Risikoprofil kann auch eine direkte stationäre Einweisung sinnvoll sein. Bei unauffälligem Marburger Herz-Score muss der Arzt prüfen, inwieweit es Hinweise auf eine der genannten akut lebensbedrohlichen Erkrankungen gibt. Bei fehlenden Hinweisen kann ein weiteres ambulantes Management erfolgen (Abb. 1).
Diagnostisches Vorgehen in der Notaufnahme
Nach der aktuellen Leitlinie der "Europäischen Gesellschaft für Kardiologie" (ESC) für Patienten mit Nicht-ST-Hebungsinfarkt (NSTEMI) sollte nach Eintreffen in der Notaufnahme innerhalb der ersten zehn Minuten ein 12-Kanal-EKG geschrieben und befundet werden [7]. Bei ST-Hebungen sollte man umgehend (falls nicht zuvor schon geschehen) > 250 mg Acetylsalicylsäure i.v. und 5.000 IE Heparin verabreichen und eine invasive Koronardiagnostik durchführen. Zeigen sich keine ST-Hebungen, ist der konsequente Ausschluss eines NSTEMI entscheidend. Da bei über 30 % der Patienten mit NSTEMI keine EKG-Veränderungen erkennbar sind [7], erfolgt der sogenannte Infarktausschluss mit Blut-Biomarkern. Aufgrund der hohen Spezifität hat sich die Bestimmung des kardialen Troponins als Goldstandard zur Entdeckung myokardialer Ischämie durchgesetzt. Mit der Entwicklung neuartiger, sogenannter hoch-sensitiver Troponin-Tests, die extrem niedrige Troponinkonzentrationen erfassen, konnte man in den letzten Jahren die Präzision für den Ausschluss und die Diagnose eines Myokardinfarkts optimieren und das diagnostische Fenster deutlich verkürzen [8 – 10].
So wurde mit den ESC-Leitlinien 2011 die Risikostratifizierung von Patienten mit V. a. Myokardinfarkt mittels zwei serieller hoch-sensitiver Troponin-Messungen im Abstand von nur drei Stunden etabliert. Die intensive Forschung mehrerer internationaler Arbeitsgruppen konnte die Sicherheit noch kürzerer Protokolle belegen [8, 9, 11]. Seit 2015 ermöglichen die Leitlinien somit den Ausschluss eines Myokardinfarkts mit zwei Troponinbestimmungen in einem zeitlichen Abstand von nur einer Stunde [7]. Hier arbeitet man mit sehr niedrigen Troponin-Grenzwerten, die nur die neuen hoch-sensitiven Tests sicher erfassen. Auf Basis dieser Algorithmen kann man rund 40 % der Patienten schon nach kurzer Zeit in der Notaufnahme wieder entlassen.
Eine entscheidende Einschränkung ist, dass die zugrundeliegenden Studien nur wenige Patienten mit sehr früher Vorstellung nach Symptombeginn eingeschlossen haben. Daher können die schnellen Algorithmen nur für Patienten mit einem Symptombeginn, der über drei Stunden zurückliegt, empfohlen werden (Abb. 1). Besonders wichtig ist, dass der behandelnde Arzt die Spezifikationen des Troponin-Tests seines Labors kennt, denn Roh- und Grenzwerte sind speziell für den jeweiligen Labortest angelegt und nicht übertragbar [12].
Durch die höhere Sensitivität der modernen Tests fallen diese mitunter auch positiv aus, ohne dass ein Myokardinfarkt vorliegt. Erkrankungen wie arterieller Hypertonus, Vorhofflimmern, Herzinsuffizienz oder Nierenfunktionsstörungen gehen häufig mit erhöhten Troponinwerten einher. Hier bleibt die Differenzialdiagnostik eine klinische Herausforderung.
Für einen akuten Myokardinfarkt spricht vor allem ein relevanter Anstieg des Troponins in einer seriellen Messung. Aber was gilt als "relevant"? Diese Definition ist derzeit Gegenstand intensiver Diskussionen. Einzelne Protokolle lassen sich aber schon im klinischen Alltag anwenden [8, 11, 13].
Der "Sofortausschluss" eines Myokardinfarkts
Neuere Untersuchungen legen nahe, dass man schon durch einmalige Troponin-Messung bei einem Großteil der Patienten mit akutem Brustschmerz einen Myokardinfarkt ausschließen kann. So konnte in einer Studie bei 28 % aller Brustschmerzpatienten durch ein Troponin I von unter3 ng/l direkt bei Aufnahme und ein EKG ohne Hinweise auf Ischämie mit an Sicherheit grenzender Wahrscheinlichkeit ein Herzinfarkt ausgeschlossen werden [14].
Für die nahe Zukunft ist vorstellbar, dass sogenannte Troponin-Schnelltests ("Point-of-Care-Assays") eine mit den aktuellen hoch-sensitiven Labortests vergleichbare Sensitivität erreichen [12]. Dies ist für den klinischen Alltag sehr bedeutsam, da unter der Voraussetzung einer kurzen Analysedauer von maximal 20 bis 30 Minuten ein rascher Ausschluss eines Myokardinfarkts auch in der ambulanten Praxis möglich ist. So können zügige und präzise Ausschlussdiagnosen bereits ambulant erzielt und so die kontinuierlich steigenden Belastungen der Notaufnahmen durch Patienten mit Brustschmerzen und niedrigem Risiko für das Vorliegen eines Herzinfarkts reduziert werden. Aktuell erreicht jedoch keines der auf dem Markt verfügbaren Geräte die entsprechende diagnostische Güte.
Ambulante und stationäre Vernetzung
Bei akuten Brustschmerzen ist die zügige weitere Diagnostik und Therapie entscheidend. Für Patienten, die sich zunächst in der Hausarztpraxis vorstellen, empfiehlt sich eine direkte Kontaktaufnahme mit der weiterversorgenden Klinik. Die klinische Einschätzung des betreuenden Hausarztes inklusive der erhobenen Befunde kann das weitere Prozedere in hohem Maße beschleunigen. Den Kontakt zu den weiterbehandelnden Kollegen sollte man deshalb immer aufnehmen. Die 256 "Chest Pain Units", die von der Deutschen Gesellschaft für Kardiologie zertifiziert wurden, eignen sich besonders für die Einweisung. In diesen CPUs werden Patienten mit akuten Brustschmerzen nach einem hochstandardisierten Ablauf versorgt – und das 24 Stunden an 365 Tagen im Jahr [15]. Informationen zu den Kliniken mit CPU findet man im Netz unter http://cpu.dgk.org/.
Interessenkonflikte: Der Autor hat keine deklariert
Erschienen in: Der Allgemeinarzt, 2018; 40 (4) Seite 18-21