Sie sind ein Graus für jeden (Hoch-)Leistungssportler: kardiale Arrhythmien. Herzrhythmusstörungen können nicht nur empfindlich an der sportlichen Leistung rütteln, sondern auch die Lebensqualität deutlich senken, für die Training und erfolgreiche Wettkampfteilnahme maßgeblich sind. Bedrohliche Rhythmusstörungen führen vereinzelt sogar zum Ausschluss vom Leistungs- oder Profisport – für den Sportler eine existenzielle Bedrohung. Möglicherweise kann ein intensives Ausdauertraining Arrhythmien sogar begünstigen. Für diese These fehlen bislang aber zuverlässige prospektive Studiendaten. Es gilt daher, für diese Patientengruppe schnellstmöglich eine effektive Therapie in die Wege zu leiten.
Supraventrikuläre Rhythmusstörungen
Supraventrikuläre Rhythmusstörungen sind selten prognostisch relevant, können aber zu psychischen Belastungssituationen führen, denn der Leistungssport stellt meist den Lebensmittelpunkt der Patienten dar [10, 17, 3]. Bei Leistungssportlern sind zudem Betablocker und Antiarrhythmika wie Flecainid, Propafenon, Dronedaron und Amiodaron aufgrund der negativen Ino- und Chronotropie (eingeschränkte Herzfrequenzadaptation und reduzierte Kontraktilität), der belastungsinduzierten Elektrolytverschiebung und des Proarrhythmierisikos kontraindiziert.
Sportler sollte man daher früh einer Katheter-ablation zuführen. Die Komplikationsraten sind an erfahrenen Zentren niedrig (vgl. Tabelle 1). Das Training ist in der Regel wenige Tage nach dem Eingriff wieder möglich. Eine mindestens zweimonatige Antikoagulation nach Eingriffen bei Vorhofflimmern (linksatriale Vorhofflimmer-Ablation) ist hier wichtig.
Präexzitation/WPW-Syndrom
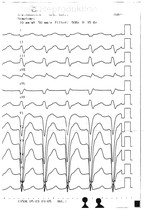
Eine "offene" akzessorische Leitungsbahn im Sinne einer Präexzitation (dokumentiert im Oberflächen-EKG) ist ein klassischer Befund des Wolff-Parkinson-White-(WPW-)Syndroms (mit paroxysmalem Herzrasen) und geht bei Vorhofflimmern und entsprechend schneller Überleitung via akzessorischer Leitungsbahn mit einem erhöhten plötzlichen Herztod-Risiko einher. Die Inzidenz für ein WPW-Syndrom liegt bei 0,1 – 0,3 %. Die Diagnose lässt sich einfach anhand eines EKGs stellen (Abb. 3). Wegen der Anstrengung im Wettkampf und Training sollte man hier früh mit der invasiven Diagnostik (elektrophysiologische Untersuchung und Ablation) beginnen, die ein extrem niedriges Komplikationsrisiko hat und sehr effektiv ist. Dies sollte aber mit dem Athleten diskutiert und von erfahrenen Zentren vorgenommen werden.
Ventrikuläre Rhythmusstörungen
Ventrikuläre Rhythmusstörungen können – im Gegensatz zu supraventrikulären – Vorboten des gefürchteten plötzlichen Herztods bei Sportlern sein. Wichtig ist hier eine korrekte Risikostratifikation. Der Ausschluss einer strukturellen Herzerkrankung durch Anamnese mit Familienanamnese, 12-Kanal-Ruhe- und Belastungs-EKG, Echokardiographie und eventuell Kardio-MRT oder gegebenenfalls invasiver Abklärung ist entscheidend für die Ausschlussdiagnose einer idiopathischen gutartigen ventrikulären Rhythmusstörung. Zudem muss man angeborene Ionenkanal-Erkrankungen wie das Long-QT-Syndrom, das Brugada-Syndrom oder die polymorphe katecholaminerge ven-trikuläre Tachykardie ausschließen. Die Rhythmusstörungen können als monomorphe oder polymorphe ventrikuläre Extrasystolen bis zu Triplets oder Salven auftreten. Eine anhaltende Kammertachykardie liegt vor, wenn die ventrikuläre (monomorphe oder polymorphe) Rhythmusstörung länger als 30 Sekunden anhält.
Bei idiopathischen Rhythmusstörungen, d. h., wenn eine strukturelle Herzerkrankung fehlt, ist von einer guten Prognose ohne erhöhtes Herztodrisiko auszugehen. In erster Linie sollte man bei idiopathischen ventrikulären Rhythmusstörungen die interventionelle Ablationstherapie zur Elimination der Rhythmusstörung durchführen. Die Erfolgsraten der Katheterablation sind bei diesen Herzrhythmusstörungen gut (vgl. Tabelle 2). Bei polymorphen ventrikulären Rhythmusstörungen sollte zunächst die zugrunde liegende Herzerkrankung behandelt werden.
Bei einer strukturellen Herzerkrankung ist ebenfalls eine interventionelle Katheterablation zur Verbesserung der Symptomatik und Rezidivreduktion empfehlenswert. Sie hat aber keinen Einfluss auf die Prognose, die im Wesentlichen durch die kardiale Grunderkrankung determiniert wird. Prinzipiell sollte der Arzt bei relevanter struktureller Herzerkrankung entsprechend den Leitlinien ein Wettkampf-, aber kein generelles Sportverbot aussprechen. Zur Orientierung kann man die Leitlinie der europäischen Gesellschaft für Kardiologie heranziehen [13].
Bei professionellen Hochleistungssportlern kann ein Wettkampf- beziehungsweise Sportverbot zu Existenzproblemen führen und schwere psychische Veränderungen mit sich bringen. Darüber hinaus gibt es Hinweise, dass auch bei Hochleistungssportlern mit bekannten Herzerkrankungen und mit implantierten Defibrillatoren ein Fortsetzen des Hochleistungssports sicher ist. In einer Arbeit von 2013 wurden Sportler mit implantiertem Defibrillator und fortgesetztem Hochleistungssport begleitet. Von 372 Personen verstarben zwei Sportler während eines Follow-ups von 31 Monaten, ein Sportler am Schreibtisch und der zweite während einer Hospitalisierung. [8] Dies hat Diskussionen angestoßen, die Leitlinien von 2005 neu zu überarbeiten. Entscheidend erscheint die frühzeitige Erkennung eines möglicherweise erhöhten Risikos bei Leistungssportlern und die dann adäquate Diagnostik und Therapie.
Häufigere Herzrhythmusstörungen?
Durch Ausdauersport kann man die Gesamt-, die kardiovaskuläre und die onkologische Mortalität senken. Es ließ sich auch nachweisen, dass die Mortalitätsreduktion mit der Intensität der sportlichen Tätigkeit korreliert [15]. Ebenso konnte man dokumentieren, dass eine Gewichtsreduktion mit Steigerung der Fitness die Inzidenz z. B. von Vorhofflimmern reduziert und die Effektivität der Katheterablation des Vorhofflimmerns über ein Follow-up von fünf Jahren deutlich erhöht wird [11, 12]. Es gibt aber auch retrospektive Analysen, die zeigen, dass bei intensivem Ausdauertraining die Mortalität sowohl bei Patienten mit Herzerkrankung als auch bei Freizeitsportlern wieder ansteigt. Es wird hier ein Grenzwert von 7,2 MET/d bei herzkranken Sportlern angegeben [9, 16].
- Supraventrikuläre Rhythmusstörungen sollten beim Leistungssportler zügig der Katheterablation zugeführt werden. Für eine medikamentöse Therapie besteht keine Indikation.
- Idiopathische benigne ventrikuläre Rhythmusstörungen sollten ebenfalls einer Katheterablation zugeführt werden, für eine medikamentöse Therapie besteht keine Indikation.
- Zur Abklärung und Definition einer benignen ventrikulären Rhythmusstörung gehören – neben einer ausführlichen Anamnese und Familienanamnese – ein 12-Kanal-EKG, ein 12-Kanal-Belastungs-EKG, eine Echokardiographie, ein Kardio-MRT und in Einzelfällen ein Links-Rechtsherzkatheter.
- Bei malignen ventrikulären Rhythmusstörungen muss die kardiale Grunderkrankung optimal behandelt werden, in Einzelfällen ist auch eine Katheterablation zur Verbesserung der Symptomatik erforderlich. Es besteht prinzipiell ein Wettkampf-, kein Sportverbot. Die Sportempfehlungen bei Herzerkrankung mit malignen Rhythmusstörungen sollten den europäischen Leitlinien entnommen werden.
- In Einzelfällen wird ein intensives und langjähriges Ausdauertraining als proarrhythmogen diskutiert.
Retrospektive Analysen weisen darauf hin, dass langjähriges, intensives Ausdauertraining unter bestimmten Bedingungen das Vorhofflimmern oder das Vorhofflattern begünstigt. So zeigt sich bei Skilangläufern eine Korrelation zwischen dem Auftreten von Vorhofflimmern und der Schnelligkeit bzw.der absolvierten Anzahl an Wettkämpfen [2].
Ebenso gibt es Hinweise, dass Vorhofflattern häufiger bei Ausdauersportlern mit sehr langen Trainingszeiten auftritt [5]. Eine Metaanalyse kommt zu dem Ergebnis, dass Hochleistungssportler ein fünffach erhöhtes Risiko für Vorhofflimmern haben [1].
Auch ventrikuläre Rhythmusstörungen scheinen bei exzessiv langen Belastungsphasen über viele Jahre getriggert zu werden. Als Ursache wird bei Sportlern eine schlechtere rechtsventrikuläre Funktion während der Ausdauerbelastung diskutiert. Es kann zu einer Fibrosierung des rechten Ventrikels kommen, die wiederum die Voraussetzung für ventrikuläre Arrhythmien ist [7]. Diese Beobachtungen wurden jedoch nur bei kleinen Kohorten von Extremsportlern mit eingeschränkter RV-Funktion unter Belastung gemacht. Damit müssen diese retrospektiven Analysen und auch Einzelfälle überdacht werden. Prospektiv randomisierte Studien sind hier wohl nicht zu erwarten.
Interessenkonflikte: Die Autorin hat keine deklariert.
Erschienen in: Der Allgemeinarzt, 2019; 41 (7) Seite 46-50