Zungenbrennen beschreibt eine komplexe Beschwerdesymptomatik, die in der Literatur unterschiedliche Bezeichnungen aufweist, wie z. B. "Burning tongue", "Glossodynia", oder "Stomatopyrosis". Im Verlauf hat sich der Begriff Burning Mouth Syndrome (BMS) durchgesetzt.
Die Internationale Kopfschmerzgesellschaft [1] definiert BMS als intraorales Brennen oder Empfindungsstörung (Dysästhesie), das täglich für mehr als zwei Stunden über drei Monate auftritt ohne klinisch nachweisbare ursächliche Veränderungen. Diese Art der Definition erinnert an die Definitionen des Reizdarmsyndroms (IBS) [2]. Auch hier liegen definierte Beschwerden vor, für die sich keine fassbaren Ursachen finden lassen. Beim IBS ist nun bewiesen, dass organische Ursachen zugrunde liegen und dass zahlreiche Subgruppen mit unterschiedlichen Pathophysiologien vorliegen [3, 4, 5]. Eine ähnliche Konstellation ist auch beim BMS zu vermuten. Typische Symptome sind das Gefühl des Brennens, Stechens bzw. Juckens, das überwiegend im Bereich der Zunge und der Lippen, weniger im Bereich der Wangenschleimhaut lokalisiert wird [6]. Häufig finden sich assoziierte Beschwerden wie ein bitterer oder metallischer Geschmack (60 %), Geschmacksstörungen (35 %) bzw. das Gefühl der Mundtrockenheit (Xerostomie, 63 %). Der Beginn ist spontan ohne erkennbare auslösende Ursachen. BMS kommt je nach betreuender Fachdisziplin und untersuchtem Patientenkollektiv häufiger vor, wobei die Prävalenzdaten aufgrund des wahrscheinlich sehr heterogenen Patientenkollektivs in der Literatur mit einer großen Variation von 0,7 – 15 % angegeben werden [7]. Das mittlere Alter beträgt 27 – 87 Jahre, wobei insbesondere peri- bzw. postmenopausale Frauen prädisponiert sind. Es besteht ein hoher Leidensdruck, auch weil die Patienten häufig nicht ernst genommen werden und hierdurch hohe indirekte und direkte Kosten im Gesundheitssystem entstehen.
Anatomie der Mundhöhle
Das Epithel der Mundhöhle besteht aus nicht verhornendem Plattenepithel, das durch das Sekret der Speicheldrüsen befeuchtet wird. Die somatosensorische Innervation der Mundschleimhaut erfolgt durch den N. trigeminus (V) und den N. glossopharyngeus (IX). Die vorderen zwei Drittel der Zunge werden durch den N. mandibularis des N. trigeminus, das hintere Drittel durch den N. glossopharyngeus (IX)versorgt. Hierdurch werden die über die Zungenpapillen aufgenommenen mechanischen, thermischen bzw. taktilen Reize weitergeleitet. Die Geschmacksrezeptoren der vorderen zwei Drittel der Zunge werden über die Chorda tympani des N. facialis (VII), die des hinteren Zungendrittels über den N. glossopharyngeus (IX) übertragen. Geschmacksrezeptoren finden sich auch am weichen Gaumen und im Larynx (N. laryngeus des N. vagus) [6].
Klassifikationen
Naturgemäß sind Klassifikationen von Erkrankungen, deren Ursachen noch unklar sind bzw. die aus mehreren Subgruppen bestehen, artifiziell. Auch beim BMS gibt es Versuche einer Klassifizierung. Diese beinhalten zum einen die pragmatische Differenzierung zwischen primär ohne erkennbare Ursache und sekundär mit auslösenden Ursachen bzw. eine Einteilung bezogen auf die Symptomatik.
Ein sekundäres BMS kann u. a. assoziiert sein mit Schilddrüsenerkrankungen (Unterfunktion), Diabetes mellitus, gastrointestinalen bzw. urogenitalen Erkrankungen, psychiatrischen Erkrankungen (u. a. Depression, Ängstlichkeit, Hypochondrie), Persönlichkeitsveränderungen (Cluster-A-Störungen), M. Parkinson, Mundinfektionen (Candida-Spezies, coliforme Enterobacter, Klebsiella), Medikamenten (ACE-Hemmer, Angiotensin-Rezeptor-Hemmer, Nevirapin, Efavirenz, Levodopa, Topiramat), Zahnbehandlungen, Vitaminmangel (B1, B2, B6, B12, Folsäure), Mineralienmangel (Zink) bzw. Nikotin. Der Versuch einer Klassifikation anhand der Symptomatik suggeriert unterschiedliche Pathophysiologien, für die es aber keine validen Daten gibt (Tabelle 1).
Ätiologie und Pathogenese
Die Pathophysiologie des BMS ist weiterhin ungeklärt. Favorisiert wird heute eine Neuropathie, wobei diskutiert wird, ob eine periphere oder zentrale Manifestation vorliegt (Tabelle 2). Wahrscheinlich gibt es, abhängig vom Patientenkollektiv, beide Formen, möglicherweise auch kombiniert. Für eine periphere sensorische Neuropathie/Axonopathie der kleinen sensorischen Nervenfasern im Mund (50 – 60 %) bzw. des N. trigeminus (20 – 25 %) sprechen erniedrigte Schwellen für Temperatur-Schmerzreize, eine erniedrigte Dichte epithelialer bzw. subpapillärer Nerven, eine axonale Degeneration, erhöhte Spiegel von Nerve Growth Factor (NGF), eine erhöhte Dichte von TRPV1-Ionenkanälen und P2X3-Rezeptoren auf Nervenfasern, eine Dysfunktion der Chorda-tympani-Äste des N. facialis, Veränderungen des Blinzelreflexes, ein positiver Einfluss durch Stimulation des Geschmackssystems bzw. ein Abfall neuroprotektiver gonadaler und adrenaler Steroide in der Menopause. Auf eine zen-trale Neuropathie (20 – 30 %) deuten eine veränderte zentrale Reizverarbeitung (Schmerz, Temperatur) im Thalamus (fMRT), eine Dysregulation des nigrostriatalen dopaminergen Systems (M. Parkinson) bzw. erhöhte Scores für Ängstlichkeit und Depression (50 % der Patienten) hin [6, 8, 9].
Klinische Diagnostik
Die klinische Diagnostik ist immer noch eine Herausforderung, da es keine allgemein akzeptierten Kriterien gibt, die klinische Symptomatik variabel sein kann und ein heterogenes Patientenkollektiv vorliegt [10]. Ein BMS kann vermutet werden, wenn eine täglich auftretende bilaterale brennende Missempfindung der Mundschleimhaut von kontinuierlicher oder zunehmender Intensität über mindestens vier bis sechs Monate vorliegt, die nicht durch Nahrungs- bzw. Flüssigkeitszufuhr verschlechtert, sondern eher verbessert wird und schlafunabhängig ist [11]. Zusätzliche Kriterien sind Geruchsveränderungen und/oder Xerostomie, Alterationen der sensorischen bzw. chemosensorischen Empfindung bzw. psychopathologische Auffälligkeiten [12].
Da das primäre BMS eine Ausschlussdiagnose ist, müssen im Einzelfall alle sekundären Ursachen abgeklärt werden (Tabelle 2). Hierzu gehören u. a. eine ausführliche Inspektion des Nasen-Rachen-Raums, des Zahnstatus, eine Ernährungsanamnese bzw. eine Medikamentenanamnese. Die Laboruntersuchungen sollten einen Mangel an Eisen, Spurenelementen, Vitamin B1, B12, einen Diabetes mellitus bzw. autoimmune Erkrankungen ggf. aufdecken können. Auch kann eine Messung des Speichelflusses hilfreich sein. Gegebenenfalls kann ein Abstrich der Mundschleimhaut auf Bakterien bzw. Pilze Aufschluss geben.
Therapie
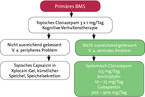
Die Therapie des BMS ist schwierig und individuell [13]. Primäres Ziel ist die Differenzierung zwischen primären und sekundären Formen (Tabelle 2). Dies bedeutet im Einzelfall, dass anhand einer Checkliste die potenziellen sekundären Faktoren in der Hoffnung einer kausalen Therapiemöglichkeit abgearbeitet und behandelt werden müssen [14, 15]. Dies ist wie bei den funktionellen Darmerkrankungen naturgemäß zeit- und kostenintensiv. Die medikamentösen Therapiestrategien sind zahlreich und werden durch das heterogene Patientenkollektiv bestimmt (Tabelle 3). Nach Ausschluss der sekundären Formen mit entsprechender spezifischer Therapie können unter dem V. a. ein primäres BMS verschiedene Therapiekonzepte versucht werden. Hierbei gibt es zzt. keinen Biomarker, der ein Therapiekonzept im Vorfeld favorisiert. Eine praktikable Therapiestrategie wurde von Kääskeläinen et al. [10] vorgeschlagen (Abbildung). Bei der Therapieentscheidung sollte ein unnötiger Aktionismus vermieden werden. So zeigen Untersuchungen, dass der Verlauf ohne Therapie über 18 Monate in 10 % eine spontane Remission und in 26 % eine moderate Besserung zeigt. 37 % der Patienten zeigen keine Änderung, 26 % eine Verschlechterung ihrer Symptomatik. Diese Ergebnisse sind formal nicht schlechter als der Verlauf mit Therapie über 18 Monate 29 % Besserung, 56 % keine Änderung, 15 % Verschlechterung [16].
Prognose
Obwohl nur wenige Follow-up-Studien vorliegen, ist davon auszugehen, dass eine "Dreierregel" gilt. Dies bedeutet, dass ca. 30 % der Patienten eine spontane Remission bzw. eine Verbesserung ihrer Symptome aufweisen werden, dass ein weiteres Drittel keine Änderung und ein weiteres Drittel eine Verschlechterung ihrer Beschwerden zeigen wird.
Was interessiert den Gastroenterologen?
Patienten mit BMS werden dem Gastroenterologen häufig unter dem V. a. eine gastroösophageale Refluxerkrankung vorgestellt. Dies ist aber bei Fehlen von typischen Refluxbeschwerden (Sodbrennen, saure Regurgitation) unwahrscheinlich, sodass im Allgemeinen keine weiterführende Refluxdiagnostik durchgeführt werden muss. Bei klinischen Hinweisen auf eine Refluxerkrankung, insbesondere bei Volumenreflux bzw. hohem Reflux, kann eine Ösophagogastroskopie zum Nachweis einer Refluxösophagitis bzw. eine Ösophagusfunktionsdiagnostik durch kombinierte 24-Stunden-pH-Metrie-Impedanzmessung durchgeführt werden. Der Stellenwert der oropharyngealen Säuremessung durch die Restech®-Sonde ist zzt. unklar [17, 18]. Erfahrungen bei der Funktionsuntersuchung von Globusgefühl bzw. Halsbrennen lassen aber vermuten, dass diese spezialisierte Funktionsdiagnostik ohne klinische Relevanz ist. Entsprechende wissenschaftlich validierte Daten liegen aber zzt. nicht vor. Ebenfalls fehlen Untersuchungen über die Relevanz von Magenschleimhaut-Heterotopien im proximalen Ösophagus bzw. die Bedeutung einer eosinophilen Ösophagitis. Diese Faktoren sollten aber im Einzelfall ausgeschlossen werden.
Prof. Dr. med. Thomas Frieling
Interessenkonflikte: Der Autor hat keine deklariert
Erschienen in: Der Allgemeinarzt, 2019; 41 (4) Seite 42-45