Phantomschmerzen gehen für betroffene Patienten mit einer ausgeprägten Beeinträchtigung der Lebensqualität einher. Die pathophysiologische Ursache von Phantomschmerzen kann in peripheren Nerven, im Rückenmark und im Gehirn lokalisiert werden. In den letzten Jahren hat vor allem die Erforschung der veränderten Hirnfunktionen neue Impulse zur Therapie gesetzt.
Offenbar kommt es bei Phantomschmerzen zu einer Störung der Wahrnehmung aus der betroffenen Körperregion. Erste Untersuchungen haben gezeigt, dass diese Störung durch eine verbesserte visuelle Kontrolle behoben werden kann. Bei Phantomschmerzen kann diese durch Spiegelung der gesunden Extremität erleichtert werden. Die Wiederherstellung der ungestörten Wahrnehmung der Extremität geht häufig mit einem Sistieren der Phantomschmerzen einher. Andere Behandlungsansätze, die auf veränderte Nervenfunktionen und die Schmerzweiterleitung im Rückenmark abzielen, haben in Studien selten überzeugt. Der Grund: Die Patienten, die von der Behandlung profitieren, können nicht anhand eindeutiger klinischer und apparativer Tests identifiziert werden. Oft bleibt hier nur der Ausweg einer Probebehandlung. Im Ergebnis können nur jene pharmakologischen Behandlungen empfohlen werden, die sich im Einzelfall als wirksam erwiesen haben. Unwirksame Therapien können und sollen beendet werden. Dabei muss man aber die Möglichkeit im Blick haben, dass einzelne Behandlungskomponenten für sich genommen zwar nicht ausreichend effektiv Schmerzen lindern, im Zusammenspiel mit anderen Verfahren aber ein Baustein der Schmerztherapie sein können. In diesem Sinne sind Phantomschmerzen, ähnlich wie viele andere Formen chronischer Schmerzen, letztlich multimodal zu behandeln. Besser als eine gelungene Behandlung kann nur die Prophylaxe sein.
Das Problem Phantomschmerz
"Es ist, als wenn jemand ein glühendes Eisen in meinen Unterschenkel bohrt und es dann langsam hin und her dreht. Aber der Unterschenkel ist gar nicht mehr da." In so bildlicher Sprache berichtete ein Motorradfahrer über die Schmerzen, die er nach dem traumatischen Verlust der distalen unteren Extremität entwickelt hatte.
Phantomschmerzen werden sehr unterschiedlich beschrieben: brennend, stechend, einschießend, bohrend, elektrisierend. Das Kriterium für die Diagnose ist die Lokalisation. Phantomschmerzen werden in einer Körperregion angegeben, die nicht mehr vorhanden ist. Patienten, die sich in einer Schmerzambulanz vorstellen, geben die Intensität der Schmerzen häufig mit sehr hohen Werten an, z. B. auf einer numerischen Analogskala von 0= kein Schmerz bis 10 = maximal vorstellbarer Schmerz mit maximal 9.
Trotz vieler Fortschritte in der schmerzmedizinischen Forschung sind Phantomschmerzen bis heute schwierig zu behandeln. Die Empfehlungen sind eher unspezifisch. Auch der Einsatz stark wirksamer Opioide wie Morphin, Oxycodon, Hydromorphon, Levomethadon, Fentanyl oder Buprenorphin ist bei Phantomschmerzen nicht immer von Erfolg gekrönt.
Pathophysiologie
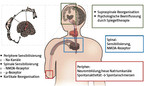
Der Verlust einer Extremität zieht Veränderungen auf unterschiedlichen Ebenen der Schmerzwahrnehmung nach sich (vgl. Übersicht 1) [1]. Nach der Durchtrennung eines gemischten peripheren Nervens kommt es zu Regenerationsvorgängen. In den proximalen verbleibenden Nervenfasern wird die Proteinbiosynthese mit dem Ziel angeregt, die Nervenfaser wieder wachsen zu lassen. Im Rahmen dieses Prozesses kann es zu fehlerhaften Verbindungen unterschiedlicher Nervenfasern kommen. So kann die Verbindung einer Faser des sympathischen Nervensystems mit sensorischen C-Fasern Schmerzen bei Aktivierung des sympathischen Nervensystems auslösen. Die Anbindung einer sensorischen A-ß-Faser mit einer C-Faser kann Schmerzen bei geringen Berührungen erklären. Darüber hinaus werden im Zuge der Nervenfaser-Regeneration vermehrt Natriumkanäle im Soma des peripheren Nervens produziert und in die Peripherie transportiert. Dort können sie eine Spontandepolarisation von Schmerzfasern auslösen. Da diese Natriumkanäle nicht immer durch Natriumkanal- Antagonisten, z. B. Carbamazepin oder Lidocain, gehemmt werden können, ist die Behandlung zurzeit noch schwierig. Hier liegt aber ein Ziel für zukünftige Entwicklungen der pharmakologischen Forschung.
Im Rückenmark kommt es infolge der ausgeprägten Depolarisation nach der Nervendurchtrennung zu verschiedenen Veränderungen, die mit einer Sensibilisierung der postsynaptischen Nervenfaser einhergehen. Der erregende Transmitter Glutamat löst über eine Bindung am N-Methyl-D-Aspartat-Rezeptor (NMDA-R) eine Kaskade von Veränderungen in der postsynaptischen Zelle aus, an deren Ende eine Steigerung des intrazellulären Kalziums und der Proteinbiosynthese steht. Diese weist auf die schmerzbedingte strukturelle Änderung der Funktion der Nervenzelle hin: Es kommt zu einer Sensibilisierung, d. h. die Nervenfaser kann durch Reize mit geringerer Schwelle depolarisiert werden und so die Information "Schmerz" weiterleiten, die unter physiologischen Bedingungen gehemmt würde.
Dieser Prozess ist das Ziel einer Vielzahl von therapeutischen Interventionen. Dazu zählen die Hemmung des NMDA-Rezeptors, die Hemmung des Kalziumeinstroms, Aktivierung von µ-Rezeptoren, α2-Rezeptoren und anderen.
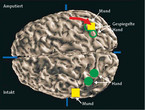
Die Veränderungen im Gehirn konnten erst mit der funktionellen Kernspintomographie und der Positronen-Emissions-Tomographie genauer erforscht werden. Bei Patienten mit Phantomschmerzen konnte eine Veränderung der topischen Zuordnung von Reizen aus Körperregionen nachgewiesen werden. So vergrößerte sich die Region, die durch eine somatische Reizung der Lippen ausgelöst wurde, im Kortex (Abb. 1). Daher spricht man hier von einer kortikalen Reorganisation. Für sich genommen wäre dieser Befund kein Beweis für einen kausalen Zusammenhang. Jedoch konnten weitere Untersuchungen zeigen, dass eine erfolgreiche Schmerzbehandlung mit einer Wiederherstellung der kortikalen Somatotopie einherging [2, 3]. Dabei scheint es zu einer Veränderung der schmerzbezogenen Aufmerksamkeit zu kommen. Insofern besteht hier offenbar eine Möglichkeit, mit psychologischen Techniken letztlich somatische Hirnfunktionen zu beeinflussen.
Therapie von Phantomschmerzen
Lange stand in der Therapie von Phantomschmerzen die pharmakologische Behandlung im Vordergrund. Aber auch verschiedene Verfahren der Physiotherapie wurden angewandt. In kontrollierten Studien wurde untersucht, ob eine generelle Schmerzlinderung erwartet werden kann. Die Ergebnisse sind widersprüchlich.
Pharmakologische Behandlung
Die Behandlung von Phantomschmerzen mit dem Natriumkanalantagonisten Mexiletin verminderte zwar die Schmerzintensität. Der Effekt war aber dem Plazebo nicht überlegen [4]. Mexiletin muss zudem unter Beachtung des Risikos maligner Rhythmusstörungen (Torsade de pointes) eingesetzt werden.
Morphin war in dieser Studie dem Plazebo überlegen [4]. Dieser Befund bestätigte eine frühere Fallserie, die auch gezeigt hatte, dass Zeichen der kortikalen Reorganisation unter erfolgreicher Behandlung mit Morphin rückläufig waren [2]. Dennoch betrug die Rate von Respondern, d. h. Patienten mit einer Schmerzreduktion von mindestens 50 % vom Ausgangswert, auch hier nur 42 % (im Vergleich zu Plazebo mit 8 %). Im Langzeitverlauf scheint die analgetische Wirkung der Opioide bei Phantomschmerzen jedoch nicht immer bestehen zu bleiben [5].
Um die Sensibilisierung im Rückenmark zu verhindern oder wieder zu reduzieren, wurden NMDA-Rezeptor-Antagonisten eingesetzt. Dazu zählen Memantine, Ketamin und Dextromethorphan. Keine dieser Substanzen führte zu einer generell nachweisbaren Reduktion von Phantomschmerzen [6]. Anders als im Tierexperiment, wo die Gabe von NMDA-Rezeptor- Antagonisten vor Amputation zu einer Reduktion der Zeichen von Phantomschmerzen führt, scheint diese Behandlung bei bereits etablierten Phantomschmerzen nicht hilfreich zu sein.
Unter den Antikonvulsiva konnte für Gabapentin eine Schmerzlinderung nachgewiesen werden [6]. Ähnlich wie bei den Opioiden muss man jedoch davon ausgehen, dass dieser Effekt nicht zuverlässig bei allen Patienten zu verzeichnen ist, sondern nur bei einer Untergruppe. Ein Therapieversuch mit Gabapentin(oiden) oder Morphin (oder Opioiden) ist sinnvoll; bei fehlendem Erfolg ist diese Therapie aber auch wieder zu beenden. Eine kritische Erfolgskontrolle sollte von Beginn an geplant werden.
Physiotherapie
Die Behandlung mit einem Strumpf, der als faradischer Schutz des Stumpfes dienen sollte, war in einer kontrollierten Untersuchung dem Plazebo-Strumpf nicht überlegen [7]. Auch die transkutane elektrische Nervenstimulation TENS konnte nicht überzeugen [8], wenngleich hier die Technik der Stimulation im Einzelnen sehr unterschiedlich sein kann. In einer neueren Untersuchung war TENS ähnlich wirksam wie Spiegeltherapie [9]. Die physiotherapeutische Behandlung mit Strom könnte im Einzelfall eine sinnvolle Ergänzung in der Behandlung von Phantomschmerzen sein.
Botulinustoxin
In einer Untersuchung an sieben Patienten konnte gezeigt werden, dass die Injektion von Botulinustoxin an Triggerpunkte im Stumpfbereich zu einer Reduktion von Restschmerz und Phantomschmerzen führen kann [10]. Der Grund für die Schmerzlinderung durch Botulinustoxin könnte darin liegen, dass die Depolarisation peripherer Nerven gehemmt wird. Dies könnte auch bei nicht vollständiger Schmerzausschaltung ein Baustein in der Therapie von Phantomschmerzen werden.
Psychologisch fundierte Behandlungsverfahren
Psychologische Behandlungsverfahren, die speziell für Phantomschmerzen entwickelt wurden, zielen auf die Beeinflussung der kortikalen Reorganisation der Schmerzwahrnehmung. In einer bedeutenden Arbeit konnten Flor und Mitarbeiter zeigen, dass durch ein Wahrnehmungstraining die Veränderungen der kortikalen Wahrnehmungsorganisation, d. h. der topischen Zuordnung von Reizlokalisation und Erregung des sensiblen Kortex, normalisiert werden können. Mit der Wiederherstellung der physiologischen Bedingungen ging die Reduktion der Phantomschmerzen einher [3]. In einer kontrollierten Untersuchung konnte bestätigt werden, dass eine Spiegeltherapie in nur vier Wochen zu einer gravierenden Reduktion von Phantomschmerzen führt [11].
Weit verbreitet ist eine abgestufte Behandlung, die schrittweise Seitendiskriminierung, Imagination und schließlich Spiegeltherapie (Graded Motory Imagery) einsetzt. Auch für dieses Verfahren liegen positive Befunde bei Phantomschmerzen vor [12].
Offenbar sind in der Therapie der Phantomschmerzen vor allem im Bereich der psychologisch fundierten Behandlung gravierende Fortschritte in den letzten Jahren erzielt worden. Dennoch sind pharmakologische Behandlungen weiterhin ein Bestandteil der Therapie, auch wenn die Effektivität im Einzelfall kritisch überprüft werden sollte.
Prophylaxe
Besser als die Behandlung könnte jedoch die Prophylaxe sein. In der Regel haben jedoch nur der Chirurg und sein Freund, der Anästhesist, die Möglichkeit, prophylaktische Maßnahmen einzuleiten. Regionalanästhesieverfahren in der perioperativen Phase können die Intensität von Phantomschmerzen reduzieren, sie können sie aber nicht ganz vermeiden [13]
Interessenkonflikte: Der Autor hat keine deklariert.
Erschienen in: Der Allgemeinarzt, 2017; 39 (8) Seite 54-60