Ein Delir kann sich unterschiedlich äußern und wird aufgrund der wechselnden Symptomatik nicht immer erkannt. Dies gilt insbesondere für das häufigere hypoaktive Delir. Die Ursachen sind vielfältig. Bei alten Menschen spielt bei den Auslösern oft die Demenz eine Rolle. Auch Infektionen und Medikamentennebenwirkungen sind zu nennen. Der Schwerpunkt des folgenden Beitrags soll auf der Therapie liegen und hierbei die Besonderheiten der einzelnen Antipsychotika beleuchten. Bei der Entscheidung für eine bestimmte Substanz sind vorherrschende Symptome und Begleiterkrankungen zu berücksichtigen.
Das Delir ist eine Störung von Bewusstsein, Aufmerksamkeit und Wahrnehmung. Der Beginn ist meist akut und der Verlauf typischerweise fluktuierend. Das hyperdyname (= „laute“) Delir ist gekennzeichnet durch exzitatorische psychomotorische Symptome. Schwieriger zu erkennen ist das hypodyname (= „leise“) Delir, bei dem die Psychomotorik stark gehemmt ist (vgl. Übersicht 1). Die Depression ist differenzialdiagnostisch nicht immer leicht abgrenzbar, zumal affektive Störungen auch beim Delir vorkommen. Häufig werden Mischformen beider Delirtypen beobachtet. Für die Umgebung belastend sind Störungen des Schlaf-Wach-Rhythmus („Sundown-Syndrome“). Aufgrund der wechselnden Symptomatik werden Delirien häufig (bis zu 60 %) nicht erkannt, was insbesondere für die hypodyname Form gilt [1, 2].
Synonyme wie Durchgangssyndrom, hirnorganisches Psychosyndrom (HOPS) o. Ä. sollten nicht verwendet werden, da sie die Bedeutung der Erkrankung tendenziell verharmlosen. Es handelt sich um eine ernste Störung mit deutlich erhöhter Mortalität. Sie ist kurzfristig massiv gesteigert (bis 20-fach) und langfristig verdoppelt [3]. Das Delir ist grundsätzlich reversibel, Defektheilungen sind jedoch möglich. Jedes Delir muss aufgrund der ernsten Konsequenzen als medizinischer Notfall angesehen werden.
Die Ursachen eines Delirs sind altersabhängig verschieden. Bei älteren Menschen muss in ca. 50 % von einer multifaktoriellen Genese ausgegangen werden [4], in etwa gleichem Ausmaß ist eine Demenz eine von mehreren auslösenden Faktoren [5]. Besonders häufig wird ein Delir ausgelöst durch Infektionen mit und ohne Exsikkose. Unerwünschte medikamentöse Wirkungen müssen immer in Betracht gezogen werden, da sie bei rund 30 % der Delirien beobachtet werden. Eine besondere Rolle spielen anticholinerge Arzneimittelwirkungen, zumal in der Pathogenese ein cholinerges Ungleichgewicht angenommen wird. Eine französische Studie in verschiedenen Hausarztpraxen konnte bereits bei klinisch unauffälligen älteren Patienten (65+) subklinische Störungen von Aufmerksamkeit, Mnestik und Koordination infolge anticholinerger Nebenwirkungen aufdecken [6]. Für Deutschland wurde mit der PRISCUS-Liste eine Aufstellung potenziell inadäquater Medikamente für Ältere erarbeitet, die als Richtschnur dienen kann [7].
Behandlung des Delirs
Die Behandlung des Delirs folgt vier Grundprinzipien:
- Vermeiden von Faktoren, die ein Delir auslösen oder verschlechtern können
- Identifikation und Behandlung potenzieller Ursachen
- Delir-reduzierende medizinische Versorgung
- Kontrolle gefährlicher Verhaltensstörungen
Die Ursachensuche beginnt wie üblich mit Anamnese und körperlicher Untersuchung. Zu achten ist auf vorbestehende kognitive Defizite (Fremdanamnese), Einnahme von Medikamenten, Schmerzen (non-verbale Zeichen), Harnverhalt, Exsikkose, Zyanose, Blässe, Schweißbildung, neurologische Symptome (Zungenbiss, Pupillen, Babinski-Reflexe etc.), vegetative Symptome als Hinweise für einen Entzug von Alkohol oder Medikamenten.
Wichtig für den Delirkranken ist eine sichere und reizarme Umgebung. Sensorische Defizite (Brille, Hörgerät) müssen ausgeglichen, der Wechsel von Bezugspersonen und ungewöhnliche Körperwahrnehmungen (Blasenkatheter, Fixierung) sollten vermieden werden. Günstig wirkt sich ein regelmäßiger Tagesablauf mit Aktivierung in den Tagstunden und Ruhe in den Nachtstunden aus. Im Sinne der Validation und des wertschätzenden Umgangs soll auf die Gedankenwelt der Delirkranken möglichst eingegangen werden; sinnlose Diskussionen oder gar Drohungen sind kontraproduktiv. Nicht unbedingt notwendige Medikamente sollten sicherheitshalber abgesetzt oder pausiert werden; die Vitalparameter (Puls, Blutdruck, Blutzucker) können eher im oberen Normbereich gehalten werden. Bei Agitation kann eine probatorische analgetische Therapie (z. B. Paracetamol 3 g/d) innerhalb von ein bis zwei Wochen zur signifikanten Verminderung der Unruhe führen [8].
Mit den genannten Maßnahmen lässt sich ein Teil der Delirien ausreichend kontrollieren, wobei „störendes Verhalten“ soweit möglich toleriert werden sollte. Erst wenn eine erhebliche Eigen- oder Fremdgefährdung vorliegt oder die Symptomatik für den Patienten quälend ist, kann begleitend medikamentös eingegriffen werden. Grundsätzlich gilt es, eine initial ausreichend hohe Dosis zu wählen, um die Notfallsituation rasch in den Griff zu bekommen. Anschließend wird die Dosis nach unten titriert mit dem Ziel, die eingesetzten Medikamente wieder abzusetzen oder sie in so niedriger Dosis wie gerade noch erforderlich fortzuführen. Alle beim Delir eingesetzten Medikamente, insbesondere Neuroleptika, besitzen ein nicht unerhebliches Schädigungspotenzial. So sind die Rate an Schlaganfällen und die Mortalität bei neuroleptischer Dauertherapie um den Faktor 2 bis 4 erhöht. Venös-thromboembolische Ereignisse sind besonders bei immobilen Patienten unter antipsychotischer Therapie häufiger. Diese Beobachtung gilt sowohl für „klassische“ als auch für „atypische“ Neuroleptika, wobei die Daten äußerst heterogen sind und zusätzlich im Kontext mit der (Multi-)Morbidität speziell bei älteren Patienten interpretiert werden müssen [10].
Pharmakotherapie des Delirs
Bei Agitation, Wahn und Halluzinationen werden Neuroleptika bevorzugt eingesetzt. Stehen Angst oder vegetative Symptome im Vordergrund, bieten sich vorübergehend Benzodiazepine (insbesondere Lorazepam), Antidepressiva und Clonidin an. Cholinerge Medikamente (z. B. Antidementiva mit Hemmung der zerebralen Acetylcholinesterase) haben sich entgegen der pathophysiologischen Erwartung beim Delir als nicht effektiv erwiesen [9].
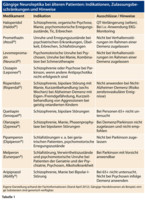
Verbreitet ist die Unterteilung in „klassische“ und „atypische“ Neuroleptika (vgl. Übersicht 2). Die Substanzklasse der Atypika wurde mit der Entwicklung von Clozapin eröffnet, da dieses Medikament quasi keine extrapyramidal motorischen Nebenwirkungen aufweist. Dies gilt aber nicht für die meisten anderen Vertreter dieser Gruppe, so dass die Sammelbezeichnung „atypisch“ eigentlich nicht gerechtfertigt ist. Besser ist es, von Neuroleptika der 1. und der 2. Generation zu sprechen. Neuroleptika der 1. Generation werden meist in hoch- und niederpotent unterschieden. Eine solche Unterteilung weist die 2. Generation (leider) nicht auf, wiewohl sie stark antipsychotische (z. B. Risperidon) und gering antipsychotische (z. B. Pipamperon) Neuroleptika umfasst. Im Allgemeinen ist es so, dass stark antipsychotische bzw. hochpotente Neuroleptika in üblichen Dosen nur gering bis gar nicht sedierend wirken, während niederpotente Neuroleptika stark sedierend und wenig antipsychotisch sind. Diese Unterschiede sind dosisabhängig und verwischen in höherem Dosisbereich. Weitere substanzspezifische (Neben-)Wirkungen sind zu beachten. Einen Überblick gibt Tabelle 1.
Aufgrund der aktuellen Datenlage scheint es so zu sein, dass „klassische“ und „atypische“ Neuroleptika eine vergleichbare Wirkung zeigen bei tendenziell geringerer Rate an motorischen Nebenwirkungen bei den „Atypika“. Haloperidol weist in niedriger Dosis (< 2 mg = 20 Tropfen) ebenfalls eine gute motorische Verträglichkeit auf. Mehrere Studien konnten aber eine Übersterblichkeit einer Therapie mit Haloperidol belegen [11], so dass es sich für die Langzeitanwendung bei Älteren nicht zu eignen scheint. In der Initialphase ist es jedoch ein rasch wirkendes und durch die Tropfenform gut titrierbares Medikament. Zudem gibt es für Notfälle eine parenterale Applikation (Cave: kardiales Monitoring wegen Gefahr der QT-Verlängerung).
Neben der wissenschaftlichen Datenlage sind Indikationen und Kontraindikationen zu beachten. Leider ist es so, dass die allermeisten Neuroleptika explizit nicht für die Anwendung bei Patienten mit Demenz zugelassen sind (Übersicht in Tabelle 1). Die Anwendung anderer Neuroleptika außerhalb ihrer zugelassenen Indikation stellt einen individuellen Heilversuch dar, an den hohe juristische Ansprüche gestellt werden (schwerwiegende Erkrankung, keine Alternativtherapie verfügbar, positive Studienlage, Einverständnis des Patienten etc.). Explizit nicht zugelassen bei Demenzpatienten ist beispielsweise das sehr häufig eingesetzte Promethazin (Atosil®), das darüber hinaus starke anticholinerge Wirkungen aufweist (Gefahr paradoxer Wirkung, kardiale Beeinträchtigungen). Generell sollen Medikamente mit ausgeprägten anticholinergen (Neben-)Wirkungen alten Menschen nicht oder nur nach sorgfältiger Abwägung verordnet werden.
Folgende praktische Empfehlung kann aktuell gegeben werden:
- Bei Vorherrschen von Halluzinationen, Wahn und Denkstörungen
Kurzfristiger Einsatz von Haloperidol oder von Risperidon.
- Bei Vorherrschen von psychomotorischer Unruhe oder Schlafstörung
Pipamperon oder Melperon, wobei der Melperon-Metabolismus über CYP2D6 Interaktionen mit verschiedenen Betablockern und Psychopharmaka aufweist. Der Abbau kann nicht-linear gehemmt werden [13]. Pipamperon weist keine klinisch relevanten Interaktionen auf.
- Bei Parkinson-Symptomatik oder Lewy-Body-Demenz
Clozapin ist möglich, es müssen jedoch sehr engmaschige Kontrollen von Blutbild (Agranulozytose) und EKG (Myokarditis, Kardiomyopathie) durchgeführt werden, die vom verordnenden Arzt sicherzustellen sind. Die Substanz verfügt über ausgeprägte anticholinerge Nebenwirkungen und ist daher per se bei Älteren eher ungünstig. Clozapin sollte nur von mit der Substanz vertrauten Ärzten angewandt werden. Alternativ kann Quetiapin versucht werden, das nur geringe extrapyramidalmotorische Nebenwirkungen hat.
- Bei bekannter Epilepsie bzw. zerebraler Krampfneigung
Melperon erniedrigt die Krampfschwelle im Gegensatz zu den meisten Antipsychotika nicht und verstärkt die Wirkung von Antiepileptika.
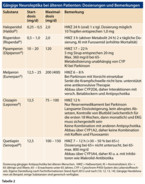
Kombinationstherapien von hoch- und niederpotenten Neuroleptika unter der Vorstellung des Kupierens psychotischer Symptome tagsüber ohne Sedation und Schlafinduktion abends werden in der Praxis nicht selten angewandt. Studiendaten zu diesem Vorgehen fehlen jedoch weitgehend. Gängige Dosierungen und Hinweise für relevante Interaktionen oder Kontrollen finden sich in Tabelle 2.
Folgende Regeln sollten bei der Anwendung von Antipsychotika bei Älteren beachtet werden:
- Behandlung potenzieller Ursachen
- Abstellen aller delirfördernden Bedingungen
- Ausschöpfen nicht medikamentöser Maßnahmen inkl. Toleranz gegen nicht gefährliche Verhaltensstörungen
- Medikamentöse Therapie unter Abwägung der erhöhten Morbidität und Mortalität aller verfügbaren Antipsychotika
- Medikamentöse Therapie nur bei erheblicher Eigen- oder Fremdgefährdung oder bei quälender Symptomatik
- Niedrigst mögliche Dosis anstreben: Dosistitration bzw. Absetzversuche bei jeder Visite

Erschienen in: Der Allgemeinarzt, 2012; 34 (11) Seite 36-40