Die Ursachen chronischer Bauchbeschwerden wie Leibschmerzen und Diarrhö sind vielfältig. Eine gute systematische Anamneseerhebung und Stufenstrategie bei der diagnostischen Abklärung dieser häufigen Symptome ist wichtig, um nicht vorschnell die „Reizdarm-Schublade“ zu bemühen. Diese vermutlich zu häufig gewählte Einordnung stellt bekanntlich eine Ausschlussdiagnose dar. Im Folgenden sollen anhand von Fallbeispielen diagnostische Hilfen dargestellt werden, die die tägliche Praxis erleichtern können.
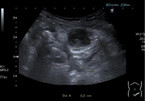
Eine 72-jährige Patientin klagt über zunehmende Unterbauchschmerzen sowie einen Wechsel von Diarrhö und Verstopfung. Sie sei bisher gesund gewesen. Zudem beklagt die Patientin eine starke Abgeschlagenheit sowie Rückenschmerzen. Bei den Laborwerten fällt ein deutlich erhöhtes CRP von 55 mg/l auf, im Blutbild eine Eisenmangelanämie (Hb: 88 g/l, Hkt: 0,288) bei mikrozytärem und hypochromem Blutbild. Die Thrombozyten sind mit 894 000/µl deutlich erhöht, ebenso die Leukozyten mit 18 540/µl. Eine Calprotectin-Bestimmung zeigt einen deutlich erhöhten Wert von 732 µg/g Faeces. Im Ultraschall ist eine Sigmadivertikulose zu sehen mit einem eindeutig entzündeten Darmabschnitt, also eine Divertikulitis (vgl. Abbildung 1).
Die Ursachen chronischer Darmbeschwerden können vielfältig sein. In diesem Fall bestand eine „rezidivierende“ Divertikulitis, die chronisch vor sich hin schwelte, ohne wirklich jemals akute Beschwerden wie im Lehrbuch zu machen. Die Anamnese war unspezifisch und hätte durchaus auf ein Reizdarmsyndrom hindeuten können.
Ernährungsgewohnheiten
Zu den häufigsten Ursachen chronischer Darmbeschwerden gehört sicherlich die Ernährung. Alkohol- sowie Koffeingenuss kann mengenabhängig zu Durchfällen und Darmkrämpfen führen. Zunehmend akzeptiert wird auch, dass eine ballaststoffreiche Ernährung in einem kleineren Anteil der Bevölkerung zu vermehrten Blähungen und Darmbeschwerden führt [1, 2]. Die individuell unterschiedliche Darmflora ist dabei in den letzten Jahren in den Fokus des Interesses gerückt. Offensichtlich gibt es Bakterien, die zur Bildung von Fäulnisgasen führen und die bei Patienten mit starker Darmgasbildung anzutreffen sind. Diese Patienten vertragen eine ballaststoffreiche Ernährung eher schlechter. Allerdings ist es schwer zu vermitteln, dass eine bislang als überaus gesund erachtete Ernährung Beschwerden machen könnte [3]. In jedem Fall lohnt es sich, einen Test mit einer ballaststoffarmen Ernährung durchzuführen. Eine gute Anleitungen für eine ballaststoffarme Ernährung findet man z. B. u ter der Adresse http://www.croehnchen-klub.de/crohn-forum/index.php?page=Thread&threadID=68315 .
Endokrine Störungen
Weiterhin gibt es endokrine Erkrankungen, die Ursachen chronischer Darmbeschwerden sein können. Hierzu zählt der Diabetes mellitus, der im Rahmen der Neuropathie eine Veränderung der Darmmotilität zur Folge haben kann. Auch die Nebenniereninsuffizienz zählt dazu.
Operationsfolgen
Folgen einer Darmresektion sind zum einen der Verlust einer bestimmten Resorptionsoberfläche, darüber hinaus können aber auch Adhäsionen entstehen, die Probleme bereiten. Auch nach einer Cholezystektomie kann es zu Beschwerden kommen. Dies wird pathophysiologisch so erklärt, dass die Gallenblase als Reservoir für die Galle nicht mehr vorhanden ist. So können dann während der Mahlzeiten, insbesondere wenn fettreiche Mahlzeiten konsumiert werden, unter Umständen zu wenig Gallensäuren für die Emulgierung des Fettes zur Verfügung stehen. Dies kann zu fettigen Durchfällen und zu Blähungen führen, wenn die Fettsäuren von den Dickdarmbakterien verstoffwechselt werden. Zwischen den Mahlzeiten können jedoch die Gallensäuren, da sie nicht mehr in der Gallenblase aufgefangen werden, auch in den Dickdarm übertreten und dort Durchfälle verursachen. Einige Kollegen empfehlen, mit einem Gallensäurebinder wie zum Beispiel Colestyramin (Quantalan®) einen Therapieversuch zu unternehmen. Wichtig ist es jedoch, diesen Gallensäurebinder dann nicht zu den Mahlzeiten zu empfehlen (wie es im Beipackzettel steht und wie es von den meisten Patienten gemacht wird), sondern in zweistündigem Abstand zu den Mahlzeiten.
Zöliakie
Eine weitere wichtige Ursache für unspezifische Darmbeschwerden sind Kohlenhydratmalabsorptionssymptome wie der Laktasemangel (Laktoseintoleranz), die Zöliakie oder die Malabsorption schlecht absorbierbarer Kohlenhydrate wie zum Beispiel Ballaststoffe.
Die Zöliakie ist mit 1 % Prävalenz eine häufige Erkrankung (vgl. Fall 2). Die Mehrzahl der Zöliakiepatienten ist noch nicht diagnostiziert [14 - 16]. Es muss davon ausgegangen werden, dass die individuelle Verträglichkeit von Gluten sehr unterschiedlich ist [17]. Während einige Patienten bereits auf Glutenkontamination der Nahrungsmittel im Bereich von ppm reagieren, können andere Patienten durchaus täglich eine Scheibe Brot essen, ohne Symptome zu haben oder eine weitgehende „Glutentoleranz“ auch wieder entwickeln [18]. Die Symptome der Zöliakie sind typischerweise Diarrhö, Blähungen und auch eine Anämie.
Ein Verdacht auf Zöliakie ergibt sich im Allgemeinen aufgrund der Serologie. Die Diagnose wird dann endoskopisch durch eine Zottenatrophie des Dünndarms bestätigt. Die Ursache liegt in einer Allergie gegen Gluten, das in vielen Getreidesorten wie Weizen, Roggen, Hafer, Gerste und anderen enthalten ist, sowie in einer genetischen Disposition. Die Behandlung erfolgt durch glutenfreie Ernährung.
Eine 26-jährige Studentin hat seit zwei Jahren immer wieder Episoden von leichten Durchfällen mit bis zu vier Stühlen am Tag mit etwas Grummeln im Bauch mehrmals die Woche. Sie verträgt subjektiv alle Nahrungsmittel außer größeren Mengen an Bier. Die Patientin ist schlank, aber nicht untergewichtig, die klinische Untersuchung ist unauffällig. Das Labor ist ebenfalls unauffällig. Das Blutbild zeigt keine Auffälligkeiten, keine Anämie, keinen Eisenmangel. In der Serumchemie findet sich ein normales CRP, normale Elektrolyte, normale Nierenwerte. Lediglich eine leicht erhöhte ASAT (35 IU/l, Normbereich < 32) und ALAT (51 IU/L, Normbereich < 33) fallen auf. In der Ultraschalluntersuchung zeigen sich dilatierte Dünndarmschlingen mit irregulären Kerckringschen Falten. Darüber wird eine mesenteriale Lymphadenopathie sichtbar. Die durchgeführten serologischen Untersuchungen zeigen, dass die Gliadin-IgA-Antikörper einen Titer von 101 IU/ml aufweisen (Normbereich < 7,0), die Gliadin-IgG-Antikörper liegen bei > 35 IU/ml (Normbereich < 7,0). Aufgrund dieser Befunde wird unter dem Verdacht einer Zöliakie eine Gastroskopie durchgeführt. Es zeigen sich Duodenalschleimhaut-Biopsate mit verplumpten Zotten, vermehrtem intraepithelialem lymphoplasmatischem Stromainfiltrat sowie deutlich vermehrte intraepitheliale Lymphozyten entsprechend einer Sprue Marsh Typ 3A. Bei dieser Patientin lag also trotz des klinisch relativ unauffälligen Verlaufs und der subjektiv vorhandenen Getreide-Eiweißverträglichkeit eine Zöliakie vor.
Laktoseintoleranz
Vermutlich ebenso häufig wie eine Zöliakie ist eine Laktoseintoleranz. Die Symptome sind ebenfalls unspezifisch. Sie manifestiert sich mit Durchfall, Blähungen, Bauchschmerzen und Flatulenz nach Genuss von Milchprodukten oder laktosehaltigen Nahrungsmitteln [10, 19].
Sie kann mittels H2-Atemtest diagnostiziert werden. Hierbei wird nach der Einnahme von Laktose die Wasserstoffkonzentration in der Ausatemluft gemessen. Wenn die Laktose nicht komplett im Dünndarm von der Laktase gespalten wird, kann sie in den Dickdarm gelangen, wo sie nicht wie normalerweise im Körper in Wasser und Kohlendioxid umgewandelt, sondern auch in Wasserstoff abgeatmet wird. Die Ursachen der Laktoseintoleranz liegen in einem Fehlen oder einer eingeschränkten Aktivität der Laktase. Die Behandlung besteht im Meiden von Milchprodukten. Seit neuestem gibt es aber auch die Möglichkeit, Laktase in Form von Tabletten zu substituieren.
Wichtig ist hier festzuhalten, dass eine Laktoseintoleranz häufig sekundärer Natur ist und die Diagnose einer Laktoseintoleranz nicht immer als alleinige Ursache der chronischen Darmbeschwerden akzeptiert werden sollte [10 - 12]. Auch nach einer Darmresektion sowie bei einer Zöliakie oder einer chronisch-entzündlichen Darmerkrankung kann eine sekundäre Laktoseintoleranz auftreten [13].
Die Laktoseintoleranz ist leicht behandelbar, sollte jedoch nicht dazu führen, keine weitere Ursachensuche zu betreiben. Richtungsweisend ist hier die Frage nach dem Genuss von Joghurt. Wird auch Joghurt schlecht vertragen, ist die Laktoseintoleranz nicht die alleinige Ursache der Beschwerden. Im Joghurt wurde durch Laktobazillen die Laktose bereits vollkommen umgesetzt, es ist keine Laktose mehr vorhanden. Daher sollte Joghurt auch von Patienten mit Laktoseintoleranz vertragen werden. Ist dies nicht der Fall, muss weiter nach Ursachen der Beschwerden geforscht werden.
Fruktose-Unverträglichkeit
Eine weitere häufige Ursache für Darmbeschwerden ist die intestinale Fruktoseintoleranz [20]. Auch sie manifestiert sich mit Blähungen, Durchfall und Unwohlsein. Sie wird ebenfalls mit einem H2-Atemtest nach dem oben genannten Prinzip diagnostiziert. Ihre Ursache liegt in der Malabsorption von Fruchtzucker und Saccharose im Dünndarm. Dies führt zum bakteriellen Abbau der in den Dickdarm übergetretenen Fruchtzucker und zu vermehrter Gasproduktion und Durchfall. Die Behandlung besteht in einer Ernährungsberatung, der Reduktion und dem Meiden von Fruktose, wobei die Verträglichkeitsgrenzen unterschiedlich sind.
Morbus Crohn, Colitis ulcerosa, lymphozytäre Kolitis
Sicherlich stellen auch chronisch entzündliche Darmerkrankungen wie Colitis ulcerosa und Morbus Crohn oder die lymphozytäre Kolitis Ursachen für unspezifische Darmbeschwerden dar (vgl. Fall 3 und 4). Die lymphozytäre Kolitis zeigt eine zunehmende Inzidenz in den letzten Jahren [4 - 8]. Insbesondere in Skandinavien, jedoch auch in Mitteleuropa werden nun erhöhte Raten neuer Fälle von lymphozytärer Kolitis beobachtet. Ihre Entstehung wird teilweise mit der Einnahme von Antidepressiva vom Typ der Serotonin-Reuptake-Inhibitoren und anderen Medikamenten assoziiert [4, 9].
Das Calprotectin muss nicht erhöht sein, wenn nur eine leichte lymphozytäre Kolitis vorliegt. Häufig finden sich aber erhöhte Werte, die sich im Lauf der Therapie normalisieren. In jedem Fall muss bei einer Koloskopie eine Biopsieentnahme erfolgen, auch wenn der Darm makroskopisch normal aussieht.
Eine Koloskopie wegen unspezifischer Darmbeschwerden, bei der keine Biopsie entnommen wurde, stellt nach dem heutigen Stand der Kenntnis einen Fehler dar.
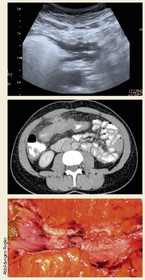
Eine 17-jährige Schülerin berichtet über seit drei Jahren immer wieder auftretende Episoden von leichten Durchfällen mit bis zu drei Stühlen am Tag und Bauchkrämpfen mehrmals die Woche über zwei bis drei Wochen. Dazwischen habe sie immer wieder lange Episoden von Wohlbefinden in den letzten Jahren gehabt. Seit sechs Monaten nehmen die Unterbauchschmerzen aber etwas zu, sie hat Krämpfe vor dem Stuhlgang, öfters Übelkeit nach dem Essen, besonders stark während der Menstruation. Der gynäkologische Kollege hat eine „Hypermenorrhö“ diagnostiziert. Die Patientin ist schlank und will Model werden. Die Eltern vermuten eine beginnende Anorexie, da sie häufig über Übelkeit klagt und weniger isst. Die klinische Untersuchung ist unauffällig bis auf einen leichten Druckschmerz im Unterbauch. In der Laboruntersuchung zeigen sich Normwerte für Elektrolyte, Nieren, Leber und CRP. Es zeigt sich ein normaler Eisenstatus. Das Vitamin B12 ist mit 121 ng/l diskret erniedrigt (Normbereich 180 - 900 ng/l). Das Gesamtprotein ist mit 65 g/l am unteren Grenzwert (Normbereich 66 - 87 g/l). Das Blutbild ist vollkommen unauffällig. Es wird eine Calprotectin-Bestimmung in den Faeces durchgeführt. Dabei zeigt sich ein Calprotectinwert von 440 µg/g Faeces (Normbereich < 50 µg/g Faeces). Daraufhin wird eine Ultraschalluntersuchung veranlasst, in der sich eine deutlich verdickte Darmwand im Bereich des Ileums zeigt (vgl. Abbildung 2). Es liegt also eine Ileitis terminalis vor, die in einer Koloskopie bestätigt wird. Damit kann bei der jungen Patientin die Diagnose eines Morbus Crohn gestellt werden.
Clostridien-Kolitis
Ein zunehmendes Problem stellt auch die antibiotikaassoziierte Diarrhö oder Clostridien-Kolitis dar [21, 22]. Es ist aber festzuhalten, dass Clostridium difficile nur eine Ursache unter verschiedenen anderen der antibiotikaassoziierten Diarrhö darstellt. Bei der Clostridium-difficile-assoziierten Diarrhö wird vorausgesetzt, dass eine Diarrhö und ein entsprechender positiver Stuhltest vorhanden sind. Eine Kolitis manifestiert sich mit klinischen Zeichen, die bis zur pseudomembranösen Kolitis gehen können. Ein toxisches Megakolon im Rahmen einer Clostridien-Kolitis wird inzwischen nur noch selten beobachtet.
Die Clostridien-Kolitis ist jedoch auf dem Vormarsch. Zu berücksichtigen ist, dass Clostridium difficile bei 20 bis 30 % der antibiotikaassoziierten Diarrhöen im Stuhl gefunden werden kann. Darüber hinaus findet sichClostridium difficile bei 50 bis 70 % der antibiotikaassoziierten schweren Diarrhöen und bei über 90 % der Fälle von pseudomembranöser Kolitis. Mindestens 5 % der Bevölkerung sind Träger von Clostridium difficile, vermutlich aber auch mehr. Während einer antibiotischen Therapie werden interessanterweise 16 bis 35 % der Patienten, die behandelt werden, positiv für Clostridium-difficile-Toxin. Falls sie keine Symptome einer Diarrhö zeigen, besteht jedoch kein Behandlungsbedarf. Nur etwa 15 bis 30 % der Patienten, die Clostridium difficile in einem Krankenhaus akquirieren, entwickeln eine symptomatische assoziierte Erkrankung.
Medikamente als Auslöser
Nahezu sämtliche Medikamente können Darmbeschwerden verursachen. Hier ist in der Anamnese natürlich darauf einzugehen, ob bestimmte Medikamente in der letzten Zeit neu eingenommen wurden. Darüber hinaus kann auch eine neue Kombination von bisher vertragenen Medikamenten eine Diarrhö auslösen. Eine Antibiotikatherapie kann zu einer antibiotikaassoziierten Kolitis führen. Typischerweise treten nach Behandlung mit Breitbandpenicillin bei etwa 20 bis 25 % der Behandelten Durchfälle auf, die bis zu drei Monate oder noch länger anhalten können. Prophylaktisch sind hier Probiotika wirksam. Deren Wirksamkeit bei der Therapie dieser Beschwerden ist jedoch umstritten.
Weitere Ursachen
Weitere Ursachen chronischer Darmbeschwerden können ischämische Darmerkrankungen, eine Strahlenenteritis oder eine paradoxe Diarrhö bei Kolonkarzinom sein. Insbesondere bei Kindern finden sich manchmal Unverträglichkeiten von Zuckeraustauschstoffen, die den Nahrungsmitteln heute vermehrt zugesetzt werden.
Wie kommen wir weiter? - Hinweise aus der Anamnese
Wie kommt man nun bei dieser Fülle möglicher Ursachen von Darmbeschwerden zu einer Diagnose? Hier können die Anamnese oder einfachste klinische Untersuchungen bereits weiterhelfen. Infektionen wie mit Viren (z. B. Noro-Viren, Rota-Viren) oder Bakterien (EHEC) führen fast immer zu einer sekretorischen Diarrhö, die aber nach kurzer Zeit wieder sistiert. Auch die Diarrhö nach Cholezystektomie bedingt durch die Gallensäuren ist eine sekretorische Diarrhö. Zudem können die meisten Medikamentennebenwirkungen zu einer sekretorischen Diarrhö führen. Eine osmotische Diarrhö wird durch nicht absorbierbare Ingesta verursacht. Hierzu zählen Abführmittel, Laktulose, ein Disaccharidasemangel wie bei Laktoseintoleranz, aber auch Zöliakie und Darmresektionen.
Wie lässt sich nun einfach zwischen einer osmotischen Diarrhö und einer sekretorischen Diarrhö unterscheiden? Die einfachste klinische Unterscheidung ist möglich durch den 24-Stunden-Hungerversuch (keine Nahrungsaufnahme über 24 h, Trinken ist natürlich weiterhin möglich). Kommt es dadurch zu einem Sistieren der Beschwerden, liegt eine osmotische Diarrhö vor. Eine sekretorische Diarrhö wird hingegen weiterbestehen.
Darüber hinaus können weitere Angaben aus der Anamnese hilfreich sein (vgl. Tabelle 1). Fettstühle oder eine Steatorrhö deuten auf eine Maldigestion oder eine Malabsorption hin. Meteorismus und Flatulenz sind sehr häufig auf den vermehrten Abbau von Kalorienträgern durch die Dickdarmflora zurückzuführen. Tabelle 2 zeigt einen Fragenkatalog zur Verdachtsabklärung von organischen Darmerkrankungen. Diese Fragen können hilfreich sein, organische Darmerkrankungen von funktionellen Darmerkrankungen zu unterscheiden.
Ganz allgemein werden sogenannte Alarmsymptome, die weitere Untersuchungen erfordern, definiert. Zu diesen Alarmsymptomen gehören Blut im Stuhl (sichtbar als frisches Blut oder durch Schwarzfärbung des Stuhles), Gewichtsverlust, Anämie, Fieber, Störung der Nachtruhe wegen Durchfall oder Bauchschmerzen und relativ kürzlich aufgetretene Symptome oder Änderung der Symptome.
Häufiges ist häufig, Seltenes ist selten
So banal dieses Statement klingen mag, es kann jedoch in der Differenzierung der chronischen Bauchbeschwerden richtungsweisend sein. Seltene Tumoren der endokrinen Zellen der Bauchwand können sicherlich ebenfalls zu chronischen Bauchbeschwerden führen. Hierzu zählen Vipome, Gastrinome oder Tumoren des pankreatischen Polypeptids. Diese sind jedoch absolute Raritäten. Ebenso ist der Morbus Whipple eine Rarität. Im Allgemeinen ist es nicht notwendig, diese Überlegungen in die Differenzialdiagnose einzubeziehen.
Diagnostische Maßnahmen
Zunächst sollte bei Patienten mit chronischen Darmbeschwerden (Diarrhö, Obstipation) eine Stuhluntersuchung stattfinden. Hier sollte nach pathogenen Bakterien wie Salmonellen, Shigellen, Campylobacter und Yersinien gesucht werden. Darüber hinaus sollte nach dem Clostridium-difficile-Bakterium auch in Form eines Toxintests gefahndet werden. Nachweis von Clostridien-Toxin im Stuhl macht bei entsprechender Symptomatik eine Clostridien-Kolitis wahrscheinlich. Einige Labors berichten über einen „bakteriologischen Normalbefund“. Ein solcher existiert jedoch nicht. Es kann lediglich nachgewiesen werden, dass pathogene Keime nicht im Stuhl in signifikanter Menge vorhanden sind.
Als Untersuchung bei Patienten mit chronischen Bauchschmerzen empfehlen sich als erste Stufe Blutuntersuchungen: BSG/CRP, Blutbild, Elektrolyte, Harnstoff, Kreatinin und TSH.
In einer zweiten Stufe sollten Vitamin B12, Transferrinsättigung, Anti-tTG-Antikörper, IgA, Antikörper gegen deamidiertes Gliadinpeptid und Calprotectin bestimmt werden.
Falls Auffälligkeiten und weiterhin Zweifel bestehen, sollten in einer dritten Stufe eine endoskopische Untersuchung (Koloskopie) und Gastroduodenoskopie mit Biopsie erfolgen. Gegebenenfalls können auch eine Röntgendiagnostik wie Abdomenübersicht und ein MRT des Darmes durchgeführt werden. Eine CT-Diagnostik sollte vermieden werden.
Erst in einer vierten Stufe müssen andere Erkrankungen bedacht werden.
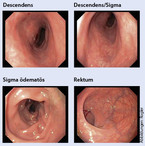
Eine selbstständige 68-jährige Patientin berichtet, vor fünf bis sechs Jahren schon einmal Bauchschmerzen und Durchfälle gehabt zu haben. Damals hätte sich eine spontane Besserung nach drei bis vier Monaten ergeben. Jetzt seien diese Beschwerden jedoch wieder aufgetreten, sie hätte ihnen zunächst wenig Beachtung geschenkt. Seit einem Jahr sei ihre Lebensqualität jedoch massiv eingeschränkt mit immer wieder auftretenden starken Bauchkrämpfen und wässrigen Durchfällen, jedoch nur zwei- bis dreimal am Tag. Vor allen Dingen morgens besteht ein imperativer Stuhldrang. Die Patientin hat ihre Ernährung auf Schonkost umgestellt, ein leichter Gewichtsverlust ist aufgetreten. Im Labor findet sich bei normalen Elektrolyten und Nierenwerten sowie normalem CRP und einem normalen Eisenstoffwechsel eine leicht erhöhte Gamma-GT von 40 U/l (Normbereich 5 - 36 U/l). Das Albumin ist mit 39 g/l am unteren Normwert (Normbereich > 40 g/l). Das Blutbild ist komplett unauffällig. Es wird eine Calprotectin-Bestimmung durchgeführt. Der Calprotectinwert liegt bei 304 µg/g Faeces. Auswärtig wird eine Koloskopie durchgeführt, der Befund ist unauffällig und die Patientin wird nicht weiterverfolgt. Bei nochmaliger Durchführung einer Sigmoidoskopie bei wiederum unauffälligen makroskopischen Befunden zeigt sich in den Biopsien eine Kolonschleimhaut mit intraepithelialer Lymphozytose, oberflächlicher Deckzelldegeneration und diffusen gemischtzelligen Entzündungsinfiltraten. Der Befund ist vereinbar mit einer lymphozytären Kolitis (vgl. Abbildung 3). Die Patientin wird mit Budesonid dreimal täglich 3 mg behandelt. Im Lauf von drei Monaten sinken die Calprotectinwerte auf unter 50 und die Beschwerden der Patientin verschwinden.
Calprotectin-Bestimmung als wichtiges Werkzeug
Calprotectin im Stuhl ist ein hervorragender Parameter zur Unterscheidung von organischen und funktionellen Darmerkrankungen [23]. Beim Calprotectin handelt es sich um ein kalziumbindendes Protein, das vor allen Dingen in Neutrophilen gefunden wird. Es kann nicht durch intestinale Bakterien abgebaut werden, daher ist es bei Raumtemperatur im Stuhl bis zu einer Woche stabil, was es zu einem idealen Parameter macht. Wenn neutrophile Granulozyten bei Entzündungen in die Darmwand einwandern, zerfallen sie und das Calprotectin wird in die Faeces freigesetzt. Der Calprotectinwert stellt also einen Summenwert über die letzten Tage dar.
Einschränkend muss gesagt werden, dass der Calprotectinwert nicht spezifisch ist. Er wird bei einer Vielzahl von organischen Darmerkrankungen erhöht gefunden. Darüber hinaus finden sich erhöhte Werte in höherem Alter, nach der Einnahme von nicht-steroidalen Antiphlogistika (die bekanntermaßen die Darmschleimhaut schädigen), bei der Einnahme von Protonenpumpeninhibitoren, bei Leberzirrhose, auch bei bakteriellen Lungenentzündungen und gastrointestinalen Infektionen.
Ein Grenzwert von 50 µg/g Faeces kann sehr gut zwischen funktionellen und organischen Darmerkrankungen unterscheiden. Daher hilft Calprotectin sehr gut bei der Differenzialdiagnose organischer und funktioneller Magen-Darmerkrankungen [24]. Es ist genauer als CRP und korreliert darüber hinaus mit der Schwere der Darmentzündung [25]. Es kann bei einer Verlaufsdiagnostik eine Endoskopie zur Therapiekontrolle ersetzen.
Darüber hinaus hat es aber natürlich Limitationen. Immer dann, wenn Blut im Stuhl ist, wird auch das Calprotectin erhöht sein. Also wird auch ein Kolonkarzinom einen erhöhten Calprotectinwert machen, ebenso wie Nasenbluten.
Erschienen in: Der Allgemeinarzt, 2013; 35 (7) Seite 16-21