Die Prinzipien der Wundversorgung sind beim Kind und Erwachsenen identisch. Jedoch sind beim Kind die Umstände, seine Ängste und die Ängste der Eltern einzuschätzen und in den Behandlungsplan mit einzubeziehen. Nicht selten hängt eine suffiziente Wundversorgung vor allem von der richtigen Einschätzung des kleinen Patienten ab.
Primäres Ziel der Wundversorgung ist die Wiederherstellung der normalen Funktion, die Schmerzbehandlung, die Reduktion des Infektionsrisikos und ein gutes kosmetisches Ergebnis. Sekundäres Ziel der Wundversorgung ist es, dem Kind, und gelegentlich auch den Eltern, die Angst vor der Behandlung zu nehmen. Dadurch fördert man die Kooperation des Kindes und damit die Möglichkeit der optimalen Wundexploration. Um dieses Ziel zu verwirklichen, ist eine ausreichende Analgesie bereits bei der Erstbeurteilung der Wunde notwendig. Auch an das Entdecken und Behandeln zusätzlicher Verletzungen sollte man denken.
Wundtypen
Es gibt viele verschiedene Wundtypen, wie Prellung, Quetschung, Schürfwunden, Quetschwunden, Risswunden, Ablederungsverletzungen, Verbrühungen und Verbrennungen, Stich-, Schnitt- und Schusswunden sowie Pfählungsverletzungen und Bisswunden. Die meisten Wunden, vor allem bei kleinen Kindern, entstehen infolge Einwirkung stumpfer Gewalt am Kopf [2]. Ein erhöhtes Infektionsrisiko besteht bei einer Verletzung über die Epidermis hinaus, bei Begleiterkrankungen wie Diabetes mellitus und Immunsuppression, wenn die Wunde älter als 19 bis 24 Stunden ist, bei einer ausgedehnten Wunde mit verminderter Durchblutung (Ablederung, Riss- oder Quetschwunde), bei starker Verschmutzung, bei Verletzung von tiefer liegenden Strukturen (Gefäße, Nerven, Sehnen, Fraktur), bei Bisswunden sowie bei Fremdkörpern in der Wunde [3].
Erstbeurteilung
Bei polytraumatisierten Patienten gilt es zunächst, den Patienten zu stabilisieren und allfällige starke Blutungen zu stoppen. Daher werden die meisten Wunden erst in einem zweiten Schritt evaluiert. Wunden mit einer Wundfläche von mehr als 10 % der Körperoberfläche sind mit einem hohen Verlust an Extrazellularflüssigkeit verbunden und können lebensbedrohlich werden [4].
Der genaue Unfallmechanismus liefert zusätzliche Informationen über die Schwere der Quetschung, die Möglichkeit der Verletzung tiefer liegender Strukturen (Gefäße, Nerven, Sehnen, Fraktur), den Grad der Verschmutzung und die Möglichkeit eines Fremdkörpers in der Wunde. Je öfter an der Wunde manipuliert wird, umso höher steigt das Infektionsrisiko und umso mehr verliert man das Vertrauen der kleinen Patienten und ihrer Eltern. Bereits jetzt ist eine ausreichende Analgesie sinnvoll.
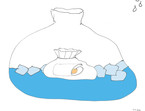
Werden Amputate mitgebracht, ist auf ihre regelrechte Versorgung zu achten (eingewickelt in eine feuchte Kompresse, kein direkter Kontakt mit Eis, vgl. Abb. 1). Ebenfalls wichtig ist das Erheben des Tetanusschutzes und das Erfassen von Allergien oder relevanten Erkrankungen, die die Wundheilung oder die Wundversorgung beeinflussen können (Diabetes mellitus, Immundefekte).
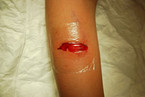
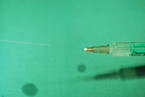
Zunächst kann die Wunde mit einer feuchten Kompresse oder bereits mit einem Lokalanästhetikum (Abb. 2) abgedeckt und bei Blutung ein Druckverband angelegt werden. Vor Applikation eines Lokalanästhetikums ist eine allfällige Nervenläsion zu erfassen. Besteht der Verdacht auf einen röntgendichten Fremdkörper oder eine Fraktur, kann nun die radiologische Untersuchung (bzw. der Transport ins Krankenhaus) erfolgen. Gegebenenfalls kann auch ein Ultraschall hinzugezogen werden, dies ist von der Kooperation des Patienten abhängig.
Primäre Wundversorgung
Die primäre Wundversorgung kann innerhalb der ersten 19 Stunden nach dem Unfallereignis erfolgen, im Gesicht sogar noch nach 24 Stunden [5].
Schürfwunden sind zu reinigen, zu desinfizieren und gegebenenfalls mit einem nicht adhäsiven Verband (z. B. Mepilex® Lite) zu versorgen. Bei großer Fläche und starker Verschmutzung braucht es zur Wundreinigung (s. u.) meist eine gute Analgosedation (s. u.).
Verletzungen am Übergang Lippenrot/Haut sind so zu adaptieren, dass es keine Stufe an der Grenze zur normalen Gesichtshaut gibt. Bei Verletzungen am Ohr ist die Knorpelbeteiligung auszuschließen. Ein Ohrhämatom kann zu Knorpelschäden führen und sollte entlastet werden. Zungenverletzungen und intraorale Verletzungen heilen großzügig von selbst und das Nahtmaterial löst sich schnell auf. Bei Spaltbildungen der Zunge ist eine Adaptation der Wundränder zu empfehlen.
Bissverletzungen haben ein erhöhtes Risiko der Infektion, weil es sich um eine kontaminierte Wunde handelt, die meist einen Kanal in die Tiefe hat. Die Wunden sollten ausgiebig gespült und exploriert werden. Vor allem bei tiefen Bisswunden und Bisswunden im Gesicht und an den Händen ist die prophylaktische Antibiotikagabe zu erwägen [1]. Im Allgemeinen sollten Bisswunden offen behandelt werden. Eine Ausnahme stellen Bisswunden im Gesicht dar, die zur Verbesserung der Kosmetik primär adaptiert werden. Bei Verbrühungen und Verbrennungen gilt es, initial die Blasen abzutragen und im Verlauf zur Beurteilung der Wunde die Beläge zu débridieren.
Oberflächen-, Infiltrations- und Leitungsanästhesie
Je nach Applikationsart und Größe des zu anästhesierenden Körperareals unterscheidet man zwischen Oberflächen- und Infiltrationsanästhesie, Leitungsanästhesie, intravenöser Regionalanästhesie und zentraler Leitungsanästhesie. In der Wundversorgung im Kindesalter spielen vor allem die Oberflächen- und Infiltrationsanästhesie sowie die Leitungsanästhesie eine Rolle, die im Folgenden genauer erläutert werden.
Diverse Studien haben gezeigt, dass die topische Applikation eines lokalanästhesierenden Gels auf die Wunde eine bessere Anästhesie erreicht als die Injektion [6]. Die US-amerikanische Academy of Pediatrics empfiehlt die Verwendung von topischen Lokalanästhetika für einfache Wunden an Kopf, Hals, Stamm und Extremitäten, die kürzer als 5 cm sind und nicht über das Subkutangewebe hinausreichen [7]. Durch ausgedehnte Resorption topischer Anästhetika können systemische Nebenwirkungen auftreten. Dies wird durch die Auswahl der Wunden (keine Schleimhäute, Wunde kleiner als 5 cm) vermieden [8]. Das Lokalanästhetikum wird in die Wunde appliziert und mit einer Folie zur besseren Resorption okklusiv abgedeckt (Abb. 2).
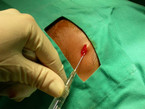
Bei der Infiltrationsanästhesie werden die Wundränder mit einem Lokalanästhetikum (Lidocain, Bupivacain) infiltriert. Dabei empfiehlt es sich, zur Schmerzreduktion dünne Nadeln zu verwenden (27 – 30 G) und bei nicht verschmutzten Wunden vom Wundrand her zu infiltrieren, um ein nochmaliges Durchstechen der Haut zu vermeiden (Abb. 3). Studien haben gezeigt, dass die langsame Injektion angewärmter Flüssigkeit, die mit Natriumbicarbonat gepuffert wurde, den Schmerz der Injektion reduziert (9 – 11). Natriumbicarbonat erhöht die Ausdehnung des Lokalanästhetikums und beschleunigt den Wirkungseintritt. Die Injektion erfolgt am besten in die Subkutis, um das Spannungsgefühl der Epidermis zu vermeiden. Die Wirkdauer beträgt bei Lidocain 1 bis 2 Stunden und bei Bupivacain 4 bis 8 Stunden [1]. Epinephrin verlängert durch Vasokonstriktion die Wirkdauer, darf aber nicht an Endstromgebieten wie Fingern, Zehen, Nase und Penis angewandt werden. Vor der Injektion kann topisches Lokalanästhetikum in die Wunde aufgetragen werden. Anschließend ist eine ausreichende Wartezeit bis zum vollständigen Wirkungseintritt einzuhalten. In dieser Zeit kann sehr gut das Wundversorgungsset gerichtet werden, um anschließend die Wundversorgung zügig durchführen zu können.
Das Einwirken topischer Lokalanästhetika benötigt 10 bis 30 Minuten, bei der Infiltrationsanästhesie mit Lidocain oder Bupivacain zirka 10 Minuten [12].
Je nach Lokalisation kann eine Leitungsblockade durchgeführt werden, zum Beispiel eine Oberst-Leitungsanästhesie an Fingern und Zehen, ein volarer Fingerblock, ein Peniswurzelblock. Es gelten die gleichen Kriterien wie bei der Lokalanästhesie mit vorheriger Analgesie der Haut mittels EMLA®-Pflaster oder -Creme, Verwenden kleiner Nadeln (25 – 27 G) und langsamem Injizieren von körperwarmem Lokalanästhetikum. Das Überprüfen und die Dokumentation der Durchblutung, Motorik und Sensibilität vor dem Durchführen der Leitungsanästhesie sind obligat. Da die Leitungsanästhesie recht schmerzhaft sein kann und die Kinder häufig vor der Nadel Angst haben, ist eine Kombination mit der inhalativen Analgosedation mit Lachgas-Sauerstoff-Gemisch (s. u.) für die Injektion in Erwägung zu ziehen.
Als Nebenwirkungen der Lokalanästhetika sind ein metallischer Geschmack, Tinnitus, Zuckungen von Lippe und Zunge, Krampfanfälle, Agitationen, Rhythmusstörungen und Allergien beschrieben. Sie treten vor allem bei Lokalanästhetika vom Estertyp (Benzocain, Cocain, Tetracain) oder durch Konservierungsstoffe auf. Kreuzreaktionen zwischen Lokalanästhetika vom Estertyp und Amidtyp sind bisher nicht beschrieben [13]. Die Maximaldosen der einzelnen Lokalanästhetika sollten deshalb beachtet werden.
Inhalative Analgosedation
Als inhalative Analgosedation bietet sich ein Lachgas-Sauerstoff-Gemisch an (50 % Lachgas und 50 % Sauerstoff). Es wirkt anxiolytisch, analgetisch und sedierend und verflüchtigt sich innerhalb von Minuten bei Raumluftatmung. Auch hier ist die Kooperation des Kindes gefordert, welches durch eine Maske atmen muss. Daher ist dieses Verfahren ab einem Alter von vier Jahren zu empfehlen. Bei jüngeren Kindern kann allenfalls durch die Applikation eines Sedativums wie Midazolam eine Kooperation erreicht werden. Dabei steigt jedoch die Nebenwirkungsrate und es ist eine anschließende Überwachung notwendig. Eine Kombination von zwei Anästhesieverfahren wie Regionalanästhesie und inhalative Analgosedation ist gut möglich und nimmt dem Kind die Angst vor der Injektion [14].
Intravenöse Analgosedation, Vollnarkose
Bei ausgedehnten Wunden, starker Verschmutzung, Verdacht auf Fremdkörperreste, Begleitverletzungen von Sehnen, Muskeln, Gelenken und bei einem unkooperativen Kind, welches das Erreichen der oben genannten Ziele der Wundversorgung unmöglich gestaltet, empfiehlt sich die Versorgung in intravenöser Analgosedation beziehungsweise Vollnarkose.
Basisanalgetika nicht vergessen
Bei all den oben aufgelisteten Verfahren sollte auch an die Applikation von Basisanalgetika (z. B. Paracetamol, NSAR) gedacht werden, damit die Kinder auch nach dem Eingriff möglichst schmerzfrei sind.
Wundreinigung
Generell ist bereits zur Wundreinigung eine ausreichende Analgesie notwendig. Es gibt verschiedene Wundreinigungstechniken, wie beispielsweise mit feuchten Kompressen, durch Einweichen der Wunde oder durch Irrigation der Wundoberfläche mit einem steten Strahl. Welches Verfahren man verwendet, hängt von der Art der Wunde und dem Grad der Verschmutzung ab.
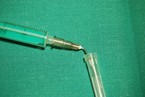
Mit feuchten Kompressen und dem Einweichen löst man eingetrockneten Schmutz und verbessert das Milieu der Wunde. Bei stärker verschmutzten Wunden ist eine Wundirrigation für die Reduktion des Infektionsrisikos wichtig, da hiermit kleine Schmutzpartikel, Fremdkörper und Bakterien am besten entfernt werden können [1]. Zur Irrigation lässt sich eine Spritze und eine abgebrochene Kanüle verwenden (Abb. 4). Bezüglich der Wahl der Spülflüssigkeit gibt es in der Literatur unterschiedliche Empfehlungen [1, 15 – 18]. Einigkeit besteht darüber, dass bei unkomplizierten, wenig verunreinigten Wunden mit gut durchblutetem Wundgrund und Wundrand eine ausgedehnte Wundreinigung nicht notwendig ist und isotone Kochsalzlösung oder Leitungswasser zur Reinigung ausreicht [1, 15, 16]. Eine prospektive Studie mit 530 Kindern, bei denen die Wunde entweder mit Kochsalzlösung oder Leitungswasser gereinigt wurde, zeigte keinen Unterschied bezüglich Wundinfektion [17].
Bei stärker verschmutzten Wunden besteht Uneinigkeit, ob die Wundreinigung mit Kochsalzlösung oder Leitungswasser ausreichend ist oder ob dafür verdünnte antiseptische Lösungen zu empfehlen sind. Argumente gegen die antiseptischen Lösungen sind deren Gewebetoxizität und die Hemmung der Proliferation von Fibroblasten [15, 16, 18].
Einen besonderen Aspekt stellt die Haarentfernung dar. Bei kleinen Wunden ist die Haarentfernung nicht notwendig, falls die Haare nicht die Wunde verunreinigen oder beim Wundverschluss stören. Sie können feucht mit dem Kamm von der Wunde weggestrichen werden. Die Rasur bis auf die Haut erhöht das Infektionsrisiko und kann die Wunde zusätzlich verunreinigen [19]. Das Rasieren der Augenbrauen ist obsolet, da diese entweder sehr langsam oder gar nicht nachwachsen.
Débridement
Für die Wundheilung sind vitale und saubere Wundverhältnisse unabdingbar. Mit dem Débridement wird nicht oder schlecht durchblutetes Gewebe mit dem Skalpell oder der Schere entfernt und die Wundränder werden begradigt, so dass der Wundverschluss besser durchführbar ist und die primäre Wundheilung verbessert wird [20]. Bei Wunden, die primär verschlossen werden sollen, ist das Débridement sofort durchzuführen. Bei sekundärer Wundheilung ist eine Nachkontrolle notwendig und eventuell ein späteres Débridement zu planen.
Wundverschluss
Unter dem Begriff Wundverschluss versteht man die Adaptation der Wundränder zur primären Wundheilung. Generell ist zu beachten, dass die Wundränder ohne Stufenbildung adaptiert werden und dass in der Tiefe keine Wundhöhle entsteht.
Oberflächliche Wunden, die die Subkutis nicht überschreiten, werden einschichtig, tiefere Wunden mehrschichtig verschlossen. Für die tieferen Schichten ist ein geflochtener resorbierbarer Faden zu empfehlen, zum Verschluss der Haut gibt es verschiedene Materialien wie Fadenmaterial, Wundkleber, Steristrips oder Klammern.
Bei Kindern werden wegen des schmerzhaften Entfernens in der Regel keine Klammern verwendet. Lediglich auf dem behaarten Kopf sind sie manchmal hilfreich.
Steristrips empfehlen sich für oberflächliche Wunden ohne Spannung. Sie können leicht vom Kind entfernt werden (Gefahr der Wunddehiszenz!). Häufig finden sie Verwendung als Wundverband zur zusätzlichen Reduktion der Spannung.
Die Stabilität von Wundklebern (Butylcyanoacrylat, Octylcyanoacrylat) entspricht einem Faden mit der Stärke 5 – 0. Wundkleber wird bei sauberen, frischen, trockenen und oberflächlichen Wunden verwendet. Die Wundränder sollten ohne Zug adaptierbar sein und die Wunde im Alltag nicht unter Spannung stehen. Unter dem Hautkleber können sich zwar Wundtaschen bilden, aber das Auftragen ist einfach und schmerzfrei und er löst sich von alleine mit der Hautschuppung nach fünf bis zehn Tagen ab. Kosmetisch erreichen korrekt angewandter Wundkleber und Faden vergleichbare Ergebnisse [21]. Mögliche Komplikationen sind Wundinfekt, das Aufreißen der Wunde und das Festkleben anderer Strukturen wie der Augenlider oder das Ankleben von Handschuh oder Kompresse bei der Applikation.
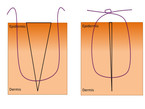
Das gängigste und häufigste Material zur Wundversorgung ist der Faden. Dabei wird für den Hautverschluss ein monofiler Faden verwendet. Die Fadendicke ist abhängig von der Lokalisation der Wunde, der Spannung der Wundränder und dem Alter des Patienten. Verwendet man nicht resorbierbaren Faden, ist die Fadenentfernung notwendig, bei resorbierbarem Faden ist die Resorptionszeit länger, bei geflochtenem Faden ist die Fremdkörperreaktion der Wunde stärker. Daher werden bei frischen Wunden vor allem im Gesicht nicht resorbierbare Fäden verwendet, um das beste kosmetische Ergebnis zu erreichen. Die Wundrandadaptation erfolgt in der Regel mit Einzelknopfnähten zur Vermeidung einer Infektion (Abb. 5). Die Zeit bis zur Wundheilung und Fadenentfernung hängt von der Lokalisation der Wunde ab (Kopf: 5 – 7 Tage; Stamm: 8 – 10 Tage; Extremitäten: 10 – 14 Tage) [1].
Bei Kindern verwenden wir bei oberflächlichen Wunden Steristrips, bei Wunden mit geraden Schnitträndern, die keine ausgedehnte Wundhöhle aufweisen und an spannungsarmen Stellen lokalisiert sind (Gesicht), Wundkleber, alle anderen Wunden werden mit Fadenmaterial verschlossen.
Als Verband empfiehlt sich einfach aufzutragendes Material, welches möglichst schmerzfrei entfernt werden kann beziehungsweise die Beurteilung der Wunde nicht behindert. Ein feuchtes Milieu begünstigt die Wundheilung und beeinflusst die Narbenbildung. Es beugt der Zelldehydratation und dem Zelltod vor, unterstützt die Angioneogenese und verbessert die Phagozytose, die Ausschüttung von Wachstumsfaktoren sowie die Reepithelisierung und damit das kosmetische Ergebnis [22]. Dabei gilt es jedoch zu beachten, wie häufig die Wunde beurteilt werden soll, das heißt wie oft der Verband gewechselt werden muss (je höher das Infektionsrisiko, desto häufiger der Verbandswechsel).
Adjuvante Therapie und Nachsorge
Falls nötig ist eine Ruhigstellung zur Vermeidung der Beanspruchung der Wunde möglich. Die Häufigkeit der Wundkontrollen hängt vom Infektionsrisiko ab. Nach der Fadenentfernung besteht ein Badeverbot für 24 Stunden, bis sich die Fadenkanäle verschlossen haben. Bei beginnender Narbenhypertrophie empfiehlt sich die Behandlung mit silikonhaltigen Pflastern oder Gels [23]. Ein guter Sonnenschutz wird bis zu drei bis sechs Monate nach Abschluss der Wundheilung empfohlen [1].
Genehmigter und bearbeiteter Nachdruck aus Ars medici 24/2012
Erschienen in: Der Allgemeinarzt, 2013; (9) Seite 51-56