Durch zeitnahes und individuelles Therapiemanagement lässt sich die Versorgung von Patienten mit Lymphödemerkrankungen optimieren. Der richtige Einsatz der Therapie erhöht die Effizienz der Behandlung, reduziert die Kosten und spart Zeit.
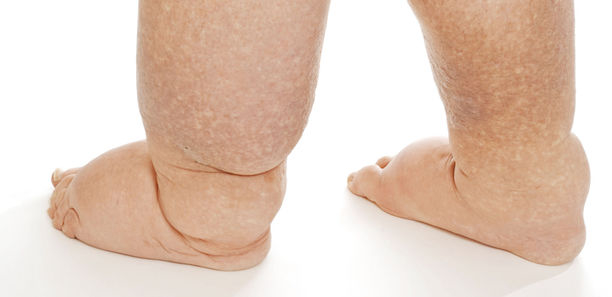
Das Lymphödem ist ein chronisches Krankheitsbild, bei dem eine Heilung zurzeit nicht erreichbar ist. Ziel der Therapie ist es, die Erkrankung in das Latenzstadium oder zumindest in das Stadium I zurückzuführen. Damit kann eine nachhaltige Linderung der Beschwerden erreicht werden. In der Folge kann die Therapie diesen Erfolg auf Dauer erhalten. 2 Fallbeispiele geben Aufschluss, was möglich ist.
Komplexe Physikalische Entstauungstherapie
Bei der 2-Phasen-Therapie handelt es sich um eine evidenzbasierte Therapie, wie Studien von Mosely et al. (2007), Devoogt et al. (2010), Lasininski et al. (2012) zeigen. In der Phase I, der Entstauung, soll die erhöhte Gewebeflüssigkeit mobilisiert werden. Ziel ist es, die Normalisierung der gestörten Homöostase im Interstitium einzuleiten. In der Phase II, der Konservierungs- und Optimierungsphase, geht es um die Verbesserung der Gewebebefunde und um die Optimierung von funktionellen Befunden (ROM).
MERKE:
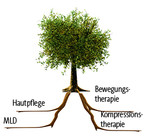
Ein unbehandeltes Lymphödem sollte immer erst mit den Maßnahmen der Phase I (Intensivphase) behandelt werden, d. h. tägliche Manuelle Lymphdrainage, Hautpflege, individuelle mehrlagige Kompressionstherapie, Bewegungstherapie, evtl. additive Physiotherapie. Die Therapie der Phase II beginnt erst nach weitgehender Entödematisierung. Es wird eine Strumpfversorgung angemessen und die Manuelle Lymphdrainage bzw. additive Physiotherapie nach Bedarf durchgeführt.
CAVE:
Ein zu früh angemessener lymphologischer Kompressionsstrumpf drückt in die Schwellung und verursacht Schmerzen! Die Patienten lehnen das Tragen der Kompressionsversorgung ab.
Tipp 1 für Patienten in der Phase II:
Alle 4 bis 6 Monate sollte vor einer neuen Strumpfversorgung eine kurze (5 Tage) Intensivphase erfolgen. Dadurch können die Umfangmaße und die Gewebebefunde optimiert werden.
Tipp 2:
Die Patienten sollten schon bei der Ausstellung der Heilmittelverordnung für die Intensivphase die Kostenübernahme für die lymphologische Strumpfversorgung bei der Krankenkasse beantragen. Denn durch Wartezeit beim Genehmigungsverfahren kann es zu einer Reödematisierung kommen.
Wie sollte eine korrekte Heilmittelverordnung aussehen?
Zunächst erfolgt die Verordnung der Therapie im Regelfall:
LY1 : 12 Behandlungen (2 x 6er HV)
LY2: 30 Behandlungen (5 x 6er HV)
LY3: 50Behandlungen (5 x 10er HV) für Pat. mit malignen Erkrankungen
Im Anschluss ist eine Verordnung außerhalb des Regelfalls möglich. Bei diesen Verordnungen außerhalb des Regelfalls muss eine medizinische Begründung mit einer prognostischen Einschätzung angegeben werden. Bei LY1 gibt es keine Verordnung außerhalb, es muss zunächst in LY2 übergeleitet werden. Eine Genehmigung durch die Krankenkassen ist von der Kasse abhängig, aber meist nicht erforderlich.
Bei Verordnungen außerhalb des Regelfalls ist die Verordnungsmenge nicht vorgeschrieben. Die Verordnungsmenge ist aber so zu bemessen, dass eine ärztliche Untersuchung längstens nach 12 Wochen erfolgt.
Heilmittel nach Maßgabe des Kataloges
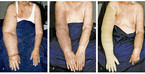
Für eine Intensivphase beispielsweise beim sekundären Armlymphödem sollten folgende Heilmittel nach Maßgabe des Kataloges verordnet werden:
- 10 x Manuelle Lymphdrainage 60 min
- 10 x Kompressionstherapie (einseitig oder bds., bitte angeben)
- 10 x Übungsbehandlung
Folgende Indikationsschlüssel kommen dabei zur Anwendung:
- LY1a/b prognostisch kurzfristiger Behandlungsbedarf – Diagnosen: bei venöser Insuffizienz, postthrombotischem Syndrom, nach interventioneller/operativer Behandlung von Gefäßerkrankungen, primärer/sekundärer Schädigung des Lymphsystems.
- LY2a prognostisch längerdauernder Behandlungsbedarf (Diagnose siehe LY1).
- LY3a prognostisch längerdauernder Behandlungsbedarf (Diagnosen Mammakarzinom, Malignome Hals-/Kopfbereich und des kleinen Beckens.
ICD-10-Code
Dies ist eine wichtige Angabe, da einige lymphangiologische Diagnosen das Heilmittelbudget nicht belasten.
189.0: Lymphödem andernorts nicht klassifiziert, Elephantiasis
C00-C97: bösartige Neubildungen nach OP/ Radiation bei Mammakarzinom, Malignome Kopf/Hals, Malignome des kleinen Beckens.
Q82.0: Hereditäres Lymphödem
Zu einer Heilmittelversorgung in der Intensivphase gehört auch die Verordnung des Materials für die Kompressionstherapie. Hierfür gibt es 2 Möglichkeiten:
1. Die Verordnung von Einzelmaterialien (nach Aufstellung des Therapeuten)
2. Die Verordnung von Lymphsets (vgl. Abb. 3)
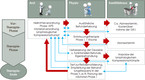
In keinem anderen medizinischen Fachgebiet ist die Zusammenarbeit zwischen den einzelnen Berufsgruppen wie zum Beispiel Ärzten, Physiotherapeuten und Sanitätsfachhandel so bedeutsam und entscheidend für den Therapieverlauf wie in der Lymphangiologie. Wichtig ist die vernetzte Zusammenarbeit mit regionalen Partnern wie beispielsweise Lymphnetzen oder einem Qualitätszirkel der Kassenärztlichen Vereinigung (vgl. Abb. 4).
Interessenkonflikte: Die Autorin hat keine deklariert.
Erschienen in: Der Allgemeinarzt, 2015; 37 (16) Seite 50-54