Das Symptom Anämie ist ein häufiger Befund in allen medizinischen Fachrichtungen. Als Nebendiagnose begleitet sie viele Krankheiten. Leichte Anämien sind häufig klinisch unauffällig, später dominieren meist Tachykardie, Leistungsminderung und Belastungsdyspnoe. Das mittlere korpuskuläre Volumen der Erythrozyten (MCV) gibt den wichtigen Hinweis auf die Genese der Anämie. Eine deutliche Erniedrigung lässt an die häufigste Ursache in der Praxis denken, die Eisenmangelanämie. Weitere Hinweise geben die restlichen Parameter des Blutbildes (Leukozyten, Thrombozyten) sowie die Retikulozyten. In einem Teil der Fälle kann die exakte Diagnose nur durch eine Knochenmarkspunktion gestellt werden.
Die Anämie ist definiert durch eine Erniedrigung der Hb-Konzentration im Blut, die eine verminderte Sauerstofftransportkapazität zur Folge hat. Leichte Anämien sind häufig symptomlos, bei ausgeprägter Blutarmut berichten die Patienten über Leistungsminderung und Belastungsdyspnoe. Wird die Anämie nicht als Zufallsbefund oder Nebendiagnose aufgedeckt, so ist der Hb-Wert bei Erstdiagnose oft bereits deutlich verringert. Die Symptome vorbestehender kardiorespiratorischer Erkrankungen wie KHK oder Herzinsuffizienz werden verstärkt.
Volumen beachten
Neben dem Hb-Wert ist dringend auf den Volumenstatus des Patienten zu achten. Selbst bei massivem akutem Blutverlust bleibt der Hb-Wert zunächst stabil und sinkt über Tage nach dem Blutverlust durch Flüssigkeitsverschiebung ins intravasale Lumen, nach Flüssigkeitssubstitution durch Infusionen natürlich schneller. Vorsicht ist auch bei starker Exsikkose geboten. Hier kann der Mangel an Flüssigkeit eine bestehende Anämie verschleiern. Dagegen haben Schwangere im 3. Trimenon durch physiologisch gesteigertes Plasmavolumen einen erniedrigten Hb-Wert und eine erniedrigte Erythrozytenzahl pro Blutvolumen, obwohl die Gesamterythrozytenzahl ebenfalls leicht ansteigt.
Wann einweisen, wann transfundieren?
Schwere Anämien, insbesondere wenn sich Hinweise auf einen raschen Verlauf oder eine akute Leukämie ergeben, sind ein Anlass für eine stationäre Abklärung (Tabelle 1a und b). Eine initiale Therapie mit Transfusionen sollte symptomorientiert erfolgen. Bei Patienten mit symptomatischen kardiovaskulären Erkrankungen besteht ein Transfusionsbedarf bereits bei einem Hb-Abfall unter 10 g/dl, sonst gesunde Patienten tolerieren in der Regel Werte bis ca. 7 g/dl ohne schwere Symptomatik.
Einteilung der Anämien
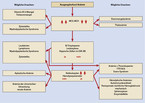
Die Einteilung nach Zellgröße liefert die ersten wichtigen Hinweise für die Differenzialdiagnose (Abb. 1). Nach dem mittleren korpuskulären Volumen (MCV) der Erythrozyten lassen sich die Anämien in makro-, normo- und mikrozytär einteilen. Veränderungen des mittleren zellulären Hämoglobins (MCH) gehen nahezu immer parallel mit dem MCV, d. h. mikrozytäre Anämien sind gleichzeitig hypochrom, makrozytäre Anämien hyperchrom. Aufgrund der parallelen Abweichungen von MCV und MCH ist die mittlere korpuskuläre Hämoglobinkonzentration (MCHC) auch in pathologischen Situationen mit wenigen Ausnahmen ein sehr stabiler Wert. Starke Abweichungen des MCHC weisen deshalb in erster Linie auf Messartefakte hin und sollten normalerweise bereits im Labor eine Ursachensuche auslösen.
Pathophysiologisch werden Produktionsstörungen im Knochenmark vom vermehrten Erythrozytenverlust unterschieden. Letzterer kann durch einen beschleunigten Abbau der Erythrozyten (hämolytische Anämien) oder durch Blutverlust entstehen und wird durch eine verstärkte Blutbildung (teilweise) kompensiert, sichtbar an einem Anstieg der Retikulozyten im peripheren Blut.
Anamnese und Befund
In der Anamnese muss immer nach Blutungen sowohl aktuell als auch in der Vorgeschichte (Ulcera? Hämorrhoiden? Teerstuhl? Menses?), Medikamenten, B-Symptomen (Fieber, Nachtschweiß, Gewichtsverlust) und vorbekannten chronischen Erkrankungen gefragt werden. Wichtig ist auch die Geschwindigkeit, mit der sich Symptome entwickelt haben. Bei der Untersuchung ist v. a. auf Blutungszeichen sowie Hinweise auf Systemerkrankungen zu achten. Bei Hämolyse kann ein Ikterus auffallen.
Für die Differenzialdiagnostik ergeben die Erythrozytenindizes erste wichtige Hinweise (Abb. 1). Bei erheblicher Verminderung von MCV und MCH denkt man insbesondere an eine Eisenmangelanämie, bei einer erheblichen Makrozytose an einen Vitamin-B12- oder Folsäuremangel. Geringe Abweichungen des MCH oder MCV vom Normwert sind wenig wegweisend. Die nächsten Hinweise finden sich in den restlichen Blutbildparametern. Thrombopenie, Leukozytose oder Leukopenie sind als Hinweis auf eine primäre Erkrankung des Knochenmarks zu werten. Wenn nicht umgehend eine Eisenmangelanämie als häufigste Ursache gesichert werden kann, sollte bei unklaren Anämien auch bei normalen Leukozytenzahlen ein mikroskopisches Differenzialblutbild angefordert werden, da atypische Zellen ebenfalls wichtige weiterführende Hinweise liefern können und nicht immer im maschinellen Differenzialblutbild erkannt werden. Im nächsten Schritt helfen Retikulozyten und weitere Hämolyseparameter bei der diagnostischen Klärung.
Eisenmangelanämie
Häufigste Ursache eines Eisenmangels ist der chronische Blutverlust, an zweiter Stelle steht die eisenarme Ernährung (z. B. bei veganer Kost). Seltener liegt eine Resorptionsstörung vor, z. B. bei Sprue. Nicht selten findet sich eine Kombination dieser Ursachen.
Die Diagnose einer Eisenmangelanämie ist gesichert bei einer mikrozytären Anämie mit eindeutig vermindertem Ferritinspiegel im Blut. Die Eisenkonzentration im Blut ist großen Schwankungen unterworfen und als diagnostischer Parameter nicht geeignet. Ferritin ist allerdings als Akut-Phase-Protein bei Entzündungen erhöht, dies kann einen Eisenmangel verschleiern und die Diagnostik erschweren. In diesen Fällen hilft die Messung des löslichen Transferrinrezeptors im Serum, der bei Eisenmangel steigt. Mit Hilfe der "Thomas-Plots" [3] (vgl. Kasten S. 30) wird der lösliche Transferrinrezeptor im Kontext des Entzündungsmarkers C-reaktives Protein und des Hb der Retikulozyten bewertet und hilft, auch bei einer Entzündungskonstellation einen Eisenmangel zu diagnostizieren.
Bei allen Patienten mit Eisenmangelanämie muss deren Ursache geklärt werden. Außer bei ganz offensichtlichen Ursachen (z. B. ausgeprägte Hämorrhoidalblutungen oder Menorrhagien) ist eine Suche nach okkulten Blutungsquellen im Gastrointestinaltrakt erforderlich (Hämoccult, endoskopische Diagnostik des GI-Trakts). Bei vaginalen Blutungen ist ggf. gynäkologische Klärung notwendig.
Zur Substitution wird in der Regel oral verabreichtes zweiwertiges Eisen verwendet. Eine Tagesdosis von 50 – 200 mg (zunächst mit niedrigerer Dosis die Verträglichkeit prüfen) morgens vor dem Frühstück wird empfohlen. Übelkeit, Obstipation und Bauchschmerzen sind häufige Nebenwirkungen und gefährden die Mitarbeit der Patienten. Oft kann eine Verteilung der Einnahme auf mehrere Dosen (z. B. in Tropfenform) oder eine Einnahme nach statt vor dem Essen die Compliance verbessern. Der Erfolg der Therapie ist durch Blutbildkontrollen alle zwei bis vier Wochen zu kontrollieren. Spätestens nach vier Wochen ist ein deutlicher Hb-Anstieg zu erwarten. Bleibt dieser aus, so muss die Zuverlässigkeit der Einnahme mit dem Patienten besprochen und ggf. nochmals die Suche nach einer Blutungsquelle und/oder Resorptionsstörung aufgenommen werden. Der gelegentlich propagierte Eisenresorptionstest, d. h. die Messung des Serumeisens vor und nach einer Gabe von oralem Eisen, ist nicht validiert und deshalb obsolet. Nach drei bis sechs Monaten sollten sich Hb und Serumferritin normalisiert haben. Bei schweren enteralen Resorptionsstörungen oder Unverträglichkeit kann eine intravenöse Eisensubstitution erfolgen. Diese birgt die Gefahr von schweren anaphylaktischen Reaktionen, die allerdings mit den modernen Präparaten sehr selten geworden sind.
Auch bei den Thalassämien sind MCH und MCV stark erniedrigt. Im Blutausstrich sieht man eine Anisozytose mit Targetzellen. Zur Diagnosesicherung wird die Hb-Elektrophorese herangezogen. Die heterozygote Thalassämia minor ist in aller Regel nicht therapiebedürftig. Die homozygote Form (Thalassämia major) geht mit schwersten Anämien und regelmäßigem Transfusionsbedarf bereits im Kleinkindesalter einher.
Anämien bei chronischen Erkrankungen sind typischerweise nur leicht mikrozytär oder aber normozytär (s. u.).
Makrozytäre Anämien
Sowohl bei Vitamin-B12- als auch bei Folsäuremangel wird die Erythropoese im Knochenmark aufgrund einer DNA-Synthesestörung bei erhöhtem Zellumsatz ineffizient. Eine große Zahl von mikroskopisch vergrößerten Erythrozytenvorläufern (Megaloblasten) geht bereits im Knochenmark wieder zugrunde. Die LDH als Zellumsatzparameter ist erhöht, die Retikulozytenzahl aber niedrig. Bei schwereren Fällen findet man zusätzlich häufig eine Granulopenie und/oder eine Thrombozytopenie.
Vitamin-B12-Mangel
VitaminB12 wird im Magen an Intrinsic factor gebunden und im terminalen Ileum resorbiert. Ist der Vitamin-B12-Mangel durch eine Autoimmungastritis mit Intrinsic-factor-Mangel und konsekutiver Resorptionsstörung bedingt, wird diese Unterform als perniziöse Anämie bezeichnet, bei der sich meist Antikörper gegen Intrinsic factor oder Parietalzellen im Serum nachweisen lassen. Andere Ursachen für einen Vitamin-B12-Mangel sind u. a. eine Gastrektomie oder eine Ileitis terminalis. Der Vitamin-B12-Mangel kann neben der Anämie sowohl zentralnervöse Störungen als auch eine Polyneuropathie verursachen, die gelegentlich das klinische Bild dominieren.
Nach der Diagnosestellung wird eine parenterale Gabe von Vitamin B12 begonnen (üblicherweise Hydroxycobalamin i. m.), die in der Regel lebenslang fortzuführen ist. Während der Therapieeinleitung kommt es zu einem raschen Anstieg der Retikulozyten und Kaliumverbrauch, weswegen das Kalium im Serum kontrolliert werden sollte.
Sowohl Vitamin B12 als auch Folsäure können heute im Serum recht zuverlässig gemessen werden. Bei Befunden an der Grenze des Normbereiches existiert jedoch eine diagnostische Grauzone. Erhöhte Homocysteinwerte können auf einen Mangel sowohl von Folsäure als auch Vitamin B12 hinweisen, allerdings sind diese Bestimmungen nicht sehr spezifisch [1]. Der Schilling-Test, bei dem radioaktiv markiertes Cobalamin verabreicht und danach die Ausscheidung im Urin gemessen wird, wird kaum noch benötigt.
Folsäuremangel
Ein Folsäuremangel tritt in erster Linie bei ungenügender Zufuhr mit der Nahrung auf. Eine klassische Konstellation ist der Alkoholabusus in Kombination mit unausgewogener Ernährung. Darmerkrankungen können zu Resorptionsstörungen führen, ebenso in seltenen Fällen Antikonvulsiva (Phenylhydantoin und Primidon). Folsäuredefizite können durch die entsprechende orale Gabe effektiv behandelt werden. Folsäuregaben können die neurologischen Symptome bei Vitamin-B12-Mangel verstärken, weshalb die alleinige Gabe von Folsäure nicht erfolgen darf, wenn ein Vitamin-B12-Mangel nicht sicher ausgeschlossen wurde.
Ausgeprägte makrozytäre Veränderungen sieht man unter der Therapie mit Zytostatika aus der Gruppe der Antimetaboliten (u. a. Cytosinarabinosid, Hydroxyurea oder Methotrexat). Da die Therapie in der Regel bekannt ist, wird dies nicht zu diagnostischen Problemen führen.
Weitere Ursachen makrozytärer Anämien
Weitere Ursachen einer Anämie mit gelegentlich erhöhtem MCV sind myelodysplastische Syndrome (MDS), Lebererkrankungen, chronischer Alkoholismus, Hypothyreose und Kupfermangel. Anämieformen, die mit einer starken Retikulozytenvermehrung einhergehen, sind ebenfalls makrozytär, weil die Retikulozyten größer als Erythrozyten sind.
Wann an Leukämie denken?
Bei Abweichungen in mehreren Zellreihen muss immer auch an eine Leukämie oder eine andere primäre Erkrankung des Knochenmarks gedacht werden. Die Retikulozytenzahl ist in diesem Fall nicht erhöht, außer bei gelegentlich begleitender Autoimmunhämolyse bei lymphatischen Neoplasien. Vielfach finden sich diagnostische Hinweise im mikroskopischen Differenzialblutbild, gelegentlich ist aus diesem bereits eine sichere Diagnosestellung möglich. Solche wegweisenden Befunde sind unreife Zellen ("Blasten") bei akuten Leukämien, Lymphozytenvermehrung oder atypische Lymphozyten bei lymphatischen Leukämien bzw. malignen Lymphomen, dysplastische Zellformen beim MDS, massive Linksverschiebung und Basophilie bei der Chronischen Myeloischen Leukämie.
In vielen Fällen erlaubt das Blutbild jedoch nur eine unsichere oder gar keine konkrete Aussage. Die Diagnosestellung muss dann durch eine Knochenmarkuntersuchung erfolgen. Hierzu wird sowohl Knochenmarkaspirat für die Zytologie und Spezialuntersuchungen (insbesondere zytogenetische Untersuchung) entnommen als auch eine Stanzbiopsie für die histologische Aufarbeitung. Wenn die Untersuchung von einem Hämatologen mit angeschlossenem Labor vorgenommen wird, kann die zytologische Beurteilung direkt erfolgen und daraufhin die ergänzende Diagnostik gezielter geplant und ggf. versandt werden.
Eine differenzierte Diskussion der möglichen Knochenmarkerkrankungen würde den Umfang dieses Beitrages überschreiten. Wichtig ist jedoch, dass bereits der Allgemeinarzt die Dringlichkeit der Untersuchung und Therapieeinleitung mit abschätzen kann. Während z. B. myelodysplastische Syndrome und chronische lymphatische Leukämien einen protrahierten Verlauf zeigen und elektiv ambulant abgeklärt werden können, kann sich der Zustand von Patienten mit akuten Leukämien innerhalb weniger Tage dramatisch verschlechtern, so dass unverzüglich die Einweisung in ein hämatologisches Zentrum erfolgen sollte (vgl. auch Tabelle 1).
Thomas-Plot
Akut-Phase-Reaktionen, wie sie z. B. bei chronischen Erkrankungen (Entzündungen, Niereninsuffizienz, Tumoren) vorkommen, können die Diagnostik eines Eisenmangels erschweren, da hierbei Ferritin als Akut-Phase-Protein erhöht ist, ohne dass ein Eisenmangel vorliegen muss. Dann hilft der sogenannte „Thomas-Plot“ weiter. Dazu braucht man folgende Parameter:
- Hämoglobingehalt der Retikulozyten (erlaubt Aussage zum Eisenbedarf der Erythropoese)
- Ferritinindex (Quotient aus löslichem Transferrinrezeptor und Logarithmus des Ferritinwertes = Marker für die Speichereisenreserve)
Die Patientenwerte werden dann in eine Vierfeldertafel eingetragen, wobei jeder Quadrant einer Diagnose zugeordnet ist.
- Anämie bei chronischer Erkrankung (ACD)
- latenter Eisenmangel
- klassischer Eisenmangel
- ACD und funktioneller Eisenmangel sowie Thalassämien
Hämolytische Anämien
Bei den hämolytischen Anämien ist die Lebenszeit der einzelnen Erythrozyten vermindert, was typischerweise durch eine verstärkte Neuproduktion im Knochenmark mit erhöhter Retikulozytenzahl im Blut (teilweise) kompensiert wird. Die Retikulozytenzahl muss in Bezug auf das Ausmaß der Anämie beurteilt werden, hierbei hilft in Grenzfällen die Berechnung des Retikulozytenproduktionsindex (RPI) [2]. Die genaue Berechnung ist in Tabelle 2 dargestellt. Eine nur mäßig erhöhte Retikulozytenzahl spricht für eine zusätzliche Bildungsstörung im Knochenmark. Im Serum wird bei Hämolyse das Haptoglobin erniedrigt gemessen (jedoch falsch hoch bei Entzündungsreaktionen), indirektes Bilirubin und LDH sind erhöht.
Die häufigste erworbene Form einer hämolytischen Anämie ist die Autoimmunhämolyse (AIHA). Diese kann idiopathisch oder in Zusammenhang mit Autoimmunerkrankungen oder niedrig malignen Lymphomen auftreten. Bei jeder Autoimmunhämolyse ist außerdem an eine Assoziation mit Medikamenten zu denken, mögliche Auslöser sollten abgesetzt werden.
Bei der Paroxysmalen Nächtlichen Hämoglobinurie (PNH) verursacht eine erworbene Mutation in der Hämatopoese einen Verlust spezifischer Oberflächenproteine. Dies führt zu einer gesteigerten Empfindlichkeit dieser Zellen gegenüber dem Komplementsystem und einer intravasalen Hämolyse, die sich nachts verstärken kann, was der Krankheit den Namen gab. Das Risiko venöser Thrombosen, auch an atypischen Orten wie Pfortader oder Lebervenen, ist bei der PNH erhöht.
Bei der Thrombotisch Thrombozytopenen Purpura (TTP) sowie beim Hämolytisch Urämischen Syndrom (HUS) findet man eine Thrombopenie kombiniert mit hämolytischer Anämie. Im Blutausstrich finden sich Fragmentozyten. Hinzu kommen außerdem Niereninsuffizienz, neurologische Symptome, Fieber und andere Allgemeinsymptome.
Direkter mechanischer Stress kann ebenfalls eine Hämolyse verursachen. Eine relativ häufige Ursache ist hierbei eine künstliche Herzklappe, insbesondere bei Fehlfunktion z. B. paravalvulärem Leck. Weitere mögliche Ursachen sind Infekte und Toxine. Angeborene Störungen der Erythrozyten werden überwiegend in der Kindheit diagnostiziert, insbesondere die hereditäre Sphärozytose (Kugelzellanämie) kann bei milder Ausprägung klinisch weitgehend unauffällig bleiben und dann erst spät diagnostiziert werden. Typisch für die Kugelzellanämie ist ein erhöhtes MCHC.
Anämie der chronischen Erkrankung
Eine der häufigsten Anämieformen in der täglichen Praxis ist die Anämie der chronischen Erkrankung (ACD), die im Wesentlichen auf einer Eisenverwertungsstörung beruht. Ausgelöst wird sie durch chronische Infektionen, Autoimmunerkrankungen und Malignome. Aufgrund von Zytokinausschüttung wird vermehrt Hepcidin gebildet, das sowohl die Eisenaufnahme als auch Eisenverwertung hemmt. Die ACD als alleinige Anämieursache ist nur selten sehr schwer ausgeprägt, deshalb muss bei niedrigen Hb-Werten eine zusätzliche Ursache (Blutung, Eisenmangel, Hämolyse) ausgeschlossen werden. Die Messung des Serumhepcidin ist für die praktische Diagnostik (noch) nicht ausreichend standardisiert.
Patienten mit chronischer Niereninsuffizienz leiden häufig unter einer teilweise ausgeprägten Anämie. Da der zentrale pathophysiologische Faktor in der Regel ein Erythropoetinmangel ist, kann dies durch eine entsprechende Substitution ausgeglichen werden. Die Messung des Serumspiegels ist differenzialdiagnostisch nicht etabliert.
Interessenkonflikte:
Erschienen in: Der Allgemeinarzt, 2012; (3) Seite 26-31