Dialysepatienten sind häufig von arteriellen Gefäßerkrankungen betroffen. Bei einer kritischen Extremitätenischämie ist es allerhöchste Zeit für eine adäquate Behandlung – dem betroffenen Patienten droht sonst die Amputation.
Bei der peripheren arteriellen Verschlusskrankheit (pAVK) zeigt sich eine weltweite Zunahme. Aktuelle statistische Auswertungen gehen von circa 200Mio. betroffenen Menschen aus, bei denen eine symptomatische pAVK diagnostiziert wurde. Neben einem stetigen Anstieg der pAVK-Prävalenz in den Industriestaaten ist aufgrund der steigenden Diabeteszahlen in Schwellenländern von einem immensen Anstieg an Gefäßerkrankungen in den nächsten Jahren und Jahrzehnten auszugehen (1, 2).
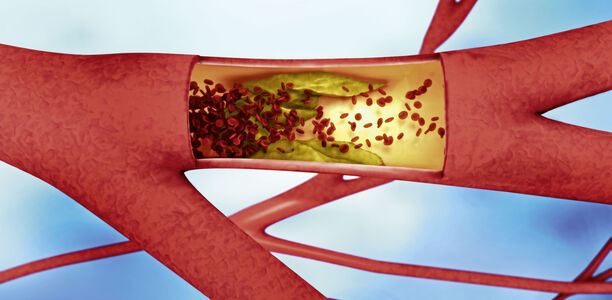
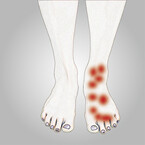
Regionale Unterschiede der Krankheitshäufigkeit werden durch die ethnische Herkunft, das Einkommen und das Geschlecht beeinflusst.Ob genetische Faktoren neben der ethnischen Zugehörigkeit einen signifikanten Einfluss zeigen, ist derzeit noch nicht wissenschaftlich geklärt. Es ist allerdings davon auszugehen, dass genetische Dispositionen (z.B. Fettstoffwechselstörungen) im Vergleich zu Risikofaktoren wie Diabetes mellitus und Nikotinabusus nicht den gleichen Stellenwert haben. Die kritische Extremitätenischämie (englisch: chronic limb threatening ischemia: CLTI) ist die schwerste Form einer chronischen Mangeldurchblutung einer Extremität (Abb. 1). Auch in Deutschland beobachten Experten seit 2005 – neben einem kontinuierlichen Anstieg der pAVK-Prävalenz – eine Zunahme der pAVK-Komplexität mit einem überproportionalen Anstieg der kritischen Extremitätenischämie (2). Jährlich werden in Deutschland etwa 40.000Beinamputationen durchgeführt, 70% davon bei Menschen mit Diabetes. Mithilfe moderner interventioneller und gefäßchirurgischer Behandlungsverfahren – besonders an den Unterschenkel- und Fußarterien – ließen sich rund 80% der Majoramputationen vermeiden, sofern eine rechtzeitige Diagnostik und Therapie stattfinden.
Definition der kritischen Extremitätenischämie
Bei der kritischen Extremitätenischämie liegen Ruheschmerzen und/oder bereits trophische Haut- und Gewebeläsionen vor. Ruheschmerzen betreffen stets die Region der "letzten Wiese", d.h. meist den Vorfuß. Unter Beintieflage kommt es häufig zu einer Linderung der Schmerzsymptomatik. Das Verhältnis zwischen Sauerstoffversorgung und dem metabolischen Bedarf der Muskel- und Weichteilgewebe ist in Ruhe nicht mehr ausreichend (8).
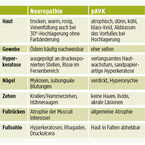
Die kritische Ischämie gilt als entscheidender Prognosefaktor für das Abheilen einer peripheren Läsion und wird neben der klinischen Symptomatik durch einen Knöchel-Arm-Index (ABI) von <0,5 und einem Pulsatilitätsindex ≤1,2 mit einer Sensitivität und Spezifität von 36% und 86% bzw. 87% und 67% beschrieben. Eine klinisch nicht immer einfache Befunddifferenzierung zwischen einer Neuropathie und einer pAVK zeigt Tabelle 1.
Chronisch kritische Extremitätenischämie
Die klinische Manifestation einer peripheren arteriellen Verschlusskrankheit reicht von einer milden intermittierenden Claudicatio bis zur Extremitäten bedrohenden CLTI. Ursächlich für das klinische Bild ist die Arteriosklerose der großen zuführenden Gefäße der Extremitäten, wodurch es zu einer endothelialen Dysfunktion und im Weiteren zu einer lipidreichen Plaquebildung in der Gefäßwand mit einem lokalen Inflammationsprozess kommt. Hieraus resultiert eine lokale Kalk-. Thrombus- und Plaquebildung, die letztlich zu einer Verringerung des Gefäßlumens bis zum Gefäßverschluss führt. Entsprechend der Risikokonstellation sind bei Diabetikern vermehrt die Unterschenkelarterien betroffen, bei Rauchern die Becken- und femoropopliteale Strombahn (3).
Zusätzlich weisen Diabetespatienten vermehrt komplexe Gefäßverschlüsse auf als einfache kurzstreckige Stenosen (4). Ein typisches Charakteristikum eines CLTI-Patienten sind Obstruktionen oder Verschlüsse der kleinen Gefäße in den Extremitäten, insbesondere in den Metatarsalgefäßen (5). Diabetiker und niereninsuffiziente Patienten sind dabei signifikant häufiger betroffen. Die sehr häufig begleitende Polyneuropathie des Diabetespatienten mit daraus resultierendem verringertem Schmerzempfinden unterdrückt den ischämischen Schmerz bzw. einen Wundschmerz, wodurch die betroffenen Patienten erst verzögert vorstellig werden.
Bei Patienten mit CLI ist eine schnelle und ausreichende Revaskularisation unabhängig von den eingesetzten Behandlungstechniken oberstes Ziel in einem gefäßmedizinischen Zentrum.
Konservative Therapie
Eine rein konservative Therapie der CLTI ist mit einer sehr ungünstigen Prognose hinsichtlich einer Amputation verbunden. Rund 40% der betroffenen Patienten werden im Durchschnitt bei einer rein konservativen Therapie nach
6Monaten amputiert (1,2). Somit sollte bei jedem Patienten mit CLTI die Möglichkeit einer Revaskularisation überprüft werden.
Im Rahmen konservativer Begleitmaßnahmen zur Revaskularisation können über Tage bis Wochen intravenöse oder intraarterielle PGE-I-Infusionen eingesetzt werden, wodurch über rheologische Mechanismen vor allem im Mikrozirkulationsbereich lokale Wundbereiche besser perfundiert werden. Eine begleitende, initial empirische, im Verlauf gezielte antibiotische Therapie von infizierten Wunden sollte man so rasch wie möglich initiieren.
Regelmäßige Wundabstriche zur mikrobiologischen Beurteilung sowie nicht austrocknende Verbände durch ein geschultes Wundmanagement-Team gehören heute zu den Standards in Gefäßzentren. Eine begleitende individuell auf die klinische Situation des Patienten ausgerichtete Schmerz- und Physiotherapie verhindert eine weitere Immobilisierung des Patienten. Durch spezielle Verbands- und Entlastungsschuhe oder auch speziell angepasste Orthesen kann die Mobilität weiter aufrechterhalten werden, sofern keine medizinischen Gründe für eine Immobilisierung sprechen.
Gerade bei multimorbiden Patienten muss präoperativ die Operationsfähigkeit erst hergestellt werden. Sehr häufig liegen kardiale Dekompensationszustände vor, die medikamentös rekompensiert werden müssen. Bei Nachweis myokardialer Ischämien bedarf es einer Koronarangiografie mit Intervention. Hyperglykämische Stoffwechselsituationen bei Diabetespatienten sind präoperativ zu korrigieren. Nicht selten liegt eine schwere chronische Niereninsuffizienz vor, die präoperativ oder präinterventionell durch eine nephrologische Stellungnahme begutachtet werden muss, um eine Dialyseindikation zu überprüfen.
Ziel der postoperativen konservativen Therapie ist es, alle Maßnahmen zu ergreifen, um das erreichte Revaskularisationsergebnis zu erhalten. Hierzu gehört eine optimale Lokalbehandlung der Nekrose- bzw. Operationswunden durch geschultes Personal. Druckstellen sollte man vermeiden, um eine ausreichende Perfusion in diesem Bereich zu erreichen. Infektionen müssen früh erkannt und lokal bzw. systemisch behandelt werden. Nicht selten tritt durch die erreichte Revaskularisation ein Reperfusionsödem auf, das durch einen erhöhten interstitiellen Druck lokale Minderperfusionen hervorrufen kann. Durch gezielte physiotherapeutische Maßnahmen können hier Entstauungsmaßnahmen durch eine Lymphdrainage erfolgen. Zur medikamentösen Therapie nach endovaskulärer oder operativer Maßnahme gehört die antithrombozytäre Therapie, um lokale Thrombosekomplikationen im Revaskularisationsbereich zu vermeiden. Diese Therapie muss individuell an die Blutungsrisikosituation des Patienten und seiner Begleitmedikation (z.B. Antikoagulation) angepasst werden. Sekundärprophylaktische Behandlungen der kardiovaskulären Risikofaktoren (Dyslipoproteinämie, arterielle Hypertonie, Diabetes mellitus) richten sich nach den nationalen und internationalen Empfehlungen, wobei insbesondere bei kardiovaskulären Hochrisikopatienten ein LDL-Wert <70mg/dl anzustreben ist (6).
- Wie bei allen anderen pAVK-Patienten ist bei Patienten mit kritischer Extremitätenischämie ein multidisziplinärer Behandlungsansatz zur Kontrolle der Schmerzen, der kardiovaskulären Risikofaktoren und der Komorbidität notwendig.
- Patienten mit kritischer Ischämie und Infektion sollen eine systemische antibiotische Therapie erhalten.
- Als medikamentöse Behandlungsmethode bei Patienten mit kritischer Extremitätenischämie, die nicht für eine Revaskularisation geeignet sind, können Prostanoide eingesetzt werden.
Indikation zur revaskularisierenden Therapie
Eine Indikation zur endovaskulären Therapie oder Bypassoperation sollte idealerweise interdisziplinär durch Angiologen, Gefäßchirurgen und Radiologen gestellt werden, wobei vor allem auf den richtigen Zeitpunkt zur Revaskularisationsmaßnahme geachtet werden sollte: Ein zu lang durchgeführter konservativer Therapieversuch kann eine klinische Situation hervorrufen, die eine Revaskularisationsmaßnahme durch eine fortgeschrittene Infektion bedingt oder große Nekroseausbildung nicht mehr möglich macht. Zur Vermeidung dieser Situation gilt die Empfehlung, bei neu aufgetretenen spontanen Wunden, Nekrosen oder Infektionen im Extremitätenbereich bei Patienten mit hohem Risikoprofil (bekannte pAVK, Diabetes mellitus, Dialysepatienten, u.a.) eine direkte gefäßmedizinische Diagnostik und ggf. revaskularisierende Maßnahme zu veranlassen.
Die aktuellen Empfehlungen der europäischen Gesellschaft für Kardiologie (ESC) sowie die S3-Leitlinien der Deutschen Gesellschaft für Angiologie (6,8) empfehlen eine Revaskularisation interdisziplinär anhand der lokalen Gegebenheiten und Expertise festzulegen.
Das 2015 erstmalig vorgestellte CRITISCH-Register (7) zeigte bei 1.200 in spezialisierten Gefäßzentren behandelten Patienten mit CLTI, dass grundsätzlich kein Unterschied zwischen einer endovaskulären Therapie und einer Bypassoperation hinsichtlich des primären Endpunkts Tod oder Amputation bestand. Das größte Risiko eines Patienten, während eines Aufenthalts zu versterben, bestand bei Patienten mit durchgeführter Amputation. Ein amputationsfreies Überleben konnte in dem Register in über 70% der Fälle nach Revaskularisation dokumentiert werden. Bei Patienten mit CLI ist eine schnelle und ausreichende Revaskularisation unabhängig von den eingesetzten Behandlungstechniken oberstes Ziel.
Bildgebende Diagnostik bei kritischer Extremitätenischämie
Neben der klinischen Befunderhebung mit Dokumentation und Beschreibung einer Wunde, einer Nekrose und einer Infektion sollte im ersten Schritt eine nicht invasive pAVK-Diagnostik stattfinden. Neben der Erhebung des Pulsstatus sollte als Basisdiagnostik eine ABI-Messung erfolgen (Dopplerdruckmessung), ggf. ergänzt durch eine Oszillografie (6).
Eine Entscheidung für oder gegen eine Revaskularisation bedarf im nächsten Schritt einer Beschreibung der Stenose- oder Verschlusslänge der arteriellen Gefäße der betroffenen Extremität, sowie deren Morphologie (Kalzifikation, Thrombus, fibrotischer Verschluss). Zudem muss erhoben werden, inwiefern zuvor implantierte Stents oder Bypässe sich noch offen oder stenosiert zeigen (1,6).
Die Duplexsonografie ist zur Beantwortung dieser Fragen in nahezu allen Gefäßabschnitten der unteren Extremität als Standardverfahren etabliert, kann jedoch im Beckenarterienbereich durch starke Luftüberlagerungen und Adipositas erschwert sein. Im Bereich der Unterschenkelarterien können starke Schallauslöschungen bei stark kalzifizierten Läsionen ebenfalls eine Einschränkung der Aussagekraft bewirken. Je nach Befunderhebung kann sich direkt an diese Diagnostik die Entscheidungsfindung zur operativen oder endovaskulären Therapie anschließen.
Gerade bei Patienten mit einer eingeschränkten Nierenfunktion sollte anhand der Duplexbefunde abgewogen werden, ob eine weitergehende, nichtinvasive Diagnostik mittels kontrastmittelgestützter CT/MRT-Angiografie sinnvoll erscheint und zusätzliche Informationen erbringt. In vielen Zentren wird eine direkte diagnostische digitale Subtraktionsangiografie (DSA) in Interventionsbereitschaft geplant (6, 8). Moderne Kliniken und Katheterlabore verwenden zur Kontrastmitteleinsparung heutzutage CO2-Angiografien, womit sich bis zum Vorfußbereich und durch moderne Algorithmen eine sehr gute Darstellbarkeit der Gefäße erreichen lässt. Neueste Entwicklungen gehen in die Richtung, Gefäße intraluminal durch einen intravaskulären Ultraschall oder durch die optische Kohärenztomografie darzustellen und Läsionen und Verschlüsse morphologisch exakt zu analysieren. Mittels dieser Techniken kann weitestgehend auf die Gabe von Kontrastmittel intraarteriell verzichtet werden.
Interventionelle Therapie
Die Art und Weise der Revaskularisation wird stark beeinflusst durch die Expertise des jeweiligen Zentrums. Grundsätzlich wird heute eine endovaskuläre Primärtherapie verfolgt, da sich die technischen Möglichkeiten in den letzten Jahren sehr weiterentwickelt haben. Bei Versagen dieser Therapie oder geringer Wahrscheinlichkeit einer effektiven Revaskularisation sollte die Möglichkeit einer Bypassoperation erwogen werden.
- Bei Mehretagenläsionen hat die Beseitigung von Einstromhindernissen Priorität vor der Behandlung nachgeschalteter Läsionen.
- Bei Patienten mit kritischer Ischämie sollen Einstrom- und nachfolgend Ausstromläsionen – soweit möglich – durch eine interventionelle Therapie behandelt werden.
- Bei gleichzeitigem Vorliegen hochgradiger Stenosen oder Verschlüssen der Arteria femoralis communis, der Art. profunda femoris und Läsionen in der aortoiliakalen Einstrombahn und/oder der femoropoplitealen Ausstrombahn ist eine Kombination von offen-operativen Verfahren und intraoperativer endovaskulärer Behandlung der weiteren Läsionen sinnvoll (sog. Hybrideingriff).
Endovaskuläre Therapie
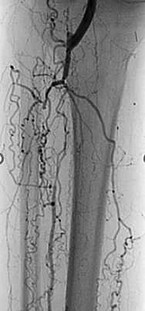
Die endovaskuläre Rekanalisation arterieller Läsionen ist seit vielen Jahren neben der Bypassoperation eine anerkannte und effektive Therapieoption (1,6,8) (Abb. 2). Moderne Nitinolstents können im Vergleich zur alleinigen Ballonangioplastie die Restenoserate signifikant reduzieren im femoropoplitealen Stromgebiet.
In den letzten Jahren ist es jedoch immer mehr zum Standard geworden, soweit wie möglich auf metallische Scaffolds zu verzichten und einer "Leave-nothing-behind"-Therapie zu folgen. Insbesondere in der gelenküberschreitenden Strombahn ist dies sehr gut nachvollziehbar. Die alternative Therapieoption mittels Drug Eluting Balloon (DEB) entsprechende Interventionen durchzuführen, hat spätestens seit den "Proof-of-Concept"-Studien in der peripheren endovaskulären Therapie einen herausragenden Stellenwert.
Die endovaskuläre Therapie mit einem Nitinolstent (Nitinol ist eine Nickel-Titan-Legierung und der bekannteste Vertreter der Formgedächtnis-Legierungen. Der Name Nitinol ist ein Akronym für Nickel Titanium Naval Ordnance Laboratory) stellt eine etablierte Revaskularisationsstrategie im Bereich der iliakalen und femoropoplitealen Strombahn dar, jedoch liegt auch in den kürzlich publizierten Stentstudien die Wahrscheinlichkeit für eine Reintervention weiterhin in vielen Fällen über 20% nach 12Monaten (9 – 11). Die Läsionslänge korreliert dabei bekanntermaßen negativ mit der primären Offenheitsrate. Der Restenoseprozess ist als multifaktoriell und komplex zu bezeichnen, wobei Faktoren wie die induzierte Gefäßwandverletzung durch die Angioplastie, der ständige Stentdruck (chronic outward force) auf die Gefäßwand, suboptimale Blutflussverhältnisse und mechanische Faktoren die größten Bedeutungen haben.
Durch die ständige mechanische Beanspruchung des Stents, die umso höher in gelenküberschreitenden Gefäßabschnitten ist, wird ein implantierter Stent in mehrfacher Hinsicht großen physikalischen Kräften ausgesetzt. Im Vordergrund der aktuellen Stententwicklung stehen aus den genannten Gründen deshalb sog. biomechanische Stents. Diese zeichnen sich durch einen ausgewogenen Kompromiss aus Flexibilität, ausreichender Radialkraft und niedrigen Frakturraten, vor allem auch im poplitealen Segment, aus. Im Unterschenkel sind die unbeschichteten Nitinolstents als auch ballonmontierte unbeschichtete Metallstents aufgrund ungünstiger Studienergebnisse keine signifikante Option, ganz im Gegensatz zum Drug Eluting Balloon oder Drug Eluting Stent.
Bypassoperation
Bei langen Verschlüssen gilt die Bypassoperation im Stadium der chronisch kritischen Extremitätenischämie als etablierte Therapie (1,6,7,8), wobei man vor allem auch crurale und pedale Anschlüsse bei sehr peripheren Gefäßverschlüssen durchführen kann. Vorrangig wird autologes Venenmaterial verwendet, wodurch sich Bypass-Offenheitsraten nach einem Jahr von etwa 80 – 90% erreichen lassen(1,6,8,12). Bypässe aus Kunststoff wie PTFE (Polytetrafluorethylen) gelten bei fehlendem oder insuffizientem autologen Venenmaterial als Alternative, die Offenheitsraten sind jedoch im Verlauf deutlich niedriger als bei Venenbypässen. Technisch sind alle Anschlussvarianten möglich: femorocrural, popliteocrural, popliteopedal. Nach distal sind kaum Grenzen der Anschlussfähigkeit gegeben, da nicht nur die A. dorsalis pedis und A. tibialis posterior verwendet werden können, sondern auch plantare Arterien mit sehr kleinen Durchmessern. Dabei unterscheidet sich die Offenheitsprognose nicht zwischen den cruralen Anschlussgefäßen, sondern wird vielmehr beeinflusst durch einen funktionierenden arteriellen Abstrom. Postoperative Wundheilungsstörungen und Infektionen sind große Herausforderungen, die in 15 – 25% der Fälle auftreten und den stationären Aufenthalt verlängern (7).
Ausblick
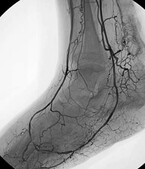
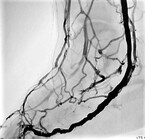
Vor allem im endovaskulären Therapiebereich sind in den letzten Jahren neue Verfahren entwickelt worden, die auch Patienten mit einem zur Amputation anstehenden Befund noch Optionen bieten können. Hierbei scheint insbesondere das Prinzip der venösen Arterialisation sehr vielversprechend zu sein (13). Dieses aufwändige und nur in wenigen deutschen Zentren durchgeführte Verfahren verwendet eine tiefe Leitvene im Unterschenkel als zuführendes arterielles Gefäß, indem eine offene Unterschenkelarterie durch eine endovaskuläre Technikprozedur mit der begleitenden Vene (Vena tibialis posterior oder Vena tibialis anterior) verbunden wird. Die arterialisierte Vene übernimmt im Weiteren den Einstrom in den Fuß (Abb. 3).
Erschienen in: Der Nierenarzt, 2020; 7 (1) Seite 8-15