Die primäre Therapie der kritischen Extremitätenischämie bei pAVK ist die endovaskuläre Revaskularisierung. Man muss allerdings wissen, dass dieses Verfahren immer nur symptomorientiert ist und weder die Morphologie arteriosklerotisch vorgeschädigter Gefäße ändert noch den arteriosklerotischen Progress verhindert. Es kann aber aufgrund des Mobilitätsgewinns zu einer langfristigen Prophylaxe führen. Zudem kann ein frühzeitiges Erkennen der Arteriosklerose, die Optimierung der Risikofaktoren und die stadiengerechte Revaskularisierung schwere Ereignisse wie Myokardinfarkt, Schlaganfall oder Beinverlust verhindern.
Die periphere arterielle Verschlusskrankheit (pAVK) als wichtige Manifestation der systemischen Atherosklerose stellt mit weltweit über 200 Millionen Patienten [1] und einer altersspezifisch zunehmenden Prävalenz von ca. 18 % in deutschen Haus- und Facharztpraxen [2] eine bedeutende Erkrankung für das globale Gesundheitssystem dar. Im Jahr 2013 wurden 232.000 invasive Behandlungen der pAVK in Deutschland abgerechnet [3]. Es besteht eine signifikante Assoziation zwischen der pAVK und anderen arteriosklerotischen Erkrankungen, wie etwa dem abdominellen Aortenaneurysma (AAA) [4] oder der extrakraniellen Karotisstenose [5]. Eine Einteilung der pAVK kann nach klinischen oder morphologisch-anatomischen Aspekten erfolgen, wobei sich in Deutschland die nach dem französischen Chirurgen René Fontaine benannte Klassifikation im Alltag durchgesetzt hat (Abb. 1).
Aufgrund der ungleich schlechteren Prognose kommt der sogenannten kritischen Extremitätenischämie (auch: Critical Limb Ischemia, CLI) eine besondere Bedeutung zu. In diesem Stadium bestehen Ruheschmerzen oder chronische Wunden mit Gewebsverlust. Bei der belastungsabhängigen Claudicatio intermittens (IC, auch: Schaufensterkrankheit) stellt das begleitete Gehtraining und die konsequente Optimierung der Risikofaktoren einen mindestens gleichwertigen Therapieansatz im Vergleich zu den invasiven Verfahren dar und wird daher auch in gültigen Leitlinien empfohlen [6 – 9]. Dennoch zeigen aktuelle Registererhebungen, dass auf die IC etwa 50 % der invasiven Revaskularisationen entfallen, was den Leitlinienempfehlungen zu widersprechen scheint [10, 11]. Der Stellenwert der verschiedenen Verfahren und Devices wird aufgrund der unzureichenden Evidenzbasis kontrovers diskutiert.Unumstritten ist dagegen der Stellenwert der invasiven Therapieverfahren bei der CLI, wo der Beinerhalt und die damit einhergehende vitale Bedrohung der Patienten im Vordergrund steht. Die Gesamtletalität von Patienten mit CLI beträgt 3,7 % nach 30 Tagen, 17,5 % nach einem Jahr und bereits 46,2 % nach fünf Jahren [12].
Diabetisches Fußsyndrom
Eine besondere Herausforderung stellt hierbei das diabetische Fußsyndrom (DFS) mit dem Symptomkomplex aus Gewebeverlust, Infektion und Neuropathien dar. Hierbei kann die Polyneuropathie die Schmerzsymptomatik verschleiern und eine Mediasklerose der peripheren Arterien kann zu falsch hohen Messwerten in der Diagnostik führen. Sobald atherosklerotische Veränderungen mit einer hämodynamisch relevanten pAVK hinzukommen, wird die Wundbehandlung limitiert und die Prognose signifikant verschlechtert. Man sollte dann wegen der Bedrohung von einer kritischen Extremitätenischämie sprechen.
Manifestationen der Atherosklerose
Neben der pAVK sind die koronare Herzkrankheit (KHK), die Karotisstenose und das abdominelle Aortenaneurysma (AAA) Manifestationen der systemischen Atherosklerose. Zu den wesentlichen Veränderungen in den betroffenen Gefäßen gehören Verengungen oder Verschlüsse mit der Ausbildung von Kollateralkreisläufen und turbulenten Strömungen. Kommt es durch die vorgenannten Veränderungen zu einer Abnahme des distalen Blutflusses, spricht man von einer kritischen Arterienstenose. Wichtige Risikofaktoren sind das Rauchen, Diabetes, hohes Alter, Hypertonie, männliches Geschlecht sowie Dyslipidämien.
Symptome und Diagnostik
Die Symptome und Ausprägungen der pAVK sind vielfältig und richten sich maßgeblich nach dem Krankheitsstadium. Abhängig von der Lokalisation der Verengung und einer möglichen Kollateralisierung treten die belastungsabhängigen Beschwerden dabei im versorgten Stromgebiet auf. Typischerweise klagen Patienten mit Läsionen der Oberschenkeletage (A. femoralis superficialis) über eine Wadenclaudicatio. Ist die distale Aorta oder die Aortenbifurkation betroffen, kommt es zu glutealen oder Oberschenkelschmerzen. Das Auftreten von Ruheschmerzen ohne jede Belastung kennzeichnet die kritische Extremitätenischämie, wobei eine diabetische Neuropathie zu einem stummen Verlauf führen kann. Oft findet sich bei der kritischen Extremitätenischämie auch eine blasse oder livide Extremität mit verzögerter oder aufgehobener Rekapillarisierung. Vor allem bei Befall der drei Unterschenkelgefäße kommt es in fortgeschrittenen Stadien nach traumatischen Verletzungen oder spontan zum Untergang von Hautgewebe, zu chronischen Wunden und Wundheilungsstörungen. Eine feuchte Nekrose oder eine Gangrän kann zu einem Befall des Knochens (Osteitis) oder septischem Verlauf führen und bedarf daher einer dringenden Behandlung.
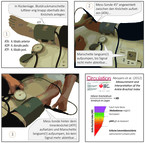
Neben der gewissenhaften Anamnese, vorzugsweise unter Nutzung eines strukturierten Fragebogens [13], und klinischen Untersuchung inklusive Pulsstatus stellt die Dopplerverschlussdruckmessung (Abb. 2) das Fundament der vaskulären Stufendiagnostik dar. Ein Ankle-Brachial-Index (ABI, auch: Knöchel-Arm-Index) unter 0,9 gilt heute als beweisend für das Vorliegen einer pAVK und sollte zu einer kardio-neuro-vaskulären Umfelddiagnostik führen [14]. Deutlich erhöhte ABI-Werte über 1,3 können dagegen auf eine diabetische Mediasklerose hinweisen. Mittels farbkodierter Duplexsonographie (FKDS) kann der geübte Untersucher die Becken-Bein-Strombahn auf Verschlüsse und Flussbeschleunigungen hin untersuchen und so die Stenosegrade abschätzen. Goldstandard der invasiven Diagnostik ist die digitale Subtraktionsangiographie (DSA), bei der jodhaltiges Kontrastmittel oder bedarfsweise CO2 verwendet werden kann. Mittels DSA lassen sich auch kleine Gefäße und Kollateralen bis in die distale Strombahn darstellen und durch die einliegende Schleuse besteht gleichzeitig die Möglichkeit einer interventionellen Revaskularisation.
Therapie der kritischen Extremitätenischämie und des diabetischen Fußsyndroms
Die Therapie der pAVK verfolgt primär eine Minimierung der Risikofaktoren, da die Prognose dieser Patientengruppe maßgeblich durch den natürlichen Verlauf der kardio-neuro-vaskulären Komorbiditäten (Myokardinfarkt, Schlaganfall, Herzinsuffizienz) bestimmt ist. Alle Patienten sollten daher einem begleiteten Gehtraining zugeführt werden. Darüber hinaus ist eine strikte Nikotinkarenz, Blutdruckeinstellung, die Gabe von Thrombozytenaggregationshemmern und Statinen sowie die Behandlung einer KHK, Herz- oder Niereninsuffizienz von lebenswichtiger Bedeutung (Tabelle 1). Patienten mit einem Diabetes mellitus sollten darüber hinaus interdisziplinär durch Gefäßmedizin, Diabetologie und Fußspezialisten betreut werden, wobei die peripher-vaskuläre Erkrankungskomponente primär durch die Gefäßmedizin betreut werden sollte.
Evidenzbasiert überlegen gegenüber dem überwachten Gehtraining ist aktuell nur die invasive Behandlung der kritischen Extremitätenischämie. Primär sollte möglichst der Versuch einer endovaskulären Revaskularisation (ER) erfolgen, solange ein mindestens gleichwertiger Behandlungserfolg zum offen-chirurgischen Vorgehen erwartet werden kann.
Femoro-popliteale Bypässe sollten wenn möglich mit autologer Vene konstruiert werden, Läsionen unterhalb des Knies sollten mittels Ballonangioplastie und ggf. mittels optionalen Stentings ("Bailout") behandelt werden. Der Stellenwert beschichteter Stents und Ballons ist nicht abschließend geklärt. Zur evidenzbasierten Therapieentscheidung bei kritischer Extremitätenischämie und diabetischem Fußsyndrom kann ein neu entwickeltes Risikoklassifikationssystem (WIfI = Wound, Ischemia and Foot Infection) hilfreich sein (Abb. 3).
Postoperative Nachbetreuung
Alle Patienten mit einer pAVK sollten mit Thrombozytenaggregationshemmern (ASS und/oder Clopidogrel) periinterventionell bzw. perioperativ behandelt werden. Vorteile für eine orale Antikoagulation konnten in der Beurteilung aller Studien zur Rezidivprophylaxe nach Bypassoperationen nicht nachgewiesen werden, während nach kardialer und arterieller Embolie und nach Lysebehandlungen arterieller appositionsthrombotischer Verschlüsse eine solche empfohlen wird. Kombinationsbehandlungen mit vorübergehender dualer Thrombozytenaggregationshemmung sind nach infrainguinaler endovaskulärer Therapie mit Stent, DEB oder PTA zu empfehlen. Falls ein infrapoplitealer Prothesenbypass angelegt werden muss, kann eine duale Plättchenhemmung mit ASS und Clopidogrel indiziert sein (CASPAR-Studie). Ebenso kann eine Kombinationsbehandlung aus ASS und oraler Antikoagulation bei einem hohen Risiko für einen Bypassverschluss verordnet werden.
Ein strukturiertes gefäßmedizinisches Nachsorgeprogramm umfasst die regelmäßige Patientenbetreuung mit konsequenter Behandlung von kardiovaskulären Risikofaktoren und Erfassung weiterer Behandlungsoptionen. Eine Duplexsonografie sollte in Intervallen zwischen drei und sechs Monaten stattfinden. Ein überwachtes Gehtraining bzw. der Einschluss in Gefäßsportgruppen gehört nach Gefäßeingriffen zur Basisbehandlung.
Interessenkonflikte: Der Autor hat keine deklariert.
Erschienen in: Der Allgemeinarzt, 2017; 39 (9) Seite 42-47