Das Update der ESC-/EACTS-Richtlinien zur Myokardrevaskularisation hat die Europäische Gesellschaft für Kardiologie (ESC) und die Europäische Gesellschaft für Herzchirurgie (EACTS) 2018 auf Basis der Richtlinien aus den Jahren 2010 und 2014 veröffentlicht. Eine gemeinsame Expertengruppe nahm unter Berücksichtigung aktueller Forschungsergebnisse eine kritische Einschätzung der diagnostischen und therapeutischen Verfahren vor – einschließlich der Bewertung des Nutzen-Risiko-Verhältnisses. Dabei ging es um die entscheidende Frage: Was verbessert die Prognose der koronaren Herzkrankheit im Langzeitverlauf? Erstmals ist jetzt eine komplette Revaskularisation des Herzmuskels empfohlen.
Die Stärke der Empfehlung richtet sich in den neuen Leitlinien weiterhin nach den Behandlungsmöglichkeiten und wird nach vordefinierten Skalen sortiert (Tabelle 1). Für die Myokardrevaskularisation gibt es zwei hocheffiziente Therapien: die perkutane Koronarintervention (PCI) und die chirurgische Revaskularisation (CABG – Bypass). Die voraussichtliche Op.-Letalität, die anatomische Komplexität der koronaren Herzerkrankung (KHK) und die zu erwartende Vollständigkeit der Revaskularisation sind hier wichtige Kriterien für eine interventionelle oder chirurgische Therapie.
Op.-Risiko und KHK-Komplexität
Für die Beurteilung des chirurgischen Risikos mit 30 Tagen Letalität und Morbidität wird primär der STS-Score empfohlen, während man den Euro-Score II jetzt von IIa B auf IIb B abgewertet hat (dieser wird nicht regelmäßig neu kalibriert). Obwohl diese Scores nützlich sind, gibt es kein Risiko-Modell mit perfekter Risikobewertung. Die Entscheidung darf deshalb nicht allein von Scores abhängen – diese sollten vielmehr als Leitfäden für Heart-Teams dienen.
Bei Ein- oder Zweigefäßerkrankungen ist mit Ausnahme der komplexen proximalen LAD-Stenose die PCI die Therapie der Wahl. Bei Hauptstammstenose oder Mehrgefäß-Koronarer Herzerkrankung wird der rein angiographische SYNTAX-Score zur Beschreibung des Schweregrads beziehungsweise der Komplexität einer KHK empfohlen [1].
Der SYNTAX-Score I berücksichtigt lediglich die Koronaranatomie. Für den SYNTAX-Score II werden zusätzlich Alter, Geschlecht, LVEF, Kreatinin-Clearance und weitere Parameter (pAVK, COPD) abgefragt. Werte von 0 – 23 beschreiben leichte Stenosen, 23 – 32 mittelschwere und Werte über 33 schwere Stenosen.
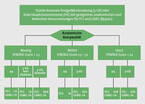
Zur Behandlung der Hauptstammstenose und der Dreigefäßerkrankung mit niedrigem SYNTAX-Score ohne Diabetes mellitus stehen die PCI und die chirurgische Revaskularisation gleichberechtigt nebeneinander (Abb. 1).
Beide Therapieoptionen haben deshalb eine IA-Empfehlung. Bei Hauptstammstenose mit hohem SYNTAX-Score und Dreigefäßerkrankung mit intermediärem oder hohem SYNTAX-Score führt die chirurgische Revaskularisation unabhängig vom Diabetes zu einer signifikant niedrigeren Letalität im Vergleich zur PCI. Die chirurgische Revaskularisation bekommt deshalb eine IA-Empfehlung, während die perkutane Koronarintervention als Alternative zur Bypass-Operation nur eine Klasse-III-Empfehlung erhält. Bessere Ergebnisse durch die chirurgische Revaskularisation gibt es nach neueren Erkenntnissen auch für die Dreigefäßerkrankung mit niedrigem SYNTAX-Score und Diabetes [2].
Deshalb wurde hier die PCI von einer IIa- auf IIb-Empfehlung herabgestuft (Abb. 1).
Die Empfehlungen zur Myokardrevaskularisation bei chronischer Herzinsuffizienz und systolischer linksventrikulärer Dysfunktion (EF < 35 %) hat man ebenfalls geändert. Sofern es technisch möglich ist, wird nun generell eine Myokardrevaskularisation empfohlen (IB). Die chirurgische Revaskularisation (laut STICHES) gilt hier als Therapie der ersten Wahl (IB) [3].
Es gilt: Bei geringer Komplexität der KHK ist der Unterschied zwischen perkutaner Koronarintervention und chirurgischer Revaskularisation vernachlässigbar. Bei hoher Komplexität, vor allem bei schlechter linksventrikulärer Funktion (EF < 35 %) und in Kombination mit Diabetes, hat die chirurgische Revaskularisation einen wesentlichen Vorteil.
Vollständige Revaskularisation
Erstmals betonen die Leitlinien, dass bei der Myokardrevaskularisation das Verfahren priorisiert werden sollte, das eine vollständige Revaskularisierung liefert [4]. Das Ziel der Revaskularisation des Herzmuskels ist, die verbleibende Ischämie zu minimieren. Dieses Konzept unterstützt die COURAGE-Studie, die eine zusätzliche Risikosenkung von Tod und Myokardinfarkt zeigt, wenn die stressinduzierte Ischämie von
> 10 % des Myokards bis < 5 % reduziert wird. In der SYNTAX-Studie ist die anatomisch vollständige Revaskularisation definiert als PCI oder Bypass aller epikardialen Gefäße mit einem Durchmesser > 1,5 mm und einer Lumenreduzierung von > 50 % in mindestens einer angiographischen Ansicht. Der Nutzen einer vollständigen Revaskularisation war dabei unabhängig von der Behandlungsmodalität [5].Laut neuer Leitlinie reicht die angiographische Beurteilung – außer bei höchstgradigen (> 90 %) Stenosen eines großen Koronargefäßes – nicht aus. Es muss die funktionelle Relevanz anhand bildgebender, nicht-invasiver Funktionstests oder intrakoronarer Druckmessungen nachgewiesen sein. Als Schwelle gilt eine FFR von weniger als 0,80 oder eine iwFR von weniger als 0,89 [6]. Ein großes Ischämieareal ist weiter als > 10 % der linksventrikulären Masse definiert. Als neues Kriterium für eine prognostisch relevante Läsion wurde eine hochabnorme FFR von weniger als 0,75 eingeführt.
Technische Aspekte
Bei der Auswahl des Stents wird der Drug-eluting Stent (DES) der neuen Generation dem Bare-metal-Stent (BMS) vorgezogen. Mit dem DES konnte die Re-Stenose-Rate um 50 – 70 % gegenüber dem BMS reduziert werden, wobei die erste Generation der DES ein erhöhtes Risiko einer späten Stentthrombose zeigt. Durch die DES der neuen Generation (u. a. ausschließlich aus Sirolimus-analogen Medikamenten) ließ sich das Spätthrombose-Risiko gegenüber der Erstgeneration senken [7]. Aufgrund eines geringeren Blutungsrisikos sollte der Standardzugang bei jeder perkutanen Koronarintervention der radiale Zugang sein. Bei der chirurgischen Revaskularisation sollte man bei hochgradigen Stenosen neben der LIMA als zweites Gefäß primär die Radialarterie vor der Vene verwenden, da diese im Langzeitverlauf bessere Offenheitsraten zeigt. Nutzt man hier die Vene, sollte sie in "No-Touch"-Technik entnommen werden, da diese Technik im Vergleich zu anderen in mehreren randomisierten Studien überlegene Offenheitsraten gezeigt hat.
Medikamentöse Therapie
Die antithrombotische Therapie nach Myokardrevaskularisation bleibt obligat. Das Medikament und die Kombination, der Zeitpunkt der Einleitung und die Dauer sind abhängig von Begleiterkrankungen, klinischer Situation (elektive versus dringliche Revaskularisation bei akutem Koronarsyndrom) und Art der Revaskularisation (PCI versus chirurgische Revaskularisation). Sowohl ischämische als auch Blutungsereignisse beeinflussen signifikant das Ergebnis. Die Wahl der Medikation sollte deshalb beide Risiken – das Risiko für Ischämie und Blutungen – widerspiegeln. Eine neue Empfehlung der Leitlinie ist, nicht-Vitamin-K-abhängige orale Antikoagulanzien (NOAK) gegenüber den Vitamin-K-Antagonisten (VKA) bei nicht-valvulärem Vorhofflimmern und Indikation zu Antikoagulation und antithrombozytärer Therapie vorzuziehen (IIa A).
Die Strategien fürs Follow-up sind seit 2014 deutlich anders. Allen Patienten nach chirurgischer Revaskularisation und PCI bei akutem Myokardinfarkt wird zur Rehamaßnahme geraten. Sekundäre Präventionsmaßnahmen, inklusive Medikation und Lebensstiländerung, sollte der Patient unabhängig von Symptomen beginnen. Auch ist eine engmaschigere Nachkontrolle mit einer Re-
evaluation drei Monate nach Revaskularisation und dann in jährlichem Abstand zur Neubewertung der Symptome empfohlen – neben der Anpassung der medikamentösen Therapie und der Einhaltung der Sekundärprävention.
Interessenkonflikte: Die Autorin hat keine deklariert.
Erschienen in: Der Allgemeinarzt, 2020; 42 (18) Seite 30-32