Viele Patienten, die Antibiotika einnehmen, klagen über Übelkeit und Durchfall. Eine antibiotikaassoziierte Diarrhö (AaD) ist in den meisten Fällen harmlos und muss nicht behandelt werden. Sie ist jedoch immer von einer Clostridioides-difficile-Infektion (CDI) abzugrenzen. Diese Infektion, die auch lebensbedrohlich verlaufen kann, tritt heute immer häufiger auf. Besonders betroffen sind ältere, multimorbide Patienten, aber auch immer mehr jüngere Menschen.
Eine Antibiotikatherapie ist häufig mit gastrointestinalen Nebenwirkungen wie Übelkeit und Diarrhö assoziiert [1]. Während die antibiotikaassoziierte Diarrhö (AaD) in der Regel unkompliziert verläuft und keiner Therapie bedarf [2], kann eine Clostridioides-difficile-Infektion (CDI) mit schweren Verläufen bis hin zum Tod einhergehen [3]. Bei Durchfällen im Rahmen einer Antibiotikatherapie sollte man daher sowohl im stationären als auch im ambulanten Bereich an eine CDI denken und gegebenenfalls eine entsprechende Diagnostik einleiten.
Bei einer AaD kommt es in Verbindung mit einer Antibiotikatherapie zu mehr als drei ungeformten beziehungsweise wässrigen Stühlen, für die es keine andere Erklärung gibt [4, 5]. Der Durchfall kann dabei gleichzeitig mit der Antibiotikaeinnahme, unmittelbar nach Abschluss der Antibiose, aber auch erst mehrere Wochen danach auftreten [4].
Eine 32-jährige Patientin wurde wegen einer Sinusitis über fünf Tage mit Cefuroxim behandelt. Ab dem zweiten Tag der Antibiose bekam sie weichen Stuhlgang, der zunehmend dünnflüssiger wurde. Am vierten Tag stellte sie sich beim Hausarzt vor. Die Diagnose: AaD. Entgegen der Erwartung, dass die Diarrhö bei Therapieende sistiert, blieb der Durchfall auch nach Beendigung der Antibiotikatherapie bestehen, nahm sogar an Intensität zu.
BefundeAm Tag 7 erfolgte eine erneute Vorstellung beim Arzt. Die Patientin hat eine wässrige Diarrhö (10 x/d) mit periumbilikalen Druckschmerzen und Krämpfen und einem Gewichtsverlust von 2 – 3 kg. Die Körpertemperatur ist subfebril (38 °C).
Labor und Diagnose
Hb 11,8 mg/dl; Leukozyten 13.000/m³ (n < 11.000);
CRP 20 mg/l (n < 5);
Kreatinin 1,3 mg/dl (n < 1,1)
Die Abdomensonografie zeigte flüssigkeitsgefüllte Darmschlingen und eine Pendelperistaltik. Eine Stuhluntersuchung auf C.-difficile-Toxin A+B verlief positiv. Diagnose: CDI.
Je nach Antibiotikum und abhängig von einer stationären oder ambulanten Therapie sind bis zu ein Viertel aller antibiotisch behandelten Patienten von einer AaD betroffen [2, 4]. Ältere Menschen leiden häufiger darunter, ansonsten gibt es aber kaum Kriterien, mit denen sich vorhersagen ließe, welcher Patient auf welches Antibiotikum eine AaD entwickelt [4].
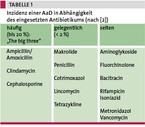
Prinzipiell kann eine AaD unter jedem Antibiotikum auftreten, häufiger ist sie unter Breitbandantibiotika – vor allem unter Amoxicillin-Clavulansäure (10 – 25 %), Ampicillin (5 – 10 %) sowie unter Clindamycin, Cephalosporinen, Chinolonen und Makroliden (vgl. Tabelle 1) [1, 2, 5].
Multifaktorielle Pathogenese
Als wichtigste Ursache einer AaD gilt die Störung der gastrointestinalen Mikrobiota. Auf direktem oder indirektem Weg werden Diversität und Anzahl der im Darm angesiedelten Bakterien verändert. Dies kann die Widerstandsfähigkeit gegenüber pathogenen Keimen beeinträchtigen und/oder zu einer übermäßigen Vermehrung beziehungsweise zur Selektion einzelner pathogener Spezies führen [1, 2]. Auch kann der Rückgang einzelner Bakterienarten den Kohlenhydrat- und Gallensäurestoffwechsel beeinflussen und daraus eine funktionelle Diarrhö resultieren [2]. Antibiotika können zudem direkte pharmakologische beziehungsweise toxische oder allergische Effekte auf Darmflora und -motilität sowie die Funktion der Darmschleimhaut haben [2, 4, 5].
Prophylaxe der AaD: Hygienemaßnahmen und Probiotika
Am besten lässt sich eine AaD durch den restriktiven Einsatz einer antibiotischen Therapie vermeiden. Dies wurde u. a. für Clindamycin und Cephalosporine nachgewiesen [2]. Auch einfache Hygienemaßnahmen, wie die Händedesinfektion, können das Auftreten einer AaD reduzieren [2]. Ist bei bereits davon betroffenen Patienten eine erneute Antibiotikatherapie nötig, lassen sich Probiotika wie Saccharomyces boulardii oder Lactobacillus GG zur Prävention einsetzen [2].
Man geht davon aus, dass Probiotika zum Erhalt einer ausgeglichenen Mikrobiota beitragen und Gesundheit sowie Leistungsfähigkeit des Magen-Darm-Trakts und des Immunsystems unterstützen [1].
Allerdings ist hier die Evidenz nicht besonders hoch [6]. Einem aktuellen Review zufolge scheint der Effekt von Probiotika jedoch vom Stamm abzuhängen. Nur für Saccharomyces boulardii und Lactobacillus GG liegt jeweils mehr als eine randomisierte kontrollierte Studie vor, die eine reduzierte AaD-Rate zeigt [6]. Eine Cochrane-Analyse zu Probiotika als AaD-Prophylaxe bei Kindern weist ebenfalls auf eine schlechte Studienlage hin: Bisher gibt es nur Hinweise darauf, dass hochdosierte Probiotika die Inzidenz und die Dauer der AaD bei Kindern reduzieren können [7]. Vorteil der Probiotika ist ihre gute Verträglichkeit [6, 7].
AaD meist selbstlimitierend, aber langfristige Konsequenzen möglich
Wichtigster Aspekt bei Diagnose und Behandlung der AaD ist die Abgrenzung von einer Clostridioides-difficile-Infektion (siehe unten), die etwa 2 – 4 % der AaD-Fälle ausmacht [5]. Nach dem Absetzen oder dem Austausch des Antibiotikums ist die antibiotikaassoziierte Diarrhö bei immunkompetenten Patienten meist selbstlimitierend [4], eine medikamentöse Therapie ist in der Regel nicht nötig [2]. So heilen unkomplizierte, antibiotikaassoziierte Diarrhöen ohne Nachweis einer floriden Kolitis in der Regel innerhalb weniger Tage nach Absetzen des Antibiotikums aus. Der Arzt sollte auch auf ausreichende orale Flüssigkeitsgabe und gegebenenfalls eine Elektrolytsubstitution achten [2].
Nach dem Persistieren des Durchfalls und einer Erholung der Gesamtzahl der Bakterien können allerdings anhaltende negative Effekte auf die Balance des Mikrobioms im Darm bestehen bleiben. Dies kann mit einer gesteigerten Empfänglichkeit für Infektionen und andere Erkrankungen einhergehen [1]. Insgesamt kann eine AaD deshalb mit einer erhöhten Komplikationsrate, verlängerten stationären Aufenthalten und entsprechend gesteigerten Kosten für das Gesundheitswesen verbunden sein [1, 4, 5].
Problemkeim Clostridioides difficile
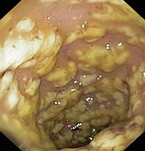
Mit einer AaD assoziierte Keime sind u. a. Clostridioides (C.) difficile, Staphylococcus aureus, Klebsiella oxytoca, Clostridium perfringens und Candida albicans [4]. C. difficile ist für 15 – 20 % aller AaD-Fälle sowie für etwa 95 % der antibiotikaassoziierten pseudomembranösen Kolitis verantwortlich (Abb. 1) [3]. Clostridioides (früher Clostridium) difficile [8] kann durch Toxine Darmentzündungen hervorrufen. Eine Infektion mit dieser Bakterienart ist bei schwerem Verlauf eine meldepflichtige Erkrankung [9].
Viele Risikofaktoren begünstigen CDI
Typische Risikofaktoren für eine CDI sind neben Antibiotika (vor allem Breitbandantibiotika) ein Lebensalter über 65 Jahre. So waren 2018 fast drei Viertel der CDI-Patienten 70 und älter [9].
Als weitere Risiken gelten eine eingeschränkte Immunkompetenz (z. B. durch maligne Erkrankungen oder Immunsuppressiva), Komorbiditäten wie chronische Nieren- oder chronisch-entzündliche Darmerkrankungen, längere Krankenhausaufenthalte sowie die häusliche Pflege. Auch Protonenpumpenhemmstoffe (PPI) begünstigen eine CDI [3, 4, 8, 9]. Risiken für einen schweren Verlauf sind der S2k-Leitlinie für gastrointestinale Infektionen zufolge u. a. ein Alter über 65 Jahre, Fieber sowie relevante Komorbiditäten (Tabelle 2) [10].
Immer mehr ambulante CDI-Fälle
In den letzten zehn Jahren haben Häufigkeit und Schwere der CDI weltweit zugenommen. Sie gehört heute zu den häufigsten nosokomialen Erkrankungen [3, 8, 11]. Ein möglicher Grund für die steigende CDI-Inzidenz könnte – neben der wachsenden Zahl an Patienten mit Risikofaktoren – das Auftreten neuer hypervirulenter Ribotypen von C. difficile sein, darunter Ribotyp 027 [4, 11, 12]. Eine starke Zunahme zeigte sich auch bei ambulant erworbenen CDI-Fällen, die aktuell über 40 % ausmachen [8, 13].
Die ambulant erworbene CDI betrifft dabei auch Personen, die zuvor nicht als Risikogruppe galten, etwa jüngere Patienten (vgl. Fall) und Menschen ohne Antibiotikaexposition in den zwölf Wochen vor der CDI [14].
Eine Übertragung von C. difficile ist vor allem durch direkten Patientenkontakt, etwa über kontaminierte Hände des Klinikpersonals, und die Umwelt möglich [9]. Die Sporen sind gegen Hitze, Säure und Antibiotika resistent, können auf Oberflächen (z. B. Toilette, Telefon, Thermometer und Stethoskop) überleben [8]. Hygienemaßnahmen sowie die Isolation dieser Patienten sind daher die wichtigste Prävention.
Das klinische Bild einer CDI ist sehr variabel – vom asymptomatischen Trägerstatus über verschieden stark ausgeprägte Diarrhöen bis zu lebensbedrohlichen Verläufen (z. B. pseudomembranöse Kolitis, toxisches Megakolon) [8, 9]. Typische Symptome einer CDI sind u. a. akute breiige bis wässrige, teils blutige Durchfälle mit charakteristisch fauligem Geruch, krampfartige Schmerzen im unteren Quadranten des Abdomens, Fieber und Leukozytose [3].
Herausfordernd sind fulminante Verlaufsformen (selten), häufige Rezidive und hohe Therapiekosten [4, 14].
Diagnosesicherung
Um eine gezielte Behandlung einzuleiten und eine nosokomiale Übertragung zu verhindern, ist eine rasche und genaue Diagnosestellung essenziell [14]. So sollte der Arzt bei mindestens drei ungeformten Stühlen in 24 Stunden und unter Antibiotikatherapie bei stationären und ambulanten Patienten an eine CDI denken. Deren Diagnose basiert auf dem Nachweis der C.-difficile-Toxine A und B mittels diverser Kontrollen wie dem Zytotoxizitätstest (Goldstandard) und dem Nachweis des Glutamat-Dehydrogenase (GDH)-Enzyms [3]. In den meisten Labors wird nach dem GDH-Test im positiven Fall eine PCR-Diagnostik angeschlossen, die den Toxin-Nachweis sichert [8, 15]. Auch sogenannte "Pseudomembranen" auf der Kolonschleimhaut sichern die Diagnose. Wird eine CDI diagnostiziert, gilt es primär, das verursachende Antibiotikum möglichst abzusetzen [16].
Initiale Therapie: die aktuellsten Empfehlungen
Die aktuellsten Empfehlungen zur Therapie der CDI finden sich im Update 2018 der Leitlinien der Infectious Diseases Society of America (IDSA) und der Society for Healthcare Epidemiology (SHEA) [16]. Die früheren Fassungen empfahlen Metronidazol oder Vancomycin zur Therapie der ersten CDI-Episode mit milder bis moderater Ausprägung. Aktuelle Studien zeigen jedoch, dass die Ansprechraten unter Metronidazol geringer sind als unter Vancomycin. Daher wird jetzt zu oralem Vancomycin oder Fidaxomicin für die initiale CDI-Episode geraten – unabhängig vom Schweregrad (Tabelle 3) [16].
Herausforderung Rezidive
Nach einer effektiven Behandlung der ersten CDI-Episode kommt es bei etwa 10 bis 25 % zu einem Rezidiv. Von den Patienten, die schon mindestens eines erfahren haben, erleiden bis zu 65 % ein erneutes Rezidiv [8]. Ein erhöhtes Risiko haben Personen, bei denen man eine nicht gegen C. difficile gerichtete Antibiose fortführt, ältere Menschen über 65, Patienten mit schweren Grunderkrankungen und/oder Nierenversagen, einer schweren initialen CDI und Patienten unter PPI [15].
Beim ersten Rezidiv sehen die Leitlinien die Gabe von Vancomycin (125 mg 4 x/d über zehn Tage) bei Patienten vor, die initial mit Metronidazol vorbehandelt waren, ansonsten empfiehlt sich Fidaxomicin für zehn Tage. Ein gepulstes Reduktionsschema mit Vancomycin scheint die Rezidivrate ebenfalls zu verringern [16]. Fidaxomicin und das gepulste Reduktionsschema mit Vancomycin setzt man auch bei weiteren Rezidiven ein.
Nach mehrfachen Rezidiven ist zudem ein fäkaler Mikrobiomtransfer (FMT) möglich. Die Behandlung mit FMT sollte erfahrenen Zentren vorbehalten bleiben, die sowohl die nötige Spenderdiagnostik vornehmen als auch die Ergebnisse in die Register eingeben, die unsere Erfahrungen mit dem FMT verbessern [16].
Interessenkonflikte: Der Autor hat keine deklariert
Erschienen in: Der Allgemeinarzt, 2020; 42 (11) Seite 41-44