In der Ernährungsmedizin dreht sich derzeit vieles ums Vitamin D. Aus gutem Grund: Denn in vielen Industrienationen ist Vitamin-D-Mangel weit verbreitet, insbesondere in den Wintermonaten. Das "Sonnenvitamin" ist nicht nur essenziell für die Knochengesundheit, sondern beugt vermutlich auch kardiovaskulären Erkrankungen, Diabetes und Hypertonie vor. Dokumentiert ist ein Zusammenhang zwischen dem 25-Hydroxy-Vitamin-D-Serumspiegel [25(OH)D] und der Mortalität. Empfohlen werden ausreichend hohe 25(OH)D-Spiegel insbesondere bei älteren Männern und Frauen zur Prävention von Stürzen, Frakturen und vorzeitigem Tod. Dazu ist bei vielen Patienten eine Supplementation von Vitamin D erforderlich. Kombinationspräparate mit synergistisch wirkenden Kofaktoren wie Magnesium können die Wirksamkeit einer Supplementationstherapie optimieren.
Vitamin D (Calciferol) ist ein fettlösliches Vitamin, das eigentlich gar kein echtes Vitamin ist, weil es nicht mit der Nahrung zugeführt werden muss. Vitamin D3 (Cholecalciferol) wird in der Haut unter Exposition von UV-B-Strahlung (280 – 320 nm) aus tierischem 7-Dehydrocholesterol (Provitamin D3) synthetisiert [1, 2]. Daneben, aber in der Regel in deutlich geringerem Maße, wird Vitamin D3 auch mit der Nahrung zugeführt, ist zum Beispiel in fettem Seefisch (Hering, Lachs, Sardinen), in Leber und Eigelb enthalten (vgl. Tabelle 1) [3]. Vitamin D2 (Ergocalciferol) wird nur in Form von pflanzlichen Lebensmitteln aufgenommen, ist zum Beispiel in einigen Pilzen enthalten, die es aus Ergosterol (Provitamin D2) synthetisieren [4].
Die Ernährung spielt aber bei den meisten Menschen für die Vitamin-D-Zufuhr nur eine untergeordnete Rolle. Selbst Fischliebhaber müssten für eine Deckung des Tagesbedarfs ausschließlich über die Ernährung täglich mindestens 200 g fetten Fisch verspeisen. Unter unseren Lebensbedingungen bei regelmäßigem Aufenthalt im Freien stammen schätzungsweise 80 bis 90 % des Vitamin D im Körper aus der endogenen Synthese in der Haut, etwa 10 bis 20 % des Vitamin D werden mit der Nahrung aufgenommen [1]. Allerdings: Je geringer die endogene Syntheseleistung ist, desto bedeutsamer wird die alimentäre Zufuhr.
Bei Annahme einer fehlenden endogenen Vitamin-D-Synthese (z. B. bei Menschen, die sich so gut wie nie im Freien aufhalten oder den Körper unter freiem Himmel vollständig bedecken) ist laut Schätzung der Deutschen Gesellschaft für Ernährung (DGE) zur Deckung des Tagesbedarfs für Kinder, Jugendliche und Erwachsene eine tägliche Zufuhr von 20 µg (800 IE) Vitamin D erforderlich. Für Säuglinge werden 10 μg (400 IE) pro Tag empfohlen (vgl. Tabelle 2) [5].
Durch eine normale Ernährung ist dieser Bedarf kaum zu decken. Nach Daten der Nationalen Verzehrsstudie II erreichen 80 % der Männer und 90 % der Frauen eine entsprechende Zufuhr von Vitamin D über die Nahrung nicht, bei Personen über 65 Jahre lag der Anteil sogar bei 94 bzw. 97 %. Im Median kamen Männer im Alter von 14 bis 80 Jahren auf nur 2,9 µg und gleichaltrige Frauen auf 2,2 µg pro Tag [6].
Sonne allein reicht nicht
Bei häufigen Aufenthalten im Freien und ausreichender Sonnenexposition kann eine ausreichende Versorgung auch ohne Vitamin-D-Supplementation erreicht werden. Die Syntheseleistung hängt außer vom Hauttyp (geringer bei dunklerem Hauttyp) vor allem von Kleidung, Sonneneinstrahlung und geografischen Faktoren (Länge, Breite, Höhe) ab. Die Exposition des Körpers in Badekleidung mit einer minimalen Erythemdosis (MED), jener UV-Dosis, die eine gerade sichtbare Hautrötung hervorruft, entspricht nach Schätzungen in etwa der oralen Einnahme von 10.000 bis 25.000 IE (250 bis 635 μg) Vitamin D [1]. Eine Exposition von Händen, Armen und Gesicht (weniger als 18 % der Körperoberfläche), zwei- bis dreimal pro Woche mit einer Dosis von bis zu einem Drittel oder der Hälfte der MED, reicht nach Ansicht einiger Autoren im Frühjahr, Sommer und Herbst aus, um eine suffiziente Vitamin-D-Versorgung zu gewährleisten [7]. Aber: In Deutschland wird ca. 6 Monate im Jahr ein UV-Index von 3 (mittlere Bestrahlungsstärke) unterschritten, so dass eine ausreichende Vitamin-D3-Synthese nicht mehr gewährleistet ist [8]. Zudem setzen sich viele Menschen wegen der karzinogenen Wirkung von UV-Licht bewusst immer seltener Sonnenstrahlung aus und wenn, dann nur unter Verwendung von Sonnenschutzmitteln mit hohem Lichtschutzfaktor. Was in puncto Hautkrebsprävention unbedingt zu empfehlen ist, wird somit zur Hürde einer ausreichenden Versorgung mit Vitamin D.
In Großteilen unserer Bevölkerung besteht deshalb eine erhebliche Unterversorgung mit Vitamin D, insbesondere bei Senioren und insbesondere in den Wintermonaten.
Wo beginnt der Vitamin-D-Mangel?
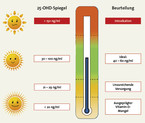
Als geeignete Messgröße für die gesamte Vitamin-D-Versorgung (endogen und exogen) hat sich der 25(OH)D-Serumwert etabliert [9]. Als Grenzen für eine unzureichende Vitamin-D-Versorgung gelten in der Regel 25(OH)D-Serumwerte < 30 ng/ml (75 nmol/l) und für einen Mangel Werte < 20 ng/ml (50 nmol/l) [3, 9]. Etwas zurückhaltender bewertet die DGE den Bedarf und spricht erst bei 25(OH)D-Serumwerten < 10 ng/ml (< 25 nmol/l) von einem echten Mangel [7].
Werte zwischen 40 und 60 ng/ml gelten als ideal, die Obergrenze liegt bei 100 ng/ml. Der toxische Bereich, der nur durch langfristige Überdosierung einer Vitamin-D-Supplementation erreicht werden kann, liegt > 150 ng/ml [3, 9] (vgl. Abb. 1).
Laut repräsentativen Untersuchungen in Deutschland im Zeitraum 2005 bis 2008 hatten im Jahresdurchschnitt rund 60 % aller Personen im Alter von 65 bis 75 Jahren, im Winterhalbjahr fast 70 %, 25(OH)D-Serumspiegel < 20 ng/ml. Mehr als jeder Fünfte hatte einen schweren Mangel mit Serumspiegeln ≤ 10 ng/ml [10].
Ältere sind für einen Vitamin-D-Mangel besonders gefährdet, weil die Vitamin-D-Synthese in der Haut mit zunehmendem Alter abnimmt [9]. Zudem halten sich ältere Menschen in der Regel weniger im Freien auf als jüngere. Zur Resorption von Vitamin D aus dem Darm ist das Vorhandensein von Nahrungsfetten erforderlich. Deshalb können chronische Magen-Darm-Erkrankungen, die mit einer Fett-Malabsorption einhergehen wie Zöliakie oder Morbus Crohn, oder auch chirurgische (Teil-)Resektionen des Darms zu einem Vitamin-D-Mangel führen [11].
Auch bei Übergewichtigen ist das Risiko für einen Vitamin-D-Mangel erhöht, da in der Haut synthetisiertes Vitamin D in geringerem Maße als bei Normalgewichtigen in den Kreislauf freigesetzt wird [9].
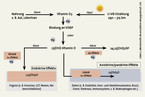
Sowohl in der Haut synthetisiertes Vitamin D3 als auch mit der Nahrung zugeführtes Vitamin D2 und D3 werden in unserem Körper auf die gleiche Art und Weise verstoffwechselt. Inaktives Vitamin D wird über das Blut zur Leber befördert, wo es zunächst in 25-Hydroxyvitamin D [25(OH)D] umgewandelt wird, das Hauptmetabolit von Vitamin D im Blut. Vor allem in der Niere, aber auch in einigen extrarenalen Geweben wird schließlich die aktive Form 1,25-Dihydroxy-Vitamin D gebildet (vor allem 1,25(OH)2D3, Calcitriol). Deshalb kann durch eine stark beeinträchtigte Nierenfunktion ebenfalls ein Vitamin-D-Mangel ausgelöst werden [9].
Last not least: Ein niedriger Magnesium-Status prädestiniert für einen Vitamin-D-Mangel [12]. So sind das Bindungsprotein für Vitamin D im Blut und die drei Enzyme, die für die Umwandlung in 25(OH)D und in aktives 1,25(OH2)D benötigt werden, Magnesium-abhängig [13, 14] (Abb. 2). Zwischen dem Spurenelement und dem Vitamin gibt es zahlreiche Wechselwirkungen. Eine insuffiziente Versorgung mit Vitamin D fördert auch eine Hypomagnesiämie. Auch bei Sarkopenie-Patienten wurde ein Zusammenhang mit dem Vitamin-D- und Magnesium-Status dokumentiert. So wurde in einer Studie an insgesamt 66 älteren Patienten in der Sarkopenie-Gruppe bei der Klinikeinweisung bei 38 % eine verringerte Vitamin-D- und bei 6 % eine verringerte Magnesium-Aufnahme nachgewiesen [15].
Wirkungen von Vitamin D
Vitamin D bzw. die aktive Form 1,25-Dihydroxyvitamin D hat vielfältige positive Wirkungen in unserem Körper: Die Beteiligung an der Regulation des Kalzium- und Phosphathaushalts ist lange bekannt. Vitamin D fördert dadurch die Mineralisierung und Härtung des Knochens [9]. Deshalb sind ausreichend hohe Vitamin-D-Spiegel für die Knochengesundheit und die Vorbeugung einer Rachitis von großer Bedeutung. Neben einer Mineralisationsstörung der Knochen gilt die Myopathie als klassisches klinisches Zeichen einer schweren Vitamin- D-Unterversorgung. Die Vitamin-D-Mangel-Myopathie äußert sich in Muskelschmerzen und Gangstörungen [7]. Unter Vitamin-D-Supplementation ist die Vitamin-D-Mangel-Myopathie innerhalb von Wochen reversibel. Vitamin D schützt darüber hinaus die Nerven und moduliert das Immunsystem.
Kardiovaskulärer Schutz
Zudem gibt es Hinweise für eine vorbeugende Wirkung von Vitamin D, was Krebs, pAVK, Diabetes, Bluthochdruck, Fettstoffwechselstörungen und KHK-Komplikationen angeht [3, 16]. Beobachtungsstudien ergaben inverse Assoziationen zwischen den 25(OH)D-Serumspiegeln und der allgemeinen und kardiovaskulären Sterblichkeit [7]. Assoziationen zwischen niedrigen Vitamin-D-Spiegeln und erhöhter Mortalität wurden vor allem bei Personen mit niedriger Magnesiumzufuhr beobachtet [12, 13]. So war in einer Studie bei gleichzeitigem Vitamin-D- und Magnesiummangel das Mortalitätsrisiko im Vergleich zum alleinigen Vitamin-D-Mangel um 29 % erhöht [13]. In einer Untersuchung an Patienten mit Metabolischem Syndrom war ein optimaler Vitamin-D-Spiegel assoziiert mit einer um 69 % reduzierten kardiovaskulären Mortalität im Vergleich zu einem schweren Vitamin-D-Defizit [25].
Vitamin D und Magnesium
Insbesondere in puncto kardiovaskulärer Gesundheit wirken Vitamin D und Magnesium synergistisch, worauf zunehmend mehr aktuelle Forschungsdaten hinweisen. So kann bei Patienten mit Hypertonie und Herzinsuffizienz ebenso wie bei Patienten mit Metabolischem Syndrom und Diabetes gehäuft ein Magnesium- und ein Vitamin-D-Mangel nachgewiesen werden [17]. In einer Studie bei 11 Patienten mit Hypertonie und Typ-2-Diabetes wurde neben diesen Defiziten auch eine Erhöhung der Interleukin-6-Spiegel belegt. Interleukin-6 ist ein Marker für die systemische Entzündung und ein Risikofaktor von Arteriosklerose und Gefäßschäden [18].
Diese Daten legen nahe, bei kardiovaskulären Risikopatienten und bei Patienten mit metabolischen Störungen sowohl auf den Vitamin-D- als auch den Magnesiumhaushalt zu achten und bei Bedarf das Vitamin gemeinsam mit dem Spurenelement zu substituieren. Empfohlen wird bei Patienten mit Magnesiumdefizit und Vitamin-D-Mangel die Gabe von 300 bis 500 mg Magnesium täglich und von mindestens 1.000 IE Vitamin D. Als Referenzwerte für einen ausreichend hohen Magnesiumstatus gelten Serumwerte ≥ 0,90 mmol/l [17]. Die Gesellschaft für Magnesiumforschung e. V. nennt vier mögliche Mechanismen für die günstigen Wirkungen von Magnesium auf den Kohlenhydratstoffwechsel und die Gefäße:- Insulin-Sensitizing-Effekt,
- Kalzium-Antagonismus,
- Stress-Regulation und
- Endothel-stabilisierender Effekt [19].
Risikogruppen
Die US-amerikanische endokrinologische Gesellschaft empfiehlt in ihrer Leitlinie zum Management eines Vitamin-D-Mangels ein Screening anhand eines verlässlichen 25(OH)D-Assays in Risikogruppen [9]. Dazu zählen zum Beispiel Patienten mit Osteoporose und chronischer Niereninsuffizienz, mit Leberversagen, Hyperparathyreoidismus und mit Malabsorptionssyndromen, außerdem alle schwangeren und erwachsenen Frauen, übergewichtige Kinder und Erwachsene sowie Ältere mit Sturz- bzw. Frakturanamnese (vgl. Tabelle 3). Hingewiesen wird außerdem darauf, dass bestimmte Medikamente einen Vitamin-D-Mangel begünstigen können, zum Beispiel Antiepileptika und Antifungizide wie Ketoconazol, Glukokortikoide, Cholestyramin sowie AIDS-Medikamente.
Zur Prävention vieler chronischer Erkrankungen sowie von Stürzen, Frakturen und vorzeitigem Tod sind bei älteren Männern und Frauen 25(OH)D-Serumspiegel mindestens ≥ 20 ng/ml (≥ 50 nmol/l) wünschenswert [7, 9]. Einige Experten und Teilnehmer eines Konsensus-Meetings in Frankfurt am Main im Jahr 2012 sehen die 25(OH)D-Zielwerte eher ≥ 30 ng/ml (≥ 75 nmol/l) und empfehlen für Personen > 60 Jahre mit Vitamin-D-Mangel eine orale Supplementation von 800 IE bis zu 2.000 IE täglich (im ersten Jahr nach Hüftfraktur) und für Jüngere eine gewichtsadaptierte Supplementation (Tabelle 3) [20, 21].
Die Zusammenhänge zwischen dem Vitamin-D-Status und der Prävention chronischer Erkrankungen wurden nicht nur in Beobachtungsstudien, sondern zum Teil auch in Interventionsstudien mit Vitamin-D-Supplementation dokumentiert. Überzeugend ist nach Einschätzung der DGE die Datenlage in der Sturz- und Frakturprävention bei Älteren, wahrscheinlich ist der Zusammenhang zwischen Vitamin D und Funktionseinbußen des Bewegungsapparates sowie der Gesamtmortalität. Möglich ist es auch, dass ein ausreichend hoher Vitamin-D-Status vor kardiovaskulären Erkrankungen schützt und das Risiko für ein kolorektales Karzinom verringert [7].
In Interventionsstudien zur Frakturprävention wurden erst bei einer Vitamin-D-Dosierung im Bereich von ca. 500 – 800 IE (12,5 – 20 μg) pro Tag Effekte nachgewiesen. Zur Sturzprävention war nach den Ergebnissen einer Meta-Analyse eine Dosierung von > 700 IE (17,5 μg) pro Tag effektiv [22]. In den Mortalitätsstudien lag die Dosierung von Vitamin D meistens zwischen 400 und 833 IE (10 – 20 μg) pro Tag. Bei den Studien mit guter statistischer Power wurde die Gesamtmortalität im Verlauf von im Mittel 5,7 Jahren relativ um 8 % verringert [23]. In einer weiteren Meta-Analyse von 50 randomisierten Interventionsstudien mit fast 95.000 Teilnehmern, meist Frauen im Alter > 70 Jahre, wurde ebenfalls eine signifikant verringerte Mortalität durch Vitamin-D3-Supplementation ermittelt [24].
Empfohlen wird von der DGE bei älteren Männern und Frauen (≥ 65 Jahre) eine Vitamin-D-Supplementation von mindestens 800 IE (20 µg) täglich (7). Einige Experten sprechen sich für eine Zufuhr von mindestens 1.000 IE (25 µg) für alle Erwachsenen aus. Dabei ist zu beachten, dass in der Schwangerschaft Dosen über 500 IE nur nach strenger Indikationsstellung eingesetzt werden dürfen. Durch eine Vitamin-D-Supplementation von 800 bis 1.000 IE täglich werden bei über 90 % der Behandelten 25(OH)D-Serumspiegel ≥ 20 ng/ml (50 nmol/l) erreicht [7].
Die American Endocrine Society (AES) unterscheidet in ihren Empfehlungen zur diätetischen Vitamin-D-Zufuhr zwischen Prävention und Therapie bei Patienten mit nachgewiesenem Mangel [9].
Prävention
- In der Prävention wird zur Optimierung der Knochengesundheit (bei Erwachsenen) eine tägliche Aufnahme von mindestens 600 IE Vitamin D bei Kindern > 1 Jahr (0 – 1 Jahre 400 IE) und Erwachsenen von 19 – 70 Jahren empfohlen; bei Senioren > 70 Jahre wird eine Zufuhr von mindestens 800 IE täglich empfohlen.
- Um die 25(OH)D-Serumspiegel konstant > 30 ng/ml (75 nmol/l) zu heben, können bei Kindern und Jugendlichen bis 18 Jahren Tagesdosen von mindestens 1.000 IE, bei Erwachsenen von 1.500 – 2.000 IE erforderlich sein.
- Schwangere und stillende Frauen brauchen täglich mindestens 600 IE Vitamin D und zum Anheben der 25(OH)D-Serumspiegel > 30 ng/ml 1.500 – 2.000 IE täglich.
- Bei übergewichtigen Kindern und Erwachsenen sowie Patienten unter Medikamenten, die den Vitamin-D-Stoffwechsel beeinträchtigen, sind mindestens zwei- bis dreifach höhere Dosierungen erforderlich als für die Altersgruppen üblich.
Therapie
Bei Personen mit nachgewiesenem Vitamin-D-Mangel werden zeitlich befristet Supplementationen in höheren Dosierungen empfohlen:- Bei Kindern und Jugendlichen bis 18 Jahre über mindestens sechs Wochen 2.000 IE täglich oder 50.000 IE einmal pro Woche, gefolgt von einer Erhaltungstherapie mit 400 bis 1.000 IE täglich (0 – 1 Jahre) bzw. mit 600 – 1.000 IE täglich.
- Alle Erwachsenen mit Vitamin-D-Mangel sollten über acht Wochen 6.000 IE täglich oder 50.000 IE einmal pro Woche erhalten, gefolgt von 1.500 – 2.000 IE täglich.
- Bei übergewichtigen Personen, Patienten mit Malabsorptionssyndrom oder unter Medikamenten mit ungünstigem Einfluss auf den Vitamin-D-Metabolismus werden initial Tagesdosen von mindestens 6.000 – 10.000 IE Vitamin D täglich empfohlen, gefolgt von einer Erhaltungstherapie mit 3.000 – 6.000 IE täglich.
- Bei Patienten mit primärem Hyperparathyreoidismus und Vitamin-D-Mangel wird eine Supplementation nach Bedarf unter Kontrolle der Serumkalziumspiegel empfohlen.
- Generell gilt die regelmäßige (tägliche bis wöchentliche) Substitution als effektiver als die Hochdosis-Bolus-Substitution, da der autokrine Syntheseweg auf eine permanente Vitamin-D3-Zufuhr angewiesen ist [26].
Für die Substitutionstherapie stehen sowohl Präparate mit Vitamin D2 als auch D3 in verschiedenen Darreichungsformen (Tropfen, Kapseln, Tabletten) zur Verfügung. Beide Vitamin-D-Formen durchlaufen in unserem Körper die gleichen Aktivierungsschritte und sind vermutlich ebenbürtig. Es gibt allerdings auch Hinweise, dass die biologische Wirksamkeit von Vitamin D2 geringer als die von Vitamin D3 sein könnte [7]. Sinnvoll können Kombinationspräparate von Vitamin D mit weiteren Spurenelementen sein, insbesondere mit Magnesium. Durch die kombinierte Gabe könnte der Schutz von Herz und Gefäßen optimiert werden.
Interessenkonflikte: Der Autor hat keine deklariert.
Auf unserem CME-Portal www.med-etraining.de können Sie ab dem 25.04.2016 diesen Beitrag bearbeiten und bekommen bei Erfolg Ihre Punkte sofort gutgeschrieben.
Erschienen in: Der Allgemeinarzt, 2016; 38 (8) Seite 42-47