Die nichtalkoholische Fettlebererkrankung (NAFLE) gilt inzwischen als die häufigste Lebererkrankung der westlichen Welt. Besonders tückisch – weil lange ohne fassbare Beschwerden verlaufend – trägt sie wesentlich zu einem erhöhten Sterberisiko der Betroffenen bei, und dies nicht nur aufgrund der Entwicklung einer Leberzirrhose und deren Komplikationen, sondern vor allem durch eine erhöhte metabolische und kardiovaskuläre Morbidität und wahrscheinlich auch durch ein höheres Darm- und Leberkrebs-Risiko der Betroffenen.
Die nichtalkoholische Fettlebererkrankung (NAFLE) und die nichtalkoholische Steatohepatitis (NASH) sind Zivilisationskrankheiten, die fast ausschließlich bei gestörter Blutzuckerregulation und Fehlernährung vorkommen. Ihre Inzidenz und Prävalenz steigen mit der Häufigkeit von Adipositas, Diabetes mellitus und Hyperlipidämie, kurz, dem metabolischen Syndrom. Andere Ursachen und Manifestationsfaktoren sind möglich, aber vergleichsweise selten: Eine Leberparenchymverfettung tritt außerhalb des metabolischen Syndroms beispielsweise infolge familiärer Fettstoffwechselstörungen oder bei unzureichend eingestelltem Typ-1-Diabetes auf, des Weiteren bei Mangelernährung im Rahmen von Essstörungen und bei übermäßigem Konsum von Süßigkeiten, Fast Food und zuckerhaltigen Limonaden. Iatrogene Ursachen sind insbesondere eine länger andauernde parenterale Ernährung, die Dauertherapie mit Methotrexat, länger andauernde zytostatische oder antibiotische Therapien sowie die Dauertherapie mit Kortison mit den bekannten Risiken Gewichtszunahme, Dyslipidämie und Blutzuckeranstieg.
Vor allem bei jungen, nicht übergewichtigen Patienten sollten endokrinologische Störungen bedacht werden. So entwickeln junge Frauen mit polyzystischem Ovarialsyndrom aufgrund der Hyperandrogenämie recht häufig auch ohne ausgeprägte Adipositas eine Steatose; bei jungen Männern muss vor allem nach einem Anabolika-Abusus (und der Einnahme von Nahrungsergänzungsmitteln) zum Muskelaufbau gefahndet werden. Eine weitere relativ häufige endokrinologische Erkrankung, die mit einer vermehrten Leberparenchymverfettung einhergehen kann, ist die Hypothyreose.
Epidemiologie
Die Fettlebererkrankung umfasst ein Krankheitsspektrum von der einfachen Fettleber über die Fettleberentzündung mit Fibrose bis hin zur Zirrhose und einem hepatozellulären Karzinom.
Die Angaben zur Prävalenz der NAFLE in der Normalbevölkerung reichen von 6,5 bis 51 % – je nach eingesetzter Screeningmethode (Ultraschall oder Leberbiopsie). Bei Menschen mit weiteren metabolischen Risikofaktoren (insbesondere Adipositas und Diabetes mellitus) liegt sie noch höher.
Diagnostik, Differenzialdiagnostik, Screening
Die Diagnostik der Fettlebererkrankung hat sich von einer reinen Ausschlussdiagnostik zu einer gezielten Berücksichtigung zugrundeliegender Stoffwechselaberrationen entwickelt. Die (Verdachts-)Diagnose einer Leberparenchymverfettung wird meistens aufgrund einer Ultraschalluntersuchung gestellt. Häufig liegen gleichzeitig Laborveränderungen vor, insbesondere eine Erhöhung der Gamma-GT oder der Transaminasen.
Wichtig ist dann, mögliche Ursachen einer Steatose – wie Alkoholmissbrauch, endokrine Störungen, familiäre Fettstoffwechselstörungen oder auch eine chronische Hepatitis C – zu evaluieren und wenn möglich zu behandeln. Besonders schwierig in diesem Zusammenhang ist die Abgrenzung von der alkoholischen Fettlebererkrankung, wegen der Unzuverlässigkeit der Anamnese und der fehlenden zuverlässigen Biomarker für den Alkoholmissbrauch. Auch sind die in den Leitlinien empfohlenen Grenzwerte (bei uns: < 30 g Alkohol/d für Männer bzw. < 20 g/d für Frauen) recht willkürlich. Können keine behandelbaren Ursachen der Steatose identifiziert werden, ist für die Führung der Patienten das individuelle metabolische und kardiovaskuläre Risikoprofil von entscheidender Bedeutung.
Warum ist das Screening und das Management metabolischer und kardiovaskulärer Risikofaktoren gerade bei Patienten mit nichtalkoholischer Fettlebererkrankung so wichtig? Verglichen mit der Normalbevölkerung haben Menschen mit NAFLE ein signifikant erhöhtes Mortalitätsrisiko. Bedeutsam ist dabei die Unterscheidung einer einfachen Fettleber – mit unveränderter Lebenserwartung – von der Fettleberhepatitis, die sich bei einem Drittel der Patienten zur Zirrhose fortentwickeln kann.
Parameter, die schwerere histologische Veränderungen vermuten lassen, sind ein höheres Alter des Patienten, Adipositas, Diabetes mellitus und eine Transaminasenerhöhung. Gerade bei diesen Patienten ist die Gewinnung einer Leberbiopsie wichtig und hilfreich, denn die Histologie trägt wesentlich zur weiteren Risikoeinschätzung bei: Histologisch nachgewiesene Entzündung und das Vorliegen einer signifikanten Fibrose sind die wichtigsten prognostischen Faktoren hinsichtlich der Entwicklung einer Fettleberzirrhose [1].
Kardiovaskuläres Risiko
Kardiovaskuläre Erkrankungen und NAFLE/NASH haben gemeinsame Risikofaktoren. Dazu gehören Insulinresistenz, bauchbetonte Adipositas, Dyslipidämie und die meisten anderen Manifestationen des metabolischen Syndroms. Bei Patienten mit NAFLE/NASH sind diverse subklinische Anzeichen von kardiovaskulären Erkrankungen signifikant häufiger nachweisbar als bei Gesunden. Der Schweregrad der Fettleberhepatitis korreliert dabei gut mit der Ausprägung der kardiovaskulären Veränderungen – beispielhaft sei hier erwähnt, dass die Intimadicke der Carotis und die Häufigkeit von Carotis-Plaques bei Patienten mit Fettleber über der von gesunden Kontrollen liegen und diese mit dem Ausmaß der vorliegenden Fibrose der Leber auch noch weiter zunehmen [2, 3]. Auch nach Herausrechnen anderer kardiovaskulärer Risikofaktoren haben Patienten mit nichtalkoholischer Fettlebererkrankung ein höheres Risiko für das Vorliegen einer koronaren Herzkrankheit. Sowohl die Gesamt- als auch die kardiovaskuläre Mortalität bei Patienten mit NAFLE/NASH ist erhöht [4].
Typ-2-Diabetes
Der Typ-2-Diabetiker hat ein zweifach erhöhtes Risiko einer chronischen Lebererkrankung, hauptsächlich NAFLE/NASH und ihre Folgen Leberzirrhose und/oder Leberkrebs [8]. Die Diagnose einer NAFLE/NASH bei Diabetikern ist zudem assoziiert mit einer schlechten Blutzuckereinstellung, einer proliferativen Retinopathie und kardiovaskulären und renalen Folgeschäden [9]. Und schließlich haben Patienten mit NAFLE/NASH im Vergleich zu Diabetikern ohne Fettlebererkrankung ein 2,2-fach erhöhtes Mortalitätsrisiko [10].
Umgekehrt kann eine nichtalkoholische Fettlebererkrankung der Diagnose eines Diabetes mellitus vorausgehen: So hat eine schwedische Langzeituntersuchung über 14 Jahre ergeben, dass 78 % der Patienten mit histologisch gesicherter NAFLE/NASH im Verlauf eine gestörte Glukosetoleranz oder einen Diabetes mellitus entwickelten [5].
Niereninsuffizienz
Auch das Risiko einer chronischen Niereninsuffizienz ist bei nichtalkoholischer Fettlebererkrankung erhöht. Die Prävalenz reicht in unterschiedlichen Studien von 21 % bis zu 54 %, im Vergleich zu 3,7–24,2 % bei Patienten ohne Fettleber. Die meisten dieser Studien kamen zudem zu dem Ergebnis, dass die NAFLE/NASH ein unabhängiger Risikofaktor ist [11].
Kolorektales Karzinom – an Vorsorge denken
Ein erhöhtes Risiko für kolorektale Karzinome wird immer wieder diskutiert. Untersuchungen haben eine höhere Inzidenz von Kolon-Adenomen (34 vs. 21 %) und -Karzinomen (18 vs. 5,5 %) bei Patienten mit NAFLD/NASH im Vergleich zu Patienten ohne Fettleber gezeigt. Ein großer Teil dieser Läsionen wurde zudem im rechtsseitigen Kolon gefunden und bei im Vergleich zum Nicht-NAFLE-Kollektiv deutlich jüngeren Patienten [12]. Es gibt zwar bisher keine prospektiven Studien, die eine echte Kausalität bestätigen könnten, die Daten reichen jedoch in jedem Fall aus, die Notwendigkeit der zeitgerechten Vorsorge-Koloskopie in diesem Patientenkollektiv zu unterstreichen.
Obstruktives Schlafapnoe-Syndrom (OSAS)
Chronische Müdigkeit ist ein Symptom, das bei vielen Lebererkrankungen auftritt; eine weitere häufige Ursache ist das obstruktive Schlafapnoe-Syndrom. Tatsächlich ist ein obstruktives Schlafapnoe-Syndrom mit einem erhöhten Risiko einer NAFLE (OR 2,99), NASH (OR 2,37) und einer fortgeschrittenen Leberfibrose (OR 2,3) assoziiert – unabhängig von Alter, Geschlecht oder BMI der Patienten. Es wird umgekehrt ein OSAS-Screening (Anamnese, ggf. Polysomnographie) für alle Patienten mit der Diagnose einer nichtalkoholischen Fettlebererkrankung empfohlen [13].
Therapie
Es gibt bisher keine medikamentöse Behandlung mit direkter Wirkung auf Leberparenchymverfettung und Entzündungsaktivität. Im Vordergrund stehen daher die Lebensstil-Modifikation (in der Regel mit dem Ziel der Gewichtsreduktion) sowie die optimale Therapie der Begleiterkrankungen. Aufgrund der häufigen und prognosebestimmenden Komorbiditäten bei NAFLE und NASH empfehlen wir, nach Diagnosestellung und Ausschluss hepatologischer Grunderkrankungen nach subklinischen Zeichen von Begleiterkrankungen zu fahnden. In Abhängigkeit von Alter, Anamnese und Symptomatik sollten zumindest eine körperliche Untersuchung mit Gefäßstatus und Blutdruckmessung, eine Laboruntersuchung mit Nüchtern-Glukose und Lipidstatus sowie eine Urinuntersuchung zum Ausschluss einer (Mikro-)Albuminurie erfolgen. Je nach Lebensstil und kardiovaskulärem Risikoprofil können weitere Untersuchungen hinzukommen.
Ernährungs- und Lebensstil-Umstellung
Die Umstellung der Lebens- und Ernährungsgewohnheiten ist der wichtigste und am besten wirksame therapeutische Ansatz zur Behandlung einer NAFLE/NASH. Es gibt eine Reihe von kleineren Studien zur Wirksamkeit von Diät und/oder körperlicher Bewegung. Dabei scheint es vor allem eine relevante und dauerhafte Gewichtsreduktion zu sein, die eine Verbesserung bewirkt. Besonders effektiv scheint eine kalorienreduzierte, kohlenhydratarme Ernährung zu sein, sogar ohne zusätzliches Bewegungstraining. Körperliches Training allein (ohne Gewichtsabnahme) hat einen weniger ausgeprägten Effekt.
Studien zeigen, dass durch Gewichtsreduktion und Ausdauertraining die Leberwerte zurückgingen, sich die Insulinresistenz verbesserte und sich der Fettgehalt der Leber verringerte. Auch signifikante histologische Verbesserungen der Entzündungsaktivität und Parenchymverfettung wurden festgestellt, und zwar vor allem bei Patienten mit einer Gewichtsreduktion von mehr als 5–7 % des Ausgangsgewichts [14–16]. Die Gewichtsreduktion kann darüber hinaus die Progression der Leberfibrose aufhalten [17].
Andere Risikofaktoren behandeln
Bei stark übergewichtigen Menschen eine relevante und vor allem dauerhafte Gewichtsabnahme zu erreichen, bedeutet eine große Herausforderung und Frustrationstoleranz aller Beteiligten. Umso wichtiger ist deshalb die Behandlung anderer Risikofaktoren, die sowohl das kardiovaskuläre Risiko erhöhen als auch den Verlauf einer nichtalkoholischen Fettlebererkrankung verschlechtern können.
Insulin-Sensitizer
In erster Linie ist hier an eine Beeinflussung der Insulinresistenz zu denken. Orale Antidiabetika, die die Insulinresistenz verbessern, sind zum einen das lange bekannte Metformin, zum anderen die sogenannten Glitazone. Metformin vermindert bei Patienten mit metabolischem Syndrom und Diabetes mellitus vor allem die hepatische, in geringerem Ausmaß aber auch die periphere Insulinresistenz. Dass Metformin die Leberwerte verbessert, wird in einer Reihe von Studien beschrieben. Was die histologischen Befunde Steatose, Entzündung und Fibrose betrifft, sind die Ergebnisse allerdings weniger eindeutig. Interessanterweise lassen neuere epidemiologische Studien einen gewissen präventiven Effekt hinsichtlich der Entstehung eines hepatozellulären Karzinoms vermuten. Insgesamt sind die durch eine Metformintherapie erzielten Verbesserungen so gering, dass die Substanz nur bei Patienten mit manifestem Diabetes mellitus zur Blutzuckereinstellung empfohlen wird.
Glitazone können bei Patienten mit NASH die Entzündungsaktivität vermindern, die periphere und hepatische Insulinresistenz günstig beeinflussen und zur Verbesserung der Leberhistologie führen. Dies wurde für Pioglitazon in mehreren Studien gezeigt [18]. Der Einsatz der Glitazone ist allerdings limitiert durch ihr Nebenwirkungsprofil (Risiko für Herzinsuffizienz und Blasenkarzinome bei Dauertherapie); Nutzen und Risiko müssen sorgfältig abgewogen werden. In Deutschland wird ihr Einsatz nur empfohlen, wenn bei ausgeprägter NASH zusätzlich ein Diabetes mellitus vorliegt.
Vitamin E
Vitamin E, so vermutet man, reduziert den oxidativen Stress, dem die Hepatozyten ausgesetzt sind. Auch zur Vitamin-E-Gabe gibt es einige Studien, darunter eine, die Vitamin E, Pioglitazon und Plazebo vergleicht. Es fand sich eine signifikante Verbesserung des NAS-Scores in 43 % unter Vitamin E, 34 % unter Pioglitazon und 19 % unter Plazebo [18]. Der Einsatz von Vitamin E bei Patienten mit NASH ohne Diabetes mellitus kann gerechtfertigt werden, muss aber dagegen abgewogen werden, dass eine dauerhafte Vitamin-E-Therapie bei gesunden Männern das Risiko, ein Prostata-Ca zu entwickeln, erhöht [24].
Hyperlipidämie und Statintherapie
Eine NAFLE oder NASH tritt im Rahmen des metabolischen Syndroms sehr häufig mit einer Fettstoffwechselstörung zusammen auf. Man vermutet zudem, dass insbesondere die Hypertriglyzeridämie die Leberparenchymverfettung begünstigt. Nicht nur zur Verbesserung des kardiovaskulären Risikoprofils ist bei diesen Patienten eine lipidsenkende Therapie indiziert.
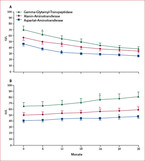
Am besten untersucht und belegt ist die Reduktion der kardiovaskulären Morbidität und Mortalität sowie eine lebensverlängernde Wirkung durch die Beta-HMG-Reduktase-Inhibitoren, die sog. Statine (Abbildung 1).
Leider sind sowohl Statine als auch Fibrate nicht nur für ihre lipidsenkende Wirkung, sondern auch für eine mögliche Hepatotoxizität als Nebenwirkung bekannt – was dazu führt, dass diese Substanzen bei Patienten mit Lebererkrankungen oft nur sehr zurückhaltend verordnet werden.
Statine führen zwar bei einigen Patienten zu einer Leberwerterhöhung, in weniger als 1 % steigt aber die GPT auf mehr als das Dreifache des Normwerts. 70 % der Patienten erfahren darüber hinaus eine spontane Normalisierung der Leberwerte bei Fortsetzung der Statintherapie. Ein Leberversagen tritt nur mit einer Häufigkeit von 0,5–1/100 000 pro Jahr auf, und das Risiko hierfür scheint bei Patienten mit NASH nicht höher zu sein als bei Patienten ohne Lebererkrankung [19–22].
Es gibt inzwischen eine Reihe von Studien, die die Auswirkungen einer Statintherapie bei Patienten mit erhöhten Leberwerten untersucht haben. Dabei zeigt sich, dass das Risiko eines Transaminasenanstiegs oder eines Leberversagens bei diesen Patienten nicht erhöht ist. Bei Patienten mit NAFLE und NASH kann es sogar zu einer Verbesserung der Laborwerte und der Leberhistologie kommen.
Zusammenfassung
Die Fettlebererkrankung ist als Bestandteil des metabolischen Syndroms von zunehmender Bedeutung. Neben der Entwicklung einer Fibrose bis hin zur Leberzirrhose mit all ihren Komplikationen sind die Betroffenen vor allem durch ein signifikant erhöhtes Risiko von kardiovaskulären Ereignissen bedroht. Nach Diagnosestellung ist deshalb die Kontrolle weiterer individueller Risikofaktoren – wie Hypertonie oder Hypercholesterinämie – für die Patienten essenziell.
Das erhöhte Darmkrebsrisiko macht darüber hinaus eine konsequente Vorsorge besonders wichtig.
Eine gezielte medikamentöse Therapie ist bisher nicht verfügbar – als gesichert gilt hier, dass Patienten mit Fettleber und einer (prä-)diabetischen Stoffwechsellage von einer Intervention profitieren. Bei isolierter Fettleberhepatitis gibt es die besten Daten – Besserung der Entzündung, Besserung der Fibrose – für Lifestyle-Interventionen, die das Ziel haben, die körperliche Aktivität zu intensivieren und eine ausgewogene Ernährung anzustreben. So einfach und so schwierig.
Interessenkonflikte: keine deklariert
Erschienen in: Der Allgemeinarzt, 2014; 36 (6) Seite 54-60