Eisenmangel und Eisenmangelanämie sind typische Erkrankungen der prämenopausalen Frau. Auch der isolierte Eisenmangel (ohne Anämie) gilt heute als therapiewürdige Krankheitsentität, die einer suffizienten, in der Regel intravenösen Eisensubstitution zugeführt werden sollte.
Der Eisenmangel ist nach Angaben der World Health Organization der häufigste Nährstoffmangel des Menschen. Dies gilt auch für westliche Industrieländer. Betroffen sind vor allem Frauen im gebärfähigen Alter [1]. Während das Problem nach der Menopause (rund 5 %) und bei Männern (unter 3 %) selten ist, liegt die Prävalenz bei menstruierenden Frauen bei 10 bis 30 % [2]. Gründe hierfür sind die heutigen Ernährungsgewohnheiten (Verzicht auf tierisches Eiweiß) und der Eisenverlust im Rahmen der Menstruationsblutung. Verstärkte Regelblutungen, wie sie bei Vorliegen von Uterusmyomen oder Antikonzeption mit einem Intrauterin-Device (IUD) vorkommen können, erhöhen das Risiko für einen Eisenmangel. Darüber hinaus entwickeln auch ältere Menschen mit intestinalen Angiodysplasien und Patienten unter Antikoagulanzientherapie oder nach bariatrischen Eingriffen häufig einen Eisenmangel.
Der Eisenmangel ist auch ein Problem im extremen Ausdauerlaufsport vor allem bei Sportlerinnen. Der wichtigste Grund hierfür ist höchstwahrscheinlich die Tendenz, sich hypokalorisch und eiweißarm zu ernähren. Darüber hinaus kommt es bei extrem langen Läufen zu Mikroblutungen im Darm und in der Harnblase (Laufen mit leerer Blase). Interessanterweise sind Radsportler hiervon praktisch nicht betroffen. Möglicherweise spielt beim Ausdauerlaufsport auch die sogenannte Foot strike hemolysis, das Zerquetschen von Erythrozyten in der Fußsohle während des Laufs, eine Rolle. Eisenverluste über den Schweiß sind quantitativ eher von untergeordneter Bedeutung [3].
Eisenbestand
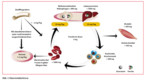
Der Eisenbestand des Menschen beträgt normalerweise 3 000 - 5 000 mg, wovon sich zwei Drittel im Hämoglobin der Erythrozyten befinden. Täglich werden 25 mg Eisen für die Erythrozyten-Neusynthese benötigt. Normalerweise wird dieser Bedarf durch Recycling von Eisen aus dem Abbau alter Erythrozyten gedeckt. Bei Blutverlusten ist der Eisenbedarf für die (gesteigerte) Erythrozyten-Neusynthese größer als die Eisenmenge, die aus dem Abbau alter Erythrozyten gewonnen wird. Unter diesen Bedingungen greift die Erythropoese dann auf an Ferritin gebundenes Speichereisen (Leber, Milz und Knochenmark) zurück (Abb. 1). Eisen wird als wichtiges Spurenelement für zahlreiche Stoffwechselvorgänge benötigt. Im Hämoglobin und Myoglobin spielt Eisen eine wichtige Rolle beim Sauerstofftransport und der intrazellulären Sauerstoffbereitstellung. In den Speicher- bzw. Transportformen liegt Eisen an Ferritin bzw. Transferrin gebunden vor, und als Bestandteil der Cytochrome ist Eisen für den Elektronentransport innerhalb der Atmungskette und damit für die mitochondriale ATP-Synthese verantwortlich. Die Eisenmangelanämie ist die klinisch wichtigste Konsequenz des Eisenmangels. Neben der Anämie kann es bei Eisenmangel durch Aktivitätsminderung eisenabhängiger Enzyme auch zu trophischen Störungen im Bereich der Haut und Schleimhäute (Haarausfall, Mundwinkelrhagaden, Aphthen) und zu ausgeprägter Adynamie kommen.
Intestinale Eisen-Resorption
Die Resorption des Nahrungseisen erfolgt ausschließlich im Duodenum, wobei Hämeisen aus tierischem Eiweiß (Fleisch) sehr viel besser resorbiert wird als pflanzliches Eisen oder pharmakologische Eisensalze (z. B. Eisensulfat). Die tägliche Eisenresorption beträgt 1 mg und steigt im Eisenmangel auf maximal 3 - 5 mg/Tag an. In der Zirkulation liegt Eisen an Transferrin gebunden vor, dem einzigen Transportprotein für Eisen im Blut (Abb. 1). Alle kernhaltigen Zellen des menschlichen Organismus verfügen über Transferrin-Rezeptoren, mit denen sie Transferrin-gebundenes Eisen aufnehmen können.
Symptome des Eisenmangels
Es gibt durchaus Situationen, z. B. bei chronischen Blutungen (intestinal oder im Rahmen der Monatsregel), die allmählich zu einer kompletten Depletion der Eisenspeicher und zu einem peripheren Eisenmangel führen, während sich die Erythropoese gerade noch ausreichend mit Eisen versorgen kann. Solche Patienten haben ein Ferritin, das gegen null geht, aber noch keine Anämie. Als Zeichen des Eisenmangels ist es aber vielleicht schon zu ausgeprägtem Haarausfall, nicht heilenden Aphthen im Bereich der Mundschleimhaut, einer schweren Fatigue oder einem Restless-Legs-Syndrom gekommen.
Isolierten Eisenmangel behandeln?
Bedarf ein isolierter Eisenmangel ohne Anämie einer Therapie? Diesbezüglich haben jetzt Wissenschaftler aus Zürich eine randomisierte, plazebokontrollierte Doppelblindstudie an 90 prämenopausalen Frauen mit isoliertem Eisenmangel und Fatigue-Syndrom publiziert [4]. Alle Studienteilnehmerinnen hatten einen Eisenmangel mit Ferritin-Werten < 50 ng/ml ohne Anämie (Hb > 12 g/dl). In der Verum-Gruppe erhielten die Frauen 800 mg Eisen-Saccharose i.v. über einen Zeitraum von zwei Wochen versus NaCl 0,9 % i.v. in der Plazebogruppe. Als Endpunkte wurden der Schweregrad der Fatigue und verschiedene Parameter des Eisenstoffwechsels untersucht. Nach zwölf Wochen hatten sich die Fatigue-Symptome in der Eisen-Gruppe bei 63 % und im Plazebo-Arm bei 34 % der Betroffenen gebessert. In der Subgruppe mit Ferritin-Werten < 15 ng/ml hatten 82 % der Frauen von der i.v.-Eisentherapie profitiert versus 35 % in der Plazebo-Gruppe (p = 0,005).
Diese Ergebnisse sind in mehrfacher Hinsicht bemerkenswert:
- Zum ersten Mal konnte in einer randomisierten, plazebokontrollierten Doppelblindstudie gezeigt werden, dass der isolierte Eisenmangel (definiert durch ein Ferritin < 50 ng/ml) ohne Anämie tatsächlich eine therapiewürdige Krankheitsentität darstellt.
- Die Menge an Eisen, die zum Ausgleich des isolierten Eisenmangels verabreicht werden musste, betrug 800 mg. Bei der menstruierenden Frau ist es praktisch unmöglich, eine solche Menge oral zu substituieren.
- Die Tatsache, dass es in der Eisen-Gruppe zu einem Anstieg des Hämoglobins um 1,0 g/dl (innerhalb des Normbereichs) gekommen war, spricht dafür, dass die Erythropoese doch unter eisendefizitären Bedingungen erfolgt ist, ohne dass dies an den Erythrozyten-Indices zu erkennen war.
- In der Studie wurde die i.v.-Eisensubstitution mit Eisen-Saccharose zu je 200 mg an vier aufeinanderfolgenden Tagen bis zum Erreichen der Gesamtmenge von 800 mg durchgeführt. Heute steht mit Eisen-Carboxymaltose (Ferinject®) ein neues i.v.-Eisenpräparat zur Verfügung, mit dem bis zu 1 000 mg als Kurzinfusion auf einmal verabreicht werden können.
Basisdiagnostik zur Beurteilung des Eisenhaushalts
Blutbild
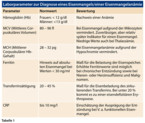
Um eine Anämie aufzudecken, sollte ein Blutbild angefertigt werden. Anhand des Hämoglobins (Hb) kann dann festgelegt werden, ob eine Anämie besteht: Frauen: Hb < 12 g/dl; Männer: Hb < 13 g/dl. Die maschinellen Blutbildanalysatoren bestimmen auch noch die Erythrozytenparameter: MCV (Mittleres Corpuskuläres Volumen: 80 - 96 fl) und MCH (Mittlerer Corpuskulärer Hb-Gehalt: 28 - 32 pg). Die Eisenmangelanämie ist klassischerweise mikrozytär (MCV erniedrigt) und hypochrom (MCH erniedrigt).
Ferritin
Serum-Ferritin ist ein Maß für die Beladung der Eisenspeicher. Ferritinwerte von weniger als 30 ng/ml gelten als Hinweis auf einen absoluten Eisenmangel. In der Regel geht der absolute Eisenmangel auch mit einer Eisenmangelanämie einher. Es gibt aber immer wieder Patienten mit sehr niedrigen Ferritinwerten, die noch keine Anämie entwickelt haben [5]. Bei Patienten mit chronischen Erkrankungen (Nieren- oder Herzinsuffizienz, Malignome) sowie chronischer Inflammation finden sich häufig erhöhte Ferritinwerte, da es zu einer Akkumulation von Eisen in den Speichern kommt, während das Eisen aus der Peripherie abgezogen wird, was zu einer Erniedrigung der Transferrinsättigung (TSAT) führt. In solchen Fällen spricht man von einem funktionellen Eisenmangel [6].
Transferrinsättigung
Die Transferrinsättigung (TSAT) ist ein Parameter für die Eisenbeladung des zirkulierenden Transferrins. Der Normalbereich wird mit 20 - 45 % angegeben [7]. Bei Werten unter 20 % kommt es in Abhängigkeit von der erythropoetischen Aktivität zur Entwicklung einer eisendefizitären Erythropoese.
C-reaktives Protein
Besteht der Verdacht auf einen funktionellen Eisenmangel (Ferritin normal oder erhöht, TSAT erniedrigt) bei signifikanten Begleiterkrankungen, sollte das C-reaktive Protein (CRP) bestimmt werden, um die Schwere der begleitenden Entzündungsreaktion und damit deren Einfluss auf die o. g. Eisenparameter abschätzen zu können.
Isolierte Bestimmung des Serum-Eisens obsolet
Die isolierte Bestimmung des Serum-Eisens wird heute nicht mehr empfohlen, da das Serum-Eisen durch eine Vielzahl von Faktoren (Eisenbestand, zirkadiane Schwankungen, entzündliche Prozesse, Aktivität der Erythropoese) beeinflusst wird.
Orale Eisensubstitution
Die orale Eisentherapie mit pharmakologischen Eisensalzen ist quantitativ in vielen Fällen unzureichend, da in der Regel nicht mehr als 5 - 7 % der eingenommenen Eisenmenge tatsächlich auch resorbiert werden (Abb. 2). Der Rest verbleibt im Darmlumen und verursacht Nebenwirkungen wie Nausea, Bauchschmerzen und Obstipation. Nüchterneinnahme verbessert die Resorption, geht aber mit mehr gastrointestinalen Beschwerden einher [8]. Grundsätzlich kann eine orale Substitution mit 100 - 200 mg Eisen pro Tag versucht werden. In den meisten Fällen wird die orale Substitution aber nicht ausreichen, um z. B. den Eisenverlust der prämenopausalen Frau (wg. des persistierenden Blutverlusts) langfristig auszugleichen.
i.v.-Eisen-Substitution
Derzeit stehen in Deutschland fünf parenterale Eisenpräparate zur Verfügung: Ferrlecit®, Venofer®, FerMed®, CosmoFer® und Ferinject®. Bei Ferrlecit® handelt es sich um einen Eisen-(III)-Gluconat-Sucrose-Komplex, Venofer® und FerMed® stellen Eisen-(III)-Hydroxid-Saccharose-Präparate dar, CosmoFer® besteht aus einem Eisen-(III)-Hydroxid-Dextran-Komplex und Ferinject® ist ein Eisen-(III)-Carboxymaltose-Komplex. Zwischen diesen Präparaten bestehen wesentliche Unterschiede hinsichtlich Stabilität der Eisenkomplexe und Inzidenz an anaphylaktoiden Reaktionen.
Die höchste Komplexstabilität weisen Eisen-Carboxymaltose und Eisen-Dextran auf, gefolgt von den Eisen-Saccharose-Präparaten. Eisen-Gluconat hat die geringste Stabilität. Dies ist insofern relevant, da Eisenpräparate mit hoher Komplexstabilität mit weniger akuter Eisentoxizität einhergehen, und deshalb in höheren Einzel-Dosierungen und schneller verabreicht werden können: Eisen-Carboxymaltose 1 000 mg in 15 min, Eisen-Dextran 1 000 mg über 6 h, Eisensaccharose-Präparate 500 mg über 3,5 h und Eisen-Gluconat 62,5 mg innerhalb von 20 - 30 min.
Parenterale Eisenpräparate können Unverträglichkeitsreaktionen hervorrufen. Diese treten jedoch in unterschiedlichen Häufigkeiten auf: Eisen-Dextran: 33/10 000 000, Eisen-Gluconat: 9/10 000 000 und Eisen-Saccharose: 6/10 000 000 [9]. Für Eisen-Dextran und Eisen-Saccharose empfehlen die Hersteller vor der erstmaligen Applikation die Verabreichung einer Testdosis, während dies bei Eisen-Carboxymaltose nicht notwendig ist, da hier keine Dextran-vermittelten anaphylaktoiden Zwischenfälle zu erwarten sind.
Vorgehen in der Praxis
Der isolierte Eisenmangel (ohne Anämie) kann in vielen Fällen mit einer einzigen Kurzinfusion von 500 mg Eisen-Carboxymaltose in 100 ml NaCl 0,9% ausgeglichen werden. Nach vier Wochen sollte eine Kontrolle von Ferritin und TSAT erfolgen. Frühere Kontrollen sind nicht sinnvoll, da Ferritin und TSAT durch die i.v.-Eisengabe selbst erhöht werden. Wenn nach vier Wochen das Serum-Ferritin noch deutlich unter 100 ng/ml liegt, kann nochmals 500 mg Eisen-Carboxymaltose nachgegeben werden.
Besteht eine Eisenmangelanämie, ist es sinnvoll, die Substitution mit 1 000 mg Eisen-Carboxymaltose in 250 ml NaCl 0,9 % zu beginnen. Für die Anämiekorrektur rechnet man mit einem Eisenbedarf von 200 mg pro Hb-Anstieg von 1g/dl, d. h. will man das Hb um 2 g/dl anheben, werden 400 mg Eisen für die Hämoglobin-Korrektur benötigt. Zusätzlich sollte man die leeren Speicher mit 500 mg Eisen bevorraten [10]. Nach vier Wochen sollten Hb, Ferritin und TSAT überprüft werden. Bei einem Ferritin unter 100 ng/ml kann es sinnvoll sein, nochmals 500 mg Eisen-Carboxymaltose nachzugeben.
Nach erfolgter Korrektur ist es bei der prämenopausalen Frau wegen des anhaltenden Blutverlusts sinnvoll, Hb und Ferritin ein- bis zweimal pro Jahr zu kontrollieren, um rechtzeitig, d. h. bevor sich erneut ein Eisenmangel entwickelt, Eisen substituieren zu können.

Erschienen in: Der Allgemeinarzt, 2011; 33 (18) Seite 42-46