Eine Anämie kommt bei älteren Menschen relativ häufig vor. Noch bis vor wenigen Jahren hat man eine milde Anämie im Alter als physiologisch erachtet und keinen Handlungsbedarf gesehen. Heute weiß man zum einen, dass eine Anämie mit einer höheren Mortalität und Morbidität verbunden ist. Zum anderen stehen effektive Therapien zur Verfügung. Deshalb sollte man auch bei über 65-Jährigen eine Anämie abklären
Gemäß WHO besteht eine Anämie bei einer Hämoglobinkonzentration von unter 120 g/l bei nicht schwangeren Frauen (bei schwangeren Frauen unter 110 g/l) und bei unter 139 g/l bei Männern, schreiben Hämatologen und Geriater des Universitätsspitals Zürich in der Zeitschrift Praxis [1]. Ob diese Grenzwerte auch für ältere Menschen gelten sollten oder aufgrund eines "physiologischen" Abfalls des Hämoglobins angepasst werden müssen, ist umstritten. Aus dem Jahr 2007 stammt die Empfehlung der Deutschen Gesellschaft für Hämatologie und Onkologie, niedrige Hämoglobinwerte bei über 80-Jährigen erst abzuklären, wenn sie weniger als 110 g/l betragen. Neuere Untersuchungen bezweifeln diesen normalen Abfall im Alter und konnten belegen, dass sich auch bei älteren Patienten eine Abklärung lohnt und in den meisten Fällen eine Ursache der Anämie gefunden wird.
Symptome und Risiken
Bei über 10 % der über 65-Jährigen lässt sich eine Anämie nachweisen und bei mehr als 20 % der über 80-Jährigen. Männer sind häufiger betroffen als Frauen. Typischerweise handelt es sich um eine leichte Anämie. Doch auch eine leichte Anämie ist bei älteren Menschen mit einer erhöhten Mortalität und Morbidität assoziiert. Dabei ist unklar, ob dieser Zusammenhang kausal ist oder die Anämie nur ein Zeichen einer beginnenden chronischen Erkrankung oder Entzündung ist. Besonders ausgeprägt ist die Erhöhung der Mortalität bei Patienten mit Herzinsuffizienz. Was die erhöhte Morbidität angeht, so leiden ältere Menschen mit Anämie häufiger unter verminderter Lebensqualität, Muskelkraft und Leistungsfähigkeit. Zudem steigen das Sturz- und das Hospitalisationsrisiko sowie das Risiko, Depressionen zu entwickeln.
Mögliche Ursachen
Laut einer US-Studie an über 65-Jährigen mit Anämie war ein Drittel davon substratbedingt, was in knapp 50 % auf Eisenmangel inklusive chronischer Blutungsanämien zurückzuführen war. Die anderen 50 % entfielen auf Folsäure- und Vitamin-B12-Mangel bzw. Kombinationen davon. Ein weiteres Drittel war auf eine chronische Entzündung, eine Nierenerkrankung oder beides zurückzuführen und in ebenfalls einem Drittel der Fälle blieb die Ursache unklar.
Von diesen unklaren Fällen könnte ein beträchtlicher Teil durch das Myelodysplastische Syndrom bedingt sein, schreiben die Schweizer Kollegen. Insbesondere wenn nur die rote Zellreihe betroffen ist, ist dies schwierig zu diagnostizieren. Hinweise darauf sind eine MCV-Erhöhung und eine zusätzliche Zytopenie. Möglicherweise spielen auch Alkoholkonsum, Polymedikation, vermindertes Ansprechen des hämatopoetischen Systems auf Erythropoietin, subklinische Entzündungszustände oder Nierenfunktionsstörungen sowie bei Männern ein Testosteronmangel bei diesen unklaren Anämien im Alter eine Rolle.
Sinnvolle Diagnostik
Bei der Abklärung einer Anämie sollten nicht nur der Hämoglobinwert, sondern auch Faktoren, die diesen beeinflussen, berücksichtigt werden. Dazu zählen Raucherstatus, Höhe über dem Meeresspiegel des Wohnorts, Testosteronspiegel (beim Mann) sowie Fluktuationen des Plasmavolumens (Dehydratation). Bei ungefähr zwei Drittel der älteren Patienten mit Anämie erlauben die Anamnese sowie die Erfassung weniger Laborwerte (Blutbild plus Ausstrich, MCV, MCHC, Retikulozyten, Ferritin, CRP, Serum-Vitamin-B12, Serum-Folsäure, Serum-Kreatinin) eine Diagnose.
Je nach MCV und MCHC kommen die folgenden Differenzialdiagnosen infrage:
- Mikrozytäre Anämie (Eisenmangel, chronische Entzündung, Thalassämie)
- Makrozytäre Anämie (Vitamin-B12- oder Folsäure-Mangel, Medikamente, Hämolyse, Myelodysplastisches Syndrom, Lebererkrankungen, Hypothyreose)
- Normozytäre Anämie (Hämolyse, chronische Erkrankung, renal oder endokrin bedingt, Frühform von Eisen- oder Vitaminmangel, Knochenmarksinfiltration)
- Hypochrome Anämie (Eisenmangel, chronische Entzündung, Thalassämie)
- Hyperchrome Anämie (Hereditäre Sphärozytose, Autoimmunhämolyse)
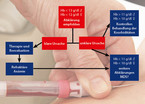
Lässt sich nach der beschriebenen Diagnostik die Anämie nicht einordnen, sind weitergehende hämatologische Untersuchungen dann indiziert, wenn es sich um eine ausgeprägte Anämie handelt, d. h. Hämoglobin < 100 g/l (Frauen) bzw. < 110 g/l (Männer). Weitere Indikationen sind Hinweise auf eine hämatologische Grunderkrankung (z. B. Myelodysplastisches Syndrom) und relevante Hämolysen (Retikulozyten!) (vgl. Abb. 1).
Myelodysplastisches Syndrom
Dem Myelodysplastischen Syndrom (MDS) kommt bei der Differenzialdiagnostik eine besondere Bedeutung zu, da neue Therapiemöglichkeiten verfügbar sind. Man schätzt, dass ungefähr ein Drittel aller unklaren Anämien darauf zurückzuführen ist. Daran denken sollte man bei folgenden Befunden:
- Makrozytäre Anämie, Thrombozytopenie und/oder Neutropenie, Monozytose
- Im Blutausstrich dysmorphe neutrophile Granulozyten oder Thrombozyten, deutliche Poikilozytose oder Anisozytose der Erythrozyten
- B-Symptome, Splenomegalie, Lymphadenopathie, Infekthäufung, verzögerte Wundheilung
In diesen Fällen sollte eine Knochenmarkuntersuchung stattfinden, wobei der Patient infektfrei sein muss, weil mögliche infektbedingte Veränderungen die Beurteilung von Dysmorphien erschweren.
Therapie
Wird eine spezifische Ursache für die Anämie gefunden, wird selbstverständlich kausal behandelt, d. h. Eisen, Folsäure oder Vitamin B12 substituiert oder nach einer Blutungsquelle gesucht. Bei einer renalen Ursache (Kreatinin-Clearance < 30 – 40 ml/min) sind erythropoesestimulierende Medikamente und evtl. Eisenpräparate gefragt. Bei Niereninsuffizienz ist ein Hb-Wert von über 100 g/l anzustreben, bei Dialysepflicht jedoch maximal 120 g/l.
Die einzige kurative Therapie des myelodysplastischen Syndroms, einer klonalen hämatopoetischen Stammzellerkrankung, besteht aus einer Stammzelltransplantation (HSCT). Deren Einsatz ist jedoch durch das Alter des Patienten und die behandlungsassoziierte Morbidität limitiert. Effektiv sind die DNA-demethylierenden Substanzen Azacitidin und Decitabin. Lenalidomid wird eingesetzt beim 5q-Syndrom. Bei einem Hb < 100 g/l und niedrigem Risiko ist die Gabe von erythropoesestimulierenden Substanzen (ESA) zu überlegen. Der Hb sollte dann aber nicht über 120 g/l angehoben werden, um keine Komplikationen zu riskieren.
Bleibt die Ursache einer Anämie auch nach erweiterter Diagnostik unklar, stellt sich die Frage, ob man mit einem Erythropoietin behandeln sollte. Dazu liegen aber bislang keine Studien vor, weshalb die Autoren im Allgemeinen davon abraten. Eine Ausnahme würden sie bei transfusionsabhängigen Patienten machen, um den Transfusionsbedarf zu senken.
Dr. med. Vera Seifert
1) A. Himmelmann, O. Rychter, J. S. Goede: Anämie im Alter: Wen, wie, warum abklären, Praxis 2012; 101 (19): 1261 – 1266
Erschienen in: Der Allgemeinarzt, 2013; 35 (17) Seite 18-19