Bei Kindern mit Verbrühungen kommt es auf eine gute Erstversorgung an und darauf, je nach Ausdehnung und Tiefe der Hautschäden sofort eine Klinikeinweisung zu veranlassen. Denn bei zu langer konservativer Behandlung können bleibende Narben entstehen. Im folgenden Beitrag soll auf die Therapie leichter bis mittelschwerer thermischer Verletzungen im ambulanten Bereich sowie auf Indikationen zur Vorstellung in spezialisierten Abteilungen eingegangen werden.
Bei der Behandlung von thermisch verletzten Kindern stehen die Verbrühungsunfälle mit 53 bis 75 % [1] stark im Vordergrund. Aufgrund der deutlich dünneren Haut von Kindern im Vergleich zu Erwachsenen kommt es bereits durch 60 bis 70 °C heiße Getränke oder Speisen zu Verbrühungen von relevanter Tiefe und Körperoberfläche (Abb. 1). Dabei entstehen oft Mischbilder bezüglich der Verletzungstiefe.
Hauptursache: Haushaltsunfälle
In den Industrienationen entfallen etwa die Hälfte aller schweren thermischen Verletzungen auf Kinder [2]. Laut dem Bundesamt für Statistik werden in Deutschland jährlich etwa 6 000 Kinder mit Verbrennungen oder Verbrühungen stationär behandelt. Hinzu kommen noch geschätzte 50 000 ambulant behandelte Fälle [3]. Die größte Häufung findet sich in der Altersgruppe der 1- bis 5-jährigen mit leichter Knabenwendigkeit [2]. Ursächlich sind in den meisten Fällen Haushaltsunfälle (Wasserkocher, Kaffeekanne, Kaminofen etc.) [1, 4, 5].
Empfehlungen für Ersthelfer
Bei der Erstversorgung ist es wichtig, eine gute Balance zwischen lokaler Kühlung und Vermeidung einer Auskühlung der kleinen Patienten zu finden. Die Kühlung mit 15- bis 20 °C kaltem Wasser für 20 Minuten innerhalb der ersten drei Stunden nach einer thermischen Verletzung resultiert in einer guten Analgesie, vermindert ein weiteres Fortschreiten der Verbrennungstiefe, fördert die Reepithelisierung und vermindert das Risiko von Narbenbildungen [6 – 11]. Allerdings besteht bei einer betroffenen Körperoberfläche (VKOF) von über 10 % ein deutlich höheres Risiko für eine Hypothermie [12]. Aufgrund der erhöhten Letalität durch Hypothermie wird bei Verbrennungen und Verbrühungen von über 15 % VKOF bei Kleinkindern, Säuglingen und Neugeborenen sowie bei intubierten und beatmeten Patienten von einer Kühlung abgeraten [13, 14]. Die Körpertemperatur sollte dokumentiert und die betroffenen Areale während des Weitertransports mit sauberen, nicht haftenden, isolierenden Folien oder Tüchern abgedeckt werden.
Betroffene Körperoberfläche (VKOF)
Zur Beurteilung der VKOF stehen dem Ersthelfer in erster Linie die modifizierte Neunerregel nach Wallace [18] bzw. deren Modifizierung bei Kindern (Tabelle 1) sowie die Handflächenregel [19] zur Verfügung. Letztere besagt, dass die Handfläche einschließlich der Finger des Patienten ca. 1 % seiner Körperoberfläche ausmacht. Zur Vermeidung einer hämodynamischen Schocksituation [15] sollte ab ca. 10 % betroffener VKOF eine Volumentherapie schon während des Transports eingeleitet werden. Diese sollte jedoch 10 ml/kg/h nicht überschreiten [16, 17]. Da in Notfallsituationen in bis zu 70 % der Fälle die VKOF deutlich überschätzt wird [24], erfolgt nach Abklingen der perifokalen Hyperämie bei Eintreffen in der Klinik immer eine Reevaluation der VKOF.
Beurteilung der Verletzungstiefe
Die Schwere der Verletzung und damit die weitere Therapieentscheidung ist neben der VKOF maßgeblich abhängig von der Verbrennungstiefe. Besondere Bedeutung kommt der Unterscheidung zwischen oberflächlich dermalen Grad-IIa- (restitutio ad integrum) und tief dermalen Grad-IIb-Verletzungen (narbige Abheilung) zu.
Zum Ausschluss einer Kindesmisshandlung muss der berichtete Unfallmechanismus bezüglich seiner Plausibilität analysiert werden. Prinzipiell verdächtig sind hier Immersionsverletzungen der Extremitäten mit Handschuh-/ Strumpfmuster oder des Gesäßes, isolierte Verbrühungen des Gesäßes oder des Perineums mit scharfen Begrenzungen nach kranial, das Vorliegen zusätzlicher Verletzungen ohne Bezug zur Verbrühung, eine inkompatible Anamnese, Kontaktverbrennungen mit scharf begrenzten geometrischen Mustern sowie multiple Verbrennungen an unterschiedlichen Körperstellen.
In welche Klink einweisen?
Verbrennungen 2. Grades von > 10% VKOF, Verbrennungen 3. Grades > 5 % VKOF, thermische Läsionen im Gesicht, an der Hand, am Fuß, im Genitalbereich oder über großen Gelenken mit relevanter Größe und Tiefe, Inhalationstraumata sowie alle thermischen Verletzungen 4. Grades sollten in einem Zentrum für Schwerbrandverletzte Kinder behandelt werden. Kinder mit Verletzungen unterhalb dieser Indikationen sollten in einer spezialisierten Klinik für brandverletzte Kinder vorgestellt werden.
Lokaltherapie
Grundsätzlich ist sowohl im ambulanten wie auch im stationären Bereich eine phasengerechte Lokaltherapie erforderlich. Deren Ziele bestehen darin, Infektionen mit der Gefahr einer sekundären Vertiefung der Verletzung zu vermeiden und eine schmerzfreie Behandlung sowie eine Minimierung verbleibender Narben zu ermöglichen. Bei unzureichendem Tetanusimpfschutz muss nach den Richtlinien der STIKO aufgefrischt werden [20].
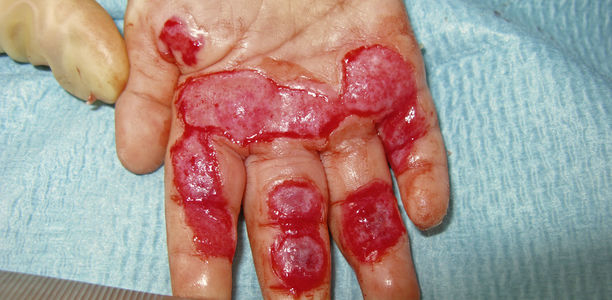
Erstgradige Verletzungen können mit fettenden Externa in Kombination mit leichten Schutzverbänden therapiert werden. Bei Verletzungen ab Grad 2 müssen die Wunden entsprechend der Tiefe der Nekrosen schmerzfrei debridiert oder nekrektomiert werden (Abb. 2). Hautblasen können einfach abgetragen werden, tiefere Gewebsnekrosen müssen entsprechend aggressiver debridiert werden. Spezielle Débridement-Schwämme, gewebeschonende Hydrochirurgie-Systeme sowie das Humby- oder Weckmesser kommen hier zur Anwendung. Bei Verletzungen dritten und vierten Grades, die mindestens 2/3 der Zirkumferenz betreffen, ist die Indikation zur Escharotomie (Durchtrennung oberflächlicher Hautschichten) zu überprüfen. Bei Verdacht auf ein Kompartmentsyndrom ist zusätzlich eine Fasziotomie erforderlich.
Bei zweitgradigen Verletzungen sollten die verwendeten modernen Wundauflagen ggf. in Kombination mit desinfizierenden Wundgelen beim Verbandwechsel eine gute Beurteilung des Wundgrundes ohne vorheriges schmerzhaftes und traumatisches Ablösen von Salbenresten oder Wundauflagen ermöglichen. Silber- oder jodhaltige Wundcremes sind daher bei der Versorgung von Kindern zu vermeiden. Nicht haftende Hydrokolloid- oder Silikongazen oder -schwämme sollten bevorzugt eingesetzt werden. Die alternative Verwendung von alloplastischem temporärem Hautersatzmaterial (Suprathel®, Biobrane® etc.) erfordert ein ausgiebiges Débridement bis in vitale, kapillär blutende Gewebsschichten, um ein Anhaften dieser kostenintensiven Materialen zu gewährleisten (Abb. 3). Bei den nachfolgenden Verbandwechseln alle drei bis sechs Tage wird dann nur noch die obere Fettgazelage gewechselt, in den abgeheilten Randbereichen löst sich im Verlauf sukzessive die Kunsthaut ab und kann reduziert werden (Abb. 4). Bei allen anderen Verbänden muss bei jedem Wechsel der Wundgrund kritisch beurteilt werden. Die Demarkation tief-dermaler Verletzungsanteile sowie eine verlängerte Reepithelisierungszeit über 21 Tage sind häufig Hinweis auf eine erforderliche Therapieerweiterung [21, 22] und sollten zu einer zeitnahen Vorstellung beim Spezialisten führen. Bei Fortführen der konservativen Therapie über diesen Zeitraum hinaus ist das Risiko für hypertrophe Narben signifikant erhöht (Abb. 5)
Bei tief-dermalen Verletzungen Grad IIb und tiefer ist eine Deckung mit Spalthaut, Keratinozyten oder ggf. Lappenplastiken erforderlich. Bei großen Defekten kann eine temporäre Deckung mit biosynthetischen Folien, allogener Spalthaut oder mittels Vakuumversiegelung durchgeführt werden.
Nachbehandlung
Nach zeitgerechter Abheilung ist ein regelmäßiges Massieren der Narbenareale (mindestens zweimal täglich) mit fetthaltigen Cremes, z. B. Dexpanthenolcreme, zu empfehlen. Zur Vermeidung bleibender Pigmentierungsstörungen ist ein adäquater Sonnenschutz erforderlich. Bei beginnender leichter Narbenbildung kann eine Therapie mit Silikonpflastern wirksam sein (Abb. 6). Bei deutlich aktiven Narben (Rötung, beginnende Verhärtung) sollte frühzeitig eine Kompressionsbehandlung mit individuell hergestellten Kompressionswäscheteilen initiiert werden (Abb. 7). Um eine Anwendung der Kompressionswäsche 24 Stunden täglich zu gewährleisten, muss diese in zweifacher Ausführung verordnet werden. Pausen sollten nur für Körperhygiene, die Narbenmassage und beim Schwimmen eingelegt werden.
Chirurgische Narbenkorrekturen sollten bei Kindern so spät wie möglich und so früh wie nötig erfolgen (v. a. bei funktionellen Einschränkungen, nach Möglichkeit erst bei bereits inaktiver Narbe).
- Kühlung möglichst nur lokal, Auskühlung unbedingt vermeiden.
- Die Kontrolle des Tetanusimpfschutzes ist immer erforderlich.
- Wundversorgung und Verbandswechsel müssen bei Kindern nach Möglichkeit schmerzfrei durchgeführt werden.
- Zur Beurteilung des Wundgrundes Verwendung von Wundauflagen, die nicht haften und keine Reste auf dem Wundgrund hinterlassen.
- Beachtung der Indikationen zur Verlegung in ein Zentrum für brandverletzte Kinder.
- Frühzeitige Vorstellung ambulanter Kinder in Spezialsprechstunden bei tief-dermalen Verletzungen (Grad IIb) sowie bei verlängerter Abheilungszeit über 21 Tage.
- Eine verlängerte Abheilungszeit korreliert direkt mit der Ausbildung hypertropher Narben.
- Regelmäßige Kontrollen auch noch nach der Abheilung zur Einleitung einer adäquaten Narbentherapie, falls erforderlich.
- Beachtung der Empfehlungen der AWMF-Leitlinie Thermische Verletzungen im Kindesalter (http://www.awmf.org/leitlinien/detail/ll/006-128.html)
Interessenkonflikte: Die Autorin hat keine deklariert.
Erschienen in: Der Allgemeinarzt, 2015; 37 (15) Seite 46-50