Medikamenten-induzierte Leberschäden äußern sich in auffälligen Laborparametern. Das Spektrum reicht von asymptomatischen Leberwerterhöhungen bis zum akuten Leberversagen. Die Diagnose der Drug-induced liver injury (DILI) erfordert den Ausschluss alternativer Ursachen für den Leberschaden.
- Dosisabhängiger (oder intrinsischer) DILI, bei dem eine Überdosierung den Leberschaden verursacht. Typisches Beispiel ist hier Paracetamol.
- Idiosynkratischer DILI (DILI im engeren Sinne), der eine Reaktion eines individuellen Patienten auf ein bestimmtes Medikament darstellt. Diese Art der Leberschädigung wird durch eine Vielzahl zugelassener Medikamente, aber auch durch Nahrungsergänzungsmittel und pflanzliche Stoffe verursacht.
Paracetamol-Intoxikation
DILI durch Paracetamol ist in über 70 % der Fälle Resultat einer in suizidaler Absicht eingenommenen Überdosis. In den USA stellt die Paracetamol-Intoxikation mit einer Inzidenz von ca. 15 Fällen/100.000 Einwohner pro Jahr die häufigste Ursache aller akuten Leberversagen dar. Mechanismus der Schädigung ist die mit zunehmender Dosis vermehrte Bildung des toxischen Metaboliten N-Acetyl-p-Benzoquinone-Imine (NAPQI). Ist die Leber vorgeschädigt und/oder sind die Glutathionspeicher erschöpft, kann die Schwellendosis, bei der es zu einer Leberschädigung kommt, herabgesetzt sein (z. B. Malnutrition, Alkoholismus, Leberzirrhose).
Paracetamol ist trotz seiner dosisabhängigen Lebertoxizität ein wichtiges Medikament: Da Paracetamol nahezu kein Risiko für eine idiosynkratische Schädigung besitzt, ist es bei der Schmerzbehandlung von Patienten mit Leberzirrhose in Dosen von 2 g/Tag (max. 3 g) das Mittel der ersten Wahl.
Idiosynkratischer DILI
Diese Art der Leberschädigung besteht in einer Reaktion eines individuellen Patienten auf ein bestimmtes Medikament. Die Inzidenz beträgt ca. 19 Fälle pro 100.000 Einwohner pro Jahr [3]. Es sind nur wenige Patienten betroffen, die das Medikament einnehmen. Aktuell wird davon ausgegangen, dass das auslösende Medikament bzw. reaktive Metabolite zu Zellstress führen (z. B. durch individuelle Stoffwechselbesonderheiten), welche über immunologische Mechanismen und mitochondriale Dysfunktion zur Leberzellschädigung führen [4]. Unter Umständen kann der in Gang gesetzte immunologische Mechanismus auch trotz Absetzen des auslösenden Medikaments ein Leberversagen verursachen. Die Reaktion tritt meist 1–6 Monate nach Beginn der fraglichen Medikation auf. In Einzelfällen kann die Latenz Jahre betragen (z. B. ist dies für Statine und Nitrofurantoin beschrieben). Auch kann es vorkommen, dass der Leberschaden erst nach Beendigung der Therapie offensichtlich wird (Amoxicillin/Clavulanat).
Häufig als ursächlich beschriebene Medikamente sind: Antibiotika (Amoxicillin/Clavulanat), Nichtsteroidale antiinflammtorische Medikamente (Diclofenac), Immunmodulatoren, Psychopharmaka, Antiepileptika, Lipidsenker (Statine) und orale Antikoagulanzien. Dies hängt wahrscheinlich auch mit deren weit verbreiteter Anwendung zusammen. Muster und Latenzzeit sind zwar variabel, können aber bei der Diagnose helfen, wenn schon Daten über die typische Signatur eines Medikaments bekannt sind (hilfreich ist hier z. B. https://livertox.nih.gov/).
DILI stellt eine besonders herausfordernde Diagnose dar, die aktuell im Wesentlichen auf dem Ausschluss anderer Ursachen beruht [5]. Die Diagnose umfasst also den Ausschluss viraler Hepatitiden, extrahepatischer Cholestase, Leberischämie (Schock, Herzinsuffizienz, Gefäßverschlüsse), Stoffwechsel- und Autoimmunerkrankungen. In der Praxis macht idiosynkratischer DILI einen Großteil der DILI -Fälle aus, weshalb sich im weiteren Text die Abkürzung DILI auf die idiosynkratische Form bezieht.
Symptomatik
Die Leberwertveränderungen bei DILI sind unspezifisch und variabel. Es werden 3 Formen unterschieden, unterteilt anhand der Ratio (R), welche den Quotienten von ALT (x-fache Erhöhung über der Norm) und AP (x-fache Erhöhung über der Norm) darstellt (Tabelle 2) [6].
Die Konsensus-Kriterien für DILI fordern fordern für klinisch relevanten DILI eine Transaminasenerhöhung von mindestens dem 5-Fachen der Norm, eine alkalische Phosphatase vom Doppelten der Norm oder Transaminasen ≥3-fache Norm und Gesamtbilirubin ≥2-fache Norm. In letzterer Situation spricht man von sog. "Hy’s Law" oder "Hy’s rule"-Fällen (nach Hyman Zimmerman; 1914–1999). Hier besteht ein Risiko für ein Leberversagen von ≥ 10 % [7].
DILI kann als asymptomatische Leberwerterhöhung auffallen oder auch Symptome verursachen. Diese variieren von Müdigkeit, Verschlechterung des Allgemeinzustands und Übelkeit bis hin zu Ikterus, Pruritus und hepatischer Enzephalopathie. Bei sogenannten immunoallergischen Reaktionen kann Fieber und ein Hautausschlag bestehen.
Diagnose
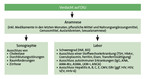
Da es sich bei DILI um eine Ausschlussdiagnose handelt, ist für die weitere Diagnostik eines DILI-Verdachtsfalles eine umfassende Anamnese erster und wichtigster Schritt. Sie erlaubt eine zielgerichtete und individuell angepasste Abklärung (Abb. 3).
Anhand der Untersuchungsergebnisse kann ein Score helfen (z. B. CIOMS/RUCAM; https://livertox.nih.gov/rucam.html), die Wahrscheinlichkeit zu bestimmen, mit der ein Medikament DILI ausgelöst hat (Kausalität). Zur Einschätzung der Schwere der Leberschädigung werden neben ALT, AST, AP und GGT auch die Syntheseparameter INR/Quick, Albumin und Bilirubin benötigt. Bei eingeschränkter Leberfunktion (INR-Erhöhung, Bilirubin-Erhöhung) und deutlich erhöhten Leberparametern sowie symptomatischen Patienten ist eine Hospitalisierung des Patienten notwendig. Ebenso sollte bei Zeichen des akuten Leberversagens (akuter Leberschaden mit INR ≥ 1,5 und Enzephalopathie/mentale Alterationen) der Patient in einem Zentrum mit der Möglichkeit zur Lebertransplantation weiterbehandelt werden. Häufig finden sich unspezifische Erhöhungen des Ferritin-Wertes (akute Phase-Reaktion) oder auch positive Auto-Antikörper. Dies sollte im Verlauf kontrolliert werden.
Die Leberbiopsie spielt bei der Diagnose von DILI eine untergeordnete Rolle, da in den meisten Fällen von DILI keine spezifischen Veränderungen vorliegen. Zeigen sich die Leberwerterhöhungen nach Absetzen des verdächtigten Medikaments rückläufig, kann meist auf eine Biopsie verzichtet werden. Im Einzelfall kann die Biopsie hilfreich sein, um andere Ursachen auszuschließen und den Schweregrad der Schädigung zu bestimmen.
Therapie
Primäre Therapie ist das Absetzen des ursächlichen Agens, was die Wichtigkeit der korrekten Diagnosestellung und Kausalitätsbeurteilung unterstreicht. Bei drohendem Leberversagen durch Paracetamol-Intoxikation ist mit N-Acetylcystein (NAC) ein effektives Antidot verfügbar. Das akute Leberversagen durch Idiosynkrasie hat eine schlechtere Prognose. Als Ansätze werden N-Acetylcystein und Steroide untersucht. Dies sollte in spezialisierten Zentren im Rahmen von Studien erfolgen.
Solange keine höhergradige hepatische Enzephalopathie vorliegt, scheint NAC einen Überlebensvorteil zu bieten. Steroide zeigen wechselnde Effektivität. Ursodeoxycholsäure kann bei prolongiertem cholestatischen Schaden probatorisch eingesetzt werden. Patienten, welche bei V. a. DILI mit Steroiden behandelt werden, müssen ausreichend nachbeobachtet werden, um sicher keine Autoimmunhepatitis zu übersehen [8].
Das auslösende Medikament sollte in Zukunft wegen des Risikos eines schwereren Verlaufs der Reaktion bei Re-Exposition gemieden werden. Eine Re-Exposition zu diagnostischen Zwecken ist unbedingt zu vermeiden und nur wenigen ausgewählten Einzelfällen vorbehalten.
Aufgrund der Herausforderungen, die sowohl für die Medikamentenentwicklung als auch für die Klinik bestehen, ist der Bedarf für eine Verbesserung der Diagnostik und auch die Entwicklung prognostischer Marker von großer Bedeutung.
Seit 2014 läuft das prospektive europäische DILI-Register (Pro-Euro-DILI) als große paneuropäische Studie, die unser Wissen über DILI weiter verbessern soll. Als aktuell vielversprechende Ansätze gelten neue Biomarker und Pharmakogenomik [9]. Ein neu entwickelter Test, welcher Monozyten aus Blutproben betroffener Patienten für die Diagnose von DILI und zur Identifizierung der auslösenden Substanz verwendet, zeigt ebenfalls vielversprechende Ergebnisse [10].
DILI durch Nahrungsergänzungsprodukte und pflanzliche Arzneimittel
Leberschädigungen durch pflanzliche Arzneimittel und Nahrungsergänzungsmittel (herbals and dietary supplements = HDS) werden in den USA zunehmend berichtet [13] und scheinen auch in Europa auf dem Vormarsch zu sein [14].
Diese Substanzen sind schwer zu bewerten, da a) meistens keine Daten aus kontrollierten Studien vorliegen, b) Kontaminanten die Ursache für den Leberschaden darstellen können (fragwürdige Ware aus dem Internethandel, wie z. B. Steroide in angeblich steroidfreien Muskelaufbaupräparaten oder natürliche Kontaminanten wie z. B. Pyrrolizidinalkaloide in Kräutertees) und c) diese Reaktionen häufig nicht erfasst werden, da viele Patienten HDS bei der Medikamentenanamnese nicht mit angeben.
In Asien ist bis zu ein Drittel der DILI-Fälle durch traditionelle chinesische Medizin (TCM) verursacht [15], in Europa sind Fallberichte für verschiedenste Substanzen veröffentlicht. Bekannt sind u. a. Kava-Kava (Marktrücknahme), Umckaloabo, Schöllkraut (Iberogast®), Grüntee-Extrakt, Noni-Saft und Echinacea.
Auch mit HDS sind schwere Verläufe mit Leberversagen und Tod beschrieben, so dass bei der Anamnese unbedingt gezielt nachgefragt werden sollte. Auch wegen etwaiger Interaktionen, wie z. B. für Johanniskraut bekannt, ist die Anamnese bezüglich solcher Präparate von hoher klinischer Relevanz.
Interessenkonflikte: Der Autor hat keine deklariert
Erschienen in: Der Allgemeinarzt, 2019; 41 (8) Seite 16-20