Bei der Diabetestherapie kommt es darauf an, den Blutzucker sicher zu senken sowie kardiovaskuläre Risikofaktoren zu minimieren. Eine gute Einstellung des Blutzuckers sollte immer unter einer Vermeidung von Hypoglykämien erfolgen. Im folgenden Beitrag gehen wir auf die Häufigkeit, Definition, Symptomatik, Komplikationen, Risikofaktoren sowie auf praktische Aspekte bei der Therapie und Vermeidung von Hypoglykämien ein.
Schwere Hypoglykämien treten bei Patienten mit Typ-1-Diabetes ca. 0,6- bis 1,7-mal pro Jahr auf. In der großen Diabetes Control and Complications Trial (DCCT)-Studie waren es 0,6 pro Jahr, wobei in dieser Studie Patienten, die bereits zuvor schwere Hypoglykämien erlitten hatten, ausgeschlossen waren [5, 11]. Bei Patienten mit Typ-2-Diabetes sind schwere Hypoglykämien deutlich seltener [10, 15]. Hier gibt es eine große Schwankung in den Angaben, ein Durchschnittswert ist ca. eine Episode jedes zweite Jahr. Da die Zahl der Patienten mit Typ-2-Diabetes ca. 10- bis 20-mal größer ist als die Zahl der Patienten mit Typ-1-Diabetes, ist jedoch die absolute Zahl von Hypoglykämien bei Typ-2-Diabetikern höher.
Milde Hypoglykämien werden bei Patienten mit Typ-1-Diabetes ca. zweimal pro Woche beobachtet und stellen eine Dunkelziffer bei Patienten mit Typ-2-Diabetes dar. Insbesondere bei Patienten mit Typ-1-Diabetes tritt die Hälfte aller hypoglykämischen Episoden in der Nacht auf.
Definition einer Hypoglykämie
Es gibt unterschiedliche Definitionen von Hypoglykämien. Kriterien sind dabei, ob Mithilfe erforderlich war, ob eine Hypoglykämie biochemisch validiert wurde und ob hypoglykämiebedingte Symptome auftraten, wie z. B. bei Blutzuckerwerten < 50 mg/dl (2,8 mmol/l). Eine Arbeitsgruppe der "Amerikanischen Diabetes Gesellschaft" hat eine sinnvolle und pragmatische Klassifikation von Hypoglykämien vorgeschlagen [16]. Diese Einteilung ist in Übersicht 1 zusammenfassend dargestellt. Eine schwere Hypoglykämie wird insbesondere durch die Erforderlichkeit von Fremdhilfe definiert. Dann gibt es bei verifizierten Blutzuckerwerten ≤ 70 mg/dl (3,9 mmol/l) entweder symptomatische oder asymptomatische Hypoglykämien. Ein Bericht von Symptomen, ohne dass diese biochemisch verifiziert worden sind, entspricht einer "wahrscheinlichen Hypoglykämie". Wichtig ist die "Pseudo-Hypoglykämie", die mit dem Patienten besprochen werden muss. Hier nehmen die Patienten typische Hypoglykämie-Symptome wahr, aber der Blutzucker ist > 70 mg/dl (3,9 mmol/l).
Symptomatik einer Hypoglykämie
Grundsätzlich werden Symptome, die durch das autonome Nervensystem bedingt sind, unterschieden von neuroglykopenischen Symptomen. Diese sind in Übersicht 2 zusammengefasst. Aus dieser Zusammenfassung geht hervor, dass insbesondere die neuroglykopenischen Symptome "chamäleonartig" auftreten können und den Arzt immer daran denken lassen sollten.
Komplikation von Hypoglykämien
Zu den neurologischen Komplikationen zählen epileptische Anfälle, ataktische Bewegungsstörungen und transiente Hemiplegien. Auch eine fokale neurologische Symptomatik ist möglich und insbesondere auch eine Amnesie, die sich klinisch wie ein "Locked-in-Syndrom" manifestieren kann [15].
Ob Hypoglykämien langfristig zu intellektueller Entwicklungsverzögerung oder eingeschränkter Leistungsfähigkeit führen können, ist in prospektiven Studien, wie z. B. der DCCT-Studie, bei Patienten mit Typ-1-Diabetes nicht belegt [4]. Im Moment wird davon ausgegangen, dass schwere Hypoglykämien durchaus mit akuten Beeinträchtigungen der kognitiven Funktion einhergehen können, dass allerdings milde Hypoglykämien mit Blutzuckerwerten über 50 mg/dl (2,8 mmol/l) zu keiner klinisch relevanten Beeinträchtigung führen. Bei Patienten mit Typ-2-Diabetes gibt es in Versorgungsforschungsdatensätzen Assoziationen zwischen Hypoglykämien und Demenz, wobei hierzu bisher keine prospektiven Studien vorliegen [1]. Des Weiteren besteht auch ein enger Zusammenhang zwischen Typ-2-Diabetes und erhöhtem Risiko für Alzheimererkrankung und Depression [1, 13, 14, 18].
Das HAAF (Hypoglycemia Associated Autonomic Failure)-Syndrom ist durch eine reduzierte Gegenregulation gekennzeichnet [3, 7, 8, 12, 17]. Die für die Gegenregulation verantwortlichen Hormone sind Glukagon, Adrenalin, Kortisol und Wachstumshormon. Glukagon und Adrenalin gelten als "schnelle" und Kortisol sowie Wachstumshormon als "verzögerte" Gegenregulatoren. Es ist bei Patienten mit Typ-1-Diabetes gezeigt worden, dass es bereits sehr frühzeitig zu einem Verlust von Alpha-Zellen und damit zu einer reduzierten oder kaum nachweisbaren Glukagon-Freisetzung kommen kann [6]. Ob diese Patienten häufiger zu Hypoglykämien neigen, ist bisher unbekannt. Patienten mit fehlendem Glukagon haben allerdings als Gegenregulation nur die Adrenalin-Achse zur Verfügung.
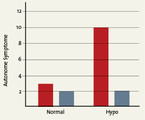
In Bezug auf den Typ-2-Diabetes ist es wichtig zu erwähnen, dass autonome und neuroglykopenische Symptome bei älteren Menschen schwächer ausgeprägt sein können. Bremer et al. haben Patienten im Alter über und unter 65 Jahre mit einem hypoglykämischen Clamp untersucht, bei dem für 30 Minuten ein Blutzuckerwert von 50 mg/dl (2,8 mmol/l) eingestellt wurde [2]. Es zeigte sich, dass ältere im Vergleich zu den jüngeren Patienten keinen Anstieg bzw. keine Aktivierung von autonomen und neuroglykopenischen Symptomen hatten (Abb. 1). Daher wurde weiter oben darauf hingewiesen, dass Hypoglykämien bei Patienten mit Typ-2-Diabetes eine Dunkelziffer darstellen.
In letzter Zeit wurde der Zusammenhang zwischen Hypoglykämien und kardiovaskulären Folgen intensiv diskutiert. Klinische Studien konnten bislang nicht belegen, dass eine therapiebedingte Hypoglykämie Ursache für kardiovaskuläre Ereignisse ist. Klar ist allerdings, dass Hypoglykämien ein Indikator für ein erhöhtes kardiovaskuläres Risiko sein können. Hanefeld et al. [9] haben kürzlich systematisch kardiale Implikationen einer Hypoglykämie bei Patienten mit Diabetes zusammengestellt. Es gibt klinische Hinweise dafür, dass z. B. experimentell kontrolliert-induzierte Hypoglykämien mit einer Verlängerung des QT-Intervalls einhergehen können. Eine Verlängerung des QT-Intervalls ist in aller Regel mit einem erhöhten arrhythmogenen Risikopotenzial verbunden. Zudem sind aus dieser Arbeit in Tabelle 1 wesentliche Phänomene zusammengestellt, die in Assoziation mit einer Hypoglykämie beobachtet werden können und wiederum direkt oder indirekt das kardiovaskuläre Risiko beeinflussen könnten.
Bei Beobachtungsstudien wird deutlich, dass die Überlebensrate von Patienten mit akutem Koronarsyndrom bzw. Herzinfarkt bei niedrigen Blutzuckerwerten sowie bei hohen Blutzuckerwerten höher ist, also eine typische U-Kurve. Dies gilt allerdings nicht allein für Patienten mit Diabetes mellitus, sondern auch für Normalpersonen. Daher scheinen hierfür hypoglykämieassoziierte Reaktionen verantwortlich zu sein, die nicht in einem unmittelbaren Zusammenhang mit dem Diabetes mellitus stehen.
Was sind Risikofaktoren für Hypoglykämien?
Risikofaktoren für Hypoglykämien betreffen im Wesentlichen das blutzuckersenkende Hormon Insulin, das Glukoseangebot selbst und das bereits oben beschriebene HAAF-Syndrom, welches mit einer verminderten Wahrnehmung sowie reduzierten Gegenregulationen verbunden ist.
Beim Insulin ist häufig die Dosierung ein Problem, d. h. entweder ist zu viel Insulin gegeben worden oder zum falschen Zeitpunkt oder das falsche Präparat. Zudem kann sich tatsächlich auch die Sensitivität erhöhen, wie z. B. nach Gewichtsverlust oder einer deutlichen Verbesserung der Glukosetoxizität. Glukosetoxizität besagt, dass hohe Blutglukosespiegel nicht nur eine residuale Betazell-Funktion von Patienten mit Typ-2-Diabetes beeinträchtigen können, sondern auch die Insulinsensitivität. Werden daher länger bestehende hohe Blutzuckerspiegel normalisiert, kommt es in aller Regel auch zu einem deutlichen Einsparpotenzial von Insulin. Zudem kann der Bedarf an Insulin erniedrigt sein, wie z. B. bei körperlicher Aktivität oder auch bei Begleiterkrankungen, wie z. B. einer Niereninsuffizienz.
In Bezug auf die Glukose könnte die Zufuhr vermindert sein, wenn z. B. Mahlzeiten ausgelassen werden oder Fasten-Programme durchgeführt werden. Zudem kann die endogene hepatische Glukoseproduktion, z. B. durch Alkohol, reduziert sein oder die körperliche Aktivität erhöht und damit der Verbrauch von Glukose erhöht sein.
Therapie und Prävention von Hypoglykämien
Akut und im Notfall sollten 15 – 20 g Kohlenhydrate appliziert werden. Bei schweren Hypoglykämien kann auch die Injektion von Glukagon notwendig werden. Dazu sollten Patienten und Angehörige geschult werden.
Die Patienten selbst und ihr Umfeld sollten über die Zusammenhänge des Blutzuckerspiegels mit der körperlichen Aktivität aufgeklärt werden. Außerdem sollten sie den Einfluss der körperlichen Aktivität auf den Blutzucker einschätzen können. Dies müssen Patienten ggf. auch selber für sich ausprobieren. Zudem ist häufig auch praktischer Aufklärungsbedarf bei der Ernährungsweise angeraten. Dies betrifft auch ggf. den nochmaligen Hinweis darauf, welche Nahrungsmittel typischerweise Kohlenhydrate enthalten.
Tipp: Patienten mit Typ-1-Diabetes sollten auf die reduzierte Glukoseaufnahme im Zusammenhang mit einer protein- und fettreichen Ernährung hingewiesen werden, was bei Patienten, die mit einer Insulinpumpe behandelt werden, einen verlängerten oder geteilten Bolus möglich macht.
Bei Patienten mit einer Hypoglykämie-Wahrnehmungsstörung sollten unbedingt Blutzuckerwerte < 60 mg/dl (3,3 mmol/l), besser < 90 mg/dl (5,0 mmol/l) vermieden werden! Es dürfen über mindestens drei Tage keine Hypoglykämien und Blutzuckerwerte unter < 90 mg/dl (5,0 mmol/l) auftreten. Man sollte frühzeitig auf eine entsprechend gezielte Schulung zur Wahrnehmungsstörung hinweisen und ggf. auch auf spezielle Zentren verweisen.
Grundsätzlich sollten die Insulindosis und die Insulinart sowie Applikationsweise überprüft werden und ggf. besteht hier eine klassische Indikation für die kontinuierliche Glukosemessung.
Welche Hinweise gibt es für "unentdeckte" Hypoglykämien?
Nächtliche Hypoglykämien führen häufig zu einer Erhöhung der Nüchternglukose und sind häufig mit einer Störung der Qualität des Schlafes verbunden. Die Patienten fühlen sich morgens unausgeschlafen, wie "erschlagen", ggf. hatten sie Alpträume und sind verschwitzt. Hier muss der Blutzucker nachts zwischen 2:00 und 3:00 Uhr kontrolliert werden. Weitere Hinweise auf eine unentdeckte Hypoglykämie sind eine Diskrepanz zwischen HbA1c- und Blutzuckerwerten. Hier gilt die "Daumenregel", dass ein HbA1c von 6,0 % ungefähr einer mittleren Plasmaglukose von 125 mg/dl (7,0 mmol/l) entspricht. Jede Erhöhung des HbA1c von 1,0 entspricht ca. einer Erhöhung der mittleren Plasmaglukose von 30 mg/dl (1,7 mmol/l).
Zudem ist die wichtigste Maßnahme bei Patienten mit Typ-2-Diabetes, Hypoglykämien zu vermeiden, orale Medikamente einzusetzen, die nicht zu Hypoglykämien führen. Dies gilt nicht nur für Metformin, sondern auch für DPP-4-Hemmer und SGLT-2-Hemmer.
Interessenkonflikte: Der Autor hat in den vergangenen drei Jahren Vortrags- und Beraterhonorare erhalten von AstraZeneca, Boehringer Ingelheim, BMS, Janssen Cilag, Lilly, MSD, Novartis, Novo Nordisk, Roche und Sanofi-Aventis.
#Erschienen in: Der Allgemeinarzt, 2015; 37 (13) Seite 42-46