Die Rheumatoide Arthritis (RA) ist die häufigste rheumatologisch-entzündliche Gelenkerkrankung in Deutschland. Trotz Verbesserung der Aufklärung und Versorgung erfolgt die Diagnose häufig noch zu spät. Ziel ist es heute, eine Therapie einzuleiten, bevor knöcherne Schäden entstehen können. Die hierfür notwendigen Therapeutika stehen uns zur Verfügung.
Arthralgien sind das Frühsymptom der RA, für sich alleine aber sehr unspezifisch und daher vom betreuenden Hausarzt – als erstem Ansprechpartner – abzugrenzen von einer Fülle an Differenzialdiagnosen. Die häufigste Ursache für Gelenkschmerzen mit ca. 15 000 000 Betroffenen in Deutschland ist die Arthrose, die mit steigedem Lebensalter zunimmt. Die entzündlich-rheumatischen Gelenkerkrankungen machen nur ca. 3 – 4 % der beim Hausarzt vorstelligen Patienten mit Gelenkschmerzen aus. Die RA ist hiervon die häufigste entzündlich-rheumatische Erkrankung und betrifft in Deutschland ca. 1 % der Bevölkerung. Frauen sind – wie bei den meisten rheumatologischen Krankheiten – häufiger betroffen, man rechnet etwa in einem Verhältnis 3:1. Der Erkrankungsgipfel liegt in Deutschland zwischen dem 55. und 65. Lebensjahr, häufig erkranken aber auch junge Patienten und Kinder [1].
Früharthritis – Window of opportunity
Mit den vielen neuen Substanzen, welche die Therapie der Rheumatoiden Arthritis in den letzten eineinhalb Jahrzehnten revolutioniert haben, hat sich auch das Therapieziel verändert. Heute ist ganz klar die Remission, d. h. die Beschwerdefreiheit und die Verhinderung von knöchernen Strukturschäden, das Ziel. Dies lässt sich allerdings nur dann erreichen, wenn die Patienten rechtzeitig diagnostiziert und frühzeitig therapiert werden.
Die sogenannte Früharthritis ist dabei zeitlich nicht klar definiert, idealerweise sollte eine Einleitung einer adäquaten Therapie innerhalb der ersten drei bis sechs Monate erfolgen. Man nennt diesen Zeitraum, in dem knöcherne Destruktionen verhindert werden können, daher auch neudeutsch "Window of opportunity". Leider bleibt als großes Problem die teilweise lange Wartezeit bis zum Termin beim Facharzt. Gerade deswegen ist eine gute Vorselektion durch den Hausarzt wertvoll.
Anamnese
Bei der Anamnese sollte die Dauer der Beschwerdesymptomatik sowie der Zeitpunkt der Hauptbeschwerden und die Schmerzintensität erfragt werden. Typisch für die Rheumatoide Arthritis ist eine deutliche Morgensteifigkeit mit > 1 Stunde; kürzere Angaben sind unspezifisch; eine Morgensteifigkeit von wenigen Minuten ist eher typisch für eine Arthrose. Auch lohnt es sich, nach einer Besserung der Beschwerden auf Wärme oder Kälte zu fragen; hier beschreiben Patienten mit einer entzündlichen Arthritis in den meisten Fällen eine Besserung auf Kälte, wohingegen die meisten anderen Patienten (mit Arthrosen, Schmerzsyndromen ...) von einer Besserung durch Wärme sprechen. Besteht der Schmerz vorwiegend in Ruhe, spricht dies auch für eine Arthritis.
Klinische Untersuchung
Bei der klinischen Untersuchung muss vor allem darauf geachtet werden, ob es sich tatsächlich um eine entzündliche Gelenkerkrankung handelt. Hierbei gelten die gleichen typischen Symptome wie bei anderen Entzündungen auch: Schmerz, Rötung, Schwellung, Überwärmung und Funktionsverlust sollten vorhanden sein.
Diese Zeichen lassen sich auch bei der Gelenkuntersuchung leicht beurteilen. Alle Gelenke sollten passiv bewegt und auf Druckschmerz untersucht werden. Prallelastische Schwellungen sprechen für einen Gelenkerguss, knöcherne Verdickungen (vom Patienten nicht selten dennoch als Schwellung empfunden) hingegen eher für eine Arthrose. Je nach Größe des Gelenkes ist ein Gelenkerguss leichter oder schwerer zu ertasten. Das Verteilungsmuster der betroffenen Gelenke kann hierbei zur weiteren Differenzialdiagnose miterfasst werden.
Typisch für eine Rheumatoide Arthritis sind der Volarflexionsschmerz der Handgelenke sowie Schmerzen beim Querdruck auf die Fingergrund- (wie beim Händedruck) und Zehengrundgelenke (sogenanntes Gaenslen-Zeichen). Die Fingerendgelenke, Daumensattelgelenke und Großzehengrundgelenke sollten bei der Beurteilung nicht berücksichtigt werden, da diese häufig arthrotisch verändert sind.
Selbstverständlich sollte bei der körperlichen Untersuchung auch auf andere, mit einer Arthritis assoziierte Veränderungen geachtet werden. Besonderes Augenmerk ist hierbei auf die Haut zu legen, da sich hier vor allem auch wichtige differenzialdiagnostische Erwägungen ableiten lassen. Eine (oft versteckte) Psoriasis, z. B. isoliert an den Nägeln oder im Bereich der Rima ani, kann Hinweis auf eine Psoriasisartritis und ein Schmetterlingserythem auf eine Kollagenose, wie systemischer Lupus erythematodes, sein.
Labor
Beim Labor sollten neben einem einfachen Routinelabor (Blutbild, Kreatinin, GGT, GPT, Harnsäure) vor allem die Entzündungsparameter BSG und CRP bestimmt werden. Diese sind nicht spezifisch für eine RA, aber geben Hinweis auf eine Inflammation im Allgemeinen. Das Routinelabor ist vor allem bei der Abgrenzung zu anderen Differenzialdiagnosen und zur Planung einer möglichen Therapie wichtig.
Als spezifischere Laborparameter sollten des Weiteren bei einer klinisch diagnostizierten Arthritis neben dem Rheumafaktor (RF) unbedingt auch die sogenannten Antikörper gegen citrullinierte Peptid-Antigene (ACPAs) bestimmt werden. Die wichtigsten Vertreter sind die Anti-CCP-AK und die Anti-MCV-AK. Diese Parameter sind viel spezifischer (bis zu 98 % Spezifität) als der RF. Rheumafaktoren sind auch bei ca. 5 % der gesunden Bevölkerung und bei anderen Erkrankungen, wie den Kollagenosen, nachweisbar [2 – 4]. Weiterhin gilt jedoch, dass ein fehlender Nachweis von RF oder ACPAs eine Rheumatoide Arthritis nicht ausschließt; vielmehr dienen diese Antikörper zur Frühdiagnose und vor allem auch zur Prognoseeinschätzung. Seropositive Pawtienten haben ein erhöhtes Risiko für einen rascheren erosiven Progress [5].
Bildgebung
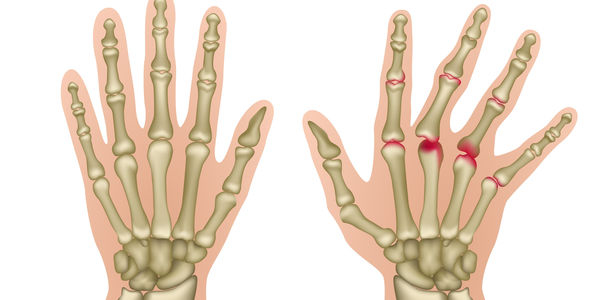
Neben der klinischen Untersuchung und der Labordiagnostik kommt der Bildgebung bei der Diagnose einer frühen RA eine zentrale Rolle zu. Die (unbehandelte) RA führt am Knochen zu charakteristischen, gelenknahen, erosiven Veränderungen. Zeigen sich diese im Röntgenbild der Hand oder des Fußes, kann hierüber die Diagnose der RA gestellt werden. Daher ist eine Röntgenaufnahme der Hände und Füße Teil der Primärdiagnostik bei Verdacht auf eine RA, auch zur Abgrenzung gegenüber arthrotischen Veränderungen.
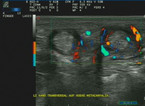
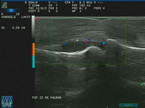
Erosive Veränderungen finden sich allerdings erst im Verlauf der Erkrankung und sollten eigentlich vermieden werden. Für die Frühdiagnose sind daher andere Untersuchungsmethoden, die Synovialitis und Ergussbildung als bildmorphologisches Korrelat der Arthritis nachweisen können, wichtiger. Hierfür eignet sich zum einen die Arthrosonografie, zum anderen die Magnetresonanztomografie. Mittels Gelenkultraschall kann in geübten Händen sehr einfach und schnell eine Synovialitis oder Tenosynovitis dargestellt werden, insbesondere mittels Hinzunahme der Powerdopplerfunktion (vgl. Abb. 1 und 2). Zusätzlich ist die Methode auch sehr sensitiv bei der Detektion von Erosionen [6].
Falls diese Untersuchungsmethode nicht zur Verfügung steht oder keinen eindeutigen Befund erbringt, sollte eine MRT-Untersuchung ergänzt werden. Hierbei eignet sich für die Diagnose der RA vor allem die Darstellung des Handgelenkes sowie der MCP- und PIP-Gelenke, welche allesamt mit einer Handspule erfasst werden können. Insbesondere durch Hinzunahme von Kontrastmittel zeigen sich hier selbst milde, beginnende Entzündungen. Teilweise kann anhand der KM-Aufnahme und der Dynamik sogar zwischen verschiedenen Arthritiden unterschieden werden [7, 8].
Die 3-Phasen-Skelettszintigrafie wird aufgrund ihrer relativ geringen Sensitivität und der schlechten anatomischen Auflösung bei der RA-Diagnostik nur noch in seltenen Fällen herangezogen.
ACR/EULAR- Klassifikationskriterien der RA
Liegen bereits typische, erosive Veränderungen an den Gelenken vor, bedarf es keiner weiteren Diagnostik. Für alle anderen Patienten mit nicht anderweitig erklärbaren Gelenkbeschwerden/ -entzündungen wurden von der Europäischen Liga gegen Rheumatismus (EULAR) und dem Amerikanischen College of Rheumatology (ACR) 2010 neue Klassifikationskriterien festgelegt, um früher eine Diagnose einer RA, insbesondere für frühe Studieneinschlüsse, stellen zu können [9](vgl. Tabelle). Hier werden mit Hilfe eines Punktsystems verschiedene Manifestationen/Laborwerte bewertet und addiert. Erreicht ein Patient mehr als fünf Punkte, gilt die Diagnose RA als sicher.
Auch für den Hausarzt ist die Nutzung dieser Kriterien sinnvoll, gerade um mit einfachen Mitteln zu einer gut begründbaren Diagnose zu kommen und so die zeitnahe Vorstellung bei einem Facharzt zu ermöglichen.
Die meisten Praxen/Kliniken bieten heutzutage eine sogenannte Früharthritissprechstunde an, hierdurch können Hausärzte durch eine kompetente Vorarbeit die Vorstellung beim Facharzt beschleunigen. Die S1-Leitlinie der Deutschen Gesellschaft für Rheumatologie rät zu einer Vorstellung beim Rheumatologen, wenn persistierende Gelenkschwellungen (z. B. länger als sechs Wochen) in mehr als zwei Gelenken bestehen [10].
Zusammenfassung und Empfehlung
Vom Hausarzt sollte bei Verdacht auf eine RA in Anamnese und klinischer Untersuchung ergänzt werden:
- BSG/CRP
- RF und Anti-CCP-AK (oder Anti-MCV)
- Ggf. Röntgen der Hände (Frage: Erosionen oder arthrotische Veränderungen?)
→ Verweis an Facharzt, am besten über eine Früharthritissprechstunde (häufig separate Anmeldungsbögen vorhanden)
- Sonografie und MRT sowie weitere Differenzierung der Arthritis können ggf. dann beim Facharzt ergänzt werden.
- Überbrückend bis zur endgültigen Diagnose können nichtsteroidale Antirheumatika (NSAR) eingesetzt werden. Eine spezifische Therapie sollte erst nach eindeutiger Diagnose durch den Facharzt erfolgen.
Interessenkonflikte: Die Autoren haben keine deklariert.
Erschienen in: Der Allgemeinarzt, 2015; 37 (12) Seite 16-20