Die Weltgesundheitsorganisation (WHO) definiert sexuelle Gesundheit als einen Zustand des körperlichen, emotionalen, mentalen und sozialen Wohlbefindens in Bezug auf die Sexualität und nicht nur als das Fehlen von Krankheit, Funktionsstörungen oder Gebrechen. In Anbetracht dessen erscheint es umso wichtiger, Wissen um Diagnostik, Therapie und Prävention von sexuell übertragbaren Infektionen (STI) sowie von deren möglichen Symptomen und Spätfolgen in das ärztliche Gespräch zu integrieren. Viele Patienten tabuisieren das Thema „Sexuelle Gesundheit“ im Gespräch mit ihrem Arzt, ebenso wie es für den Arzt ein mit Tabus besetztes Tätigkeitsfeld ist, sodass wichtige Informationen über mögliche Ursachen von Symptomen – wie etwa Fieber – nicht preisgegeben werden.
Der Versorgungs-, Beratungs- und Aufklärungsbedarf ist hier erheblich, denn es geht nicht nur um die Behandlung und Prävention von STI, sondern um alle Aspekte, die eine gesunde Sexualität ermöglichen. In Deutschland zeigt sich deutlich, dass dieser Bereich strukturell und personell unterversorgt ist, die Versorgungsangebote meist stark fragmentiert vorliegen und für Patienten und selbst für Ärzte nicht immer transparent sind. Aus diesem Grunde ist es wichtig, dass – wie bei anderen schweren, nur multidisziplinär zu behandelnden Erkrankungen – nach dem Vorbild einer ambulanten spezialfachärztlichen Versorgung. Zentren eingerichtet werden, damit die Patienten interdisziplinär versorgt werden können.
Der vorliegende Artikel bietet einen Überblick über die wichtigsten STI und ihre Relevanz in der allgemeinmedizinischen Praxis.
HIV
Erstmalig seit der AIDS-Epidemie in den 1980er Jahren lassen sich weltweit sinkende Infektionszahlen bei HIV-Neuinfektionen und Mortalitätsraten verzeichnen. Dies ist einerseits durch die Wirksamkeit der Präventionskampagnen zu erklären. Andererseits erhalten wesentlich mehr infizierte Patienten einen Zugang zur medikamentösen Therapie. Die in den 1980er und 1990er Jahren – teils durch starke Nebenwirkungen – belastenden und zu Beginn der HIV-Epidemie auch nur palliativen Therapiestrategien konnten in den vergangenen 20 Jahren deutlich verbessert und vereinfacht werden. Eine einmalige Tabletteneinnahme pro Tag zur Kontrolle der vormals tödlich verlaufenden Infektion ist für viele Patienten möglich. HIV ist zu einer chronischen viralen Erkrankung geworden. Und immer mehr Patienten mit einer HIV-Infektion haben eine fast normale Lebenserwartung. Die allgemeinmedizinische Gesundheitsversorgung ist gerade im Hinblick sowohl auf die Früherkennung einer HIV-Infektion als auch auf die alternden HIV-Patienten die Basis dieser Versorgung.
Die primäre HIV-Infektion
Das klinische Bild einer primären HIV-Infektion kann unterschiedlich verlaufen. Nach einer Inkubationszeit von einigen Tagen bis Wochen nach HIV-Exposition treten erste Symptome in Erscheinung. Das Leitsymptom einer akuten HIV-Infektion ist Fieber. Dies tritt in 80 % der Fälle auf. Neben Hauterscheinungen – meist flüchtigen Exanthemen (rund 50 % der Fälle) – besteht meist eine Allgemeinsymptomatik mit Abgeschlagenheit und Myalgien. Es kommt gehäuft zu zervikaler und axillärer Lymphadenopathie sowie Pharyngitis oder oralen Ulzerationen.
Die Symptome können einem gewöhnlichen grippalen Infekt oder einer Mononukleose sehr ähnlich sein. In Anbetracht dieser Tatsache ist beim Vorliegen der geschilderten Symptome eine entsprechende Risikoanamnese unerlässlich. HIV betrifft nicht nur junge Erwachsene. Die Daten des HIV/AIDS-Registers des Robert Koch-Instituts zeigen, dass 60 % der HIV-Neudiagnosen im Jahr 2011 bei Patienten im Alter von 30 – 49 Jahren erfolgte.
Die akute Infektion wird in den ersten sechs Monaten nach Ansteckung als frühe HIV-Infektion bezeichnet. Es kommt zu einer raschen Vermehrung der HI-Viren im Wirt bis zu mehreren Millionen Viruskopien pro Milliliter Serum. Patienten sind in diesem Erkrankungsstadium hochinfektiös. Bis zu 50 % der HIV-Neuinfektionen werden durch sexuelle Kontakte mit Menschen im Stadium der frühen Infektion, in dem die Betroffenen noch nicht von ihrer Infektion wissen, erworben.
Die Latenzphase
Nach der primären Ansteckung tritt die Infektion in ihre Latenzphase, die bis zu zehn Jahre anhalten kann. Die Patienten bleiben infektiös. Körperliche Beschwerden bestehen selten. Das unkontrollierte Persistieren des Virus führt jedoch zu einer chronischen Immunaktivierung, sodass ein deutlich erhöhtes Risiko für kardiovaskuläre Erkrankungen und Malignome besteht. Die vom HI-Virus infizierten T-Helferzellen (CD4-positive Lymphozyten) sinken im Verlauf dieser Latenzphase von ihrem normalen Wert ab, bei Erwachsenen auf 600 – 1 200 CD4-positive T-Lymphozyten pro µl. Je weiter die Helferzellen sinken, desto häufiger kommt es zum Auftreten von Infektionen. Ab einer CD4-Zellzahl von 350/µl oder niedriger kommt es vermehrt zu Herpes zoster, Candida-Infektionen, Leukoplakien oder etwa chronischer Diarrhoe. Fällt die CD4-Zellzahl weiter, treten opportunistische Infektionen wie Tuberkulose und schwere Infektionen, hervorgerufen etwa durch Kryptokokken, Cytomegalievirus oder Pneumocystis jirovecii, auf.
Therapiestrategien der HIV-Infektion
Die in den 1980er und 1990er teils sehr belastenden Therapiestrategien haben sich stark vereinfacht. Gegenwärtig stehen sechs Substanzklassen zur Therapie der HIV-Infektion zur Verfügung. Neben Protease-Inhibitoren (PI) stellen nukleosidische (NRTI) und nicht-nukleosidische Reverse-Transkriptase-Inhibitoren (NNRTI) das Rückgrat der Therapie dar. Neuere Wirkstoffklassen wie Integrase-Inhibitoren oder Ko-Rezeptorantagonisten (CCR5) kommen ebenfalls zum Einsatz.
Die aktuellen Leitlinien empfehlen eine Kombinationstherapie aus drei antiretroviral wirksamen Substanzen, die gemeinsam eingesetzt werden. Retardformulierungen ermöglichen mittlerweile Einzeltablettenregime (Singletablettenregime, STR), die bei Therapieadhärenz die Infektion zu einer chronischen Erkrankung mit fast normaler Lebenserwartung werden lassen.
Wechselwirkungen
Aus allgemeinmedizinischer Sicht ist das Wissen um mögliche Arzneiinteraktionen unverzichtbar. Inhibitoren und Induktoren des Cytochromsystems können einerseits zu einem gefährlichen Absinken der antiretroviral wirksamen Konzentrationen der HIV-Medikamente führen. Andererseits kann es zu toxischen Wirkstoffspiegeln anderer Arzneimittel durch die Blockade des Enzymsystems kommen. Die Liste der interagierenden Substanzen ist lang und beinhaltet Antihypertensiva und Antiarrhythmika sowie neurotrope Substanzen, Lipidsenker, Protonenpumpenhemmer, Antibiotika und Substitutionsmittel. Im Alltag hat sich zur Überprüfung einer möglichen Interaktion der Einsatz von Interaktionsdatenbanken (zum Beispiel http://www.hiv-druginteractionslite.org ) bewährt und ist daher unverzichtbar.
Therapieziel und Beginn der antiretroviralen Therapie
„Ziel der antiretroviralen Therapie (ART) ist es, durch die Hemmung der HIV-Replikation infektionsbedingte Symptome zu unterdrücken, die Krankheitsprogression zu vermindern, eine Rekonstitution der zellulären Immunität zu erreichen und die chronische Immunaktivierung mit ihren resultierenden Entzündungsprozessen zu reduzieren“ [AWMF-Leitlinie].
Die Einleitung einer ART sollte durch einen HIV-erfahrenen Arzt erfolgen. Die deutsch-österreichischen Leitlinienempfehlen eine Therapieeinleitung ab 500 CD4-Zellen/µl. In der Einleitungsphase kann es – je nach verwendeten Substanzen – zu passageren Nebenwirkungen wie Kopfschmerzen, Übelkeit oder Diarrhoe kommen. Manche Substanzen zeigen jedoch auch zentralnervöse Nebenwirkungen und verursachen Schlafstörungen, z. T. mit halluzinogenen Träumen. Die Ausprägung der Nebenwirkungen kann individuell sehr variieren. Das Absetzen einer neu eingeleiteten Therapie sollte jedoch nur nach Rücksprache mit einem in der HIV-Therapie erfahrenen Arzt erfolgen. Bei der Verordnung von Medikamenten zur Symptomkontrolle ist auf mögliche Interaktionen (s. o.) zu achten.
Adhärenz
Der Therapieerfolg ist essenziell mit der Adhärenz der antiretroviralen Therapie assoziiert. Kommt es durch unregelmäßige Therapieeinnahme zu Schwankungen der Medikamentenspiegel, kann dies zur Resistenzentstehung führen. Bei nicht-nukleosidischen Reverse-Transkriptase-Inhibitoren kommt es häufig nicht nur zur Resistenz gegen den ungenau oder gar nicht eingenommenen Wirkstoff, sondern durch chemische Ähnlichkeit häufig zur Resistenz gegen die gesamte Wirkstoffklasse, die somit zur Behandlung der HIV-Infektion nicht mehr wirksam ist und dem Patienten nicht mehr zur Verfügung steht. Studien zeigen einen deutlichen positiven Zusammenhang zwischen gutem psychosozialen Umfeld der Erkrankten und höherer Therapieadhärenz. Dies ist gerade in Anbetracht der nach wie vor vorhandenen Stigmatisierung HIV-infizierter Patienten und eines daraus resultierenden individuellen Rückzugs ein therapiebeeinflussender Faktor.
Chronische virale Erkrankung
Die HIV-Infektion ist durch die derzeitigen Therapiestrategien zu einer gut kontrollierbaren chronischen viralen Infektion geworden. Je früher mit einer antiretroviralen Therapie begonnen wird, desto komplikationsloser ist der weitere Verlauf und das Gesamtüberleben. Durch die chronische Immunaktivierung besteht jedoch ein erhöhtes Risiko, an kardiovaskulären Erkrankungen sowie Malignomen zu erkranken. Entsprechende Vorsorgeuntersuchungen zur Früherkennung werden daher angeraten.
- Mononukleose-ähnliches Krankheitsbild
- sexuell übertragbare Infektionen (Syphilis, Gonorrhoe, Chlamydien, Lymphogranuloma venereum, Herpes genitalis, Condylomata accuminata, Hepatitis A, B und C)
- neurologische Krankheitsbilder (Demenz, Meningitis, Enzephalitis, Fazialisparese, Polyneuropathie)
- Hodgkin-Lymphom
- mukokutane Läsionen mit Candida albicans, Herpes zoster
- bei < 40-Jährigen: seborrhoische Dermatitis, orale Haarleukoplakie, unklare Exantheme, generalisierte periphere Lymphadenopathie, Analkarzinom, Dysplasie der Cervix uteri
- Wasting-Syndrom
- Schwangerschaft
- Blut-, Samen- und Organspende
- AIDS-definierende Erkrankungen
Gonorrhoe
Junge Erwachsene im Alter von 15 bis 25 Jahren erkranken am häufigsten an Gonorrhoe. Die urethrale Infektion tritt meist zwei bis sieben Tage (Inkubationszeit 3 – 14 Tage) nach Exposition auf und äußert sich in einer akuten Urethritis mit weißlichem Fluor und Schmerzen in der Urethra. Bei Männern kann es zum Auftreten des Bonjour-Tropfens kommen – ein eitriges Sekret am Ostium urethrae. Die Symptomatik kann jedoch deutlich variieren. Bei Frauen bleibt die Infektion häufig unbemerkt. Bei Männern, vor allem jedoch bei Männern, die Sex mit Männern haben (MSM), finden sich vermehrt asymptomatische Infektionen des Rektums und des Pharynx. Die fachgerechte Verwendung von Kondomen schränkt die Übertragungswahrscheinlichkeit auf 40 – 70 % ein.
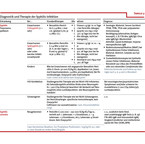
N. gonorrhoe besitzt einerseits durch chromosomale Modifikation und andererseits durch Plasmide die Fähigkeit zur Resistenzbildung gegen Antibiotika. Die Resistenzen können daher an nachfolgende Bakteriengenerationen weitergegeben werden. In Deutschland ist die Resistenzsituation nach der Änderung des Infektionsschutzgesetzes im Jahr 2001 schlecht abgebildet. Neuere Studien zeigen jedoch bis zu 70 % Resistenzen gegen Chinolone in Deutschland. Ein Therapieleitfaden Gonorrhoe ist in Tabelle 1 dargestellt. Eine gezielte Sexualanamnese und entsprechende Probengewinnung von Abstrichen ist beim Verdacht einer Gonorrhoe unerlässlich. Die Generationszeit der Gonorrhoe beträgt weniger als 30 Minuten, so dass von einer ungezielten antiinfektiven Therapie vor Gewinnung der Abstriche zur Bakterienkultur und Nukleinsäureamplifikation (NAAT/PCR) abzuraten ist.
Komplikationen
Im Rahmen einer Gonorrhoe kann es zur Perihepatitis mit passagerem Anstieg der Transaminasen sowie in sehr seltenen Fällen zur disseminierten Gonokokkensepsis kommen. Eine weitere Komplikation stellt der Morbus Reiter – eine Symptomtrias mit reaktiver Arthritis, Konjunktivitis (Iritis) und Urethritis nach stattgehabter Infektion – dar. „Can’t see, can’t pee, can’t climb a tree“ dient als Merksatz dieses Krankheitsbildes, das bis zu zwei Jahre nach Infektion und in seltenen Fällen auch chronisch verlaufen kann.
Chlamydia trachomatis
Chlamydien sind obligat intrazelluläre Bakterien, die, ähnlich der Gonorrhoe, zu entzündlichen, jedoch nicht eitrigen Infektionen der Urethra führen. Chlamydia trachomatis stellt weltweit die häufigste STI dar. Bis zu 40 % der Patienten zeigen Doppelinfektionen von Chlamydien und Gonorrhoe. Neben den Erregern der unkomplizierten nicht-gonorrhoischen Urethritis, durch Genovare D – K verursacht, treten vor allem die Genovare L1 – L3, die Erreger des Lymphogranuloma venereum, vermehrt in Erscheinung. Das Lymphogranuloma venereum ist eine in drei Stadien verlaufende Infektion der Lymphbahnen und -knoten, sowie der Genitalschleimhaut.
Da Chlamydieninfektionen in bis zu 20 % als Koinfektionen gemeinsam mit N. gonorrhoe auftreten, sollte bei passender Anamnese mit rezeptivem analen Sexualkontakt (auch durch Sextoys) und positivem Chlamydien-Nachweis mittels Nukleinsäureamplifikation (NAAT) eine weiterführende Differenzierung hinsichtlich des Genotypus in einem Referenzlabor durchgeführt werden. Die Diagnostik der Chlamydieninfektion allgemein sollte mittels Nukleinsäureamplifikationsverfahren (NAAT) erfolgen (vgl. Tabelle 2). Zumeist ist dies in einer Probengewinnung gemeinsam mit N. gonorrhoe möglich. Für junge Frauen unter 25 Jahren besteht die Möglichkeit, eine Screeninguntersuchung auch ohne aktuelle klinische Beschwerden durchführen zu lassen.
Syphilis
Die Syphilis (Lues) ist eine Infektionserkrankung mit dem Spirochäten-Bakterium Treponema pallidum und wird vor allem durch direkten sexuellen Kontakt übertragen. Die Erkrankung lässt sich in vier Stadien einteilen. Im ersten Stadium – ca. drei bis vier Wochen nach der Ansteckung – zeigt sich häufig ein Primäraffekt im Sinne eines schmerzlosen Ulkus mit Lymphknotenschwellung. Dieses gerötete Geschwür befindet sich häufig am Penis, am Introitus vaginae, im Dammbereich, anal, aber auch oral, und sondert gelegentlich eine farblose Flüssigkeit ab. Ca. ab diesem Zeitpunkt reagiert ein TPHA-Test (Treponema-Pallidum-Hämagglutinationshemmtest) im Blut positiv. Da die Geschwüre unbehandelt nach vier bis sechs Wochen abheilen, bleibt ein Arztbesuch nicht selten aus.
Im Stadium zwei, ca. acht Wochen nach der Ansteckung, können sich disseminierte Papeln (Syphilide) über das gesamte Integument ausbreiten, die nach ca. zehn Wochen wieder abheilen. Auch die Handinnenflächen und Fußsohlen können hierbei befallen sein. Zudem klagen die Patienten häufig über ein allgemeines Krankheitsgefühl mit Müdigkeit, Fieber, generalisierter Schwäche und Abgeschlagenheit. Es können auch breite, weiche Papeln im Genitalbereich auftreten, die sogenannten Condylomata lata. Insgesamt berichten die Patienten über wenig bis keinen Juckreiz.
Drei bis fünf Jahre später (Tertiärstadium) haben sich die Erreger im gesamten Körper ausgebreitet und auch viele innere Organe sind befallen, z. B. Herz, GI-Trakt, Muskeln, Blutgefäße (cave: Aortenaneurysma) und Knochen. Häufig sind hier sogenannte Gummen (schmerzhafte Knoten) unter der Haut zu beobachten.
Bei ca. einem Fünftel tritt zehn bis zwanzig Jahre später das vierte Stadium (die Neurosyphilis) auf. Hierbei kommt es zu einer chronischen Entzündung des zentralen Nervensystems. Häufig ist eine progressive Demenz ein Hauptsymptom.
Zur Diagnose stehen einige Tests zur Verfügung: TPHA, VDRL (Veneral Disease Research Laboratory, Verlaufskontrolle) und der FTA-Abs (T. pallidum-Antikörper-Fluoureszenztest, Bestätigungstest). Der direkte Erregernachweis gelingt über die Dunkelfeldmikroskopie. Als Therapie kommen in den Frühstadien 2,4 Mio. IE Benzathin-Benzylpenicllin i.m. zum Einsatz. Zur Prophylaxe einer Jarish-Herxheimer-Reaktion auf Penicilline sollten zudem 50 – 100 mg Prednisolon p. o. verabreicht werden (vgl. Tabelle 3). Weiter fortgeschrittene Stadien sollten über einen längeren Zeitraum am besten im Rahmen eines stationären Aufenthaltes behandelt werden. Bei einer positiv getesteten Syphilis-Infektion muss eine Meldung an das Robert Koch-Institut erfolgen.
Interessenkonflikte: Der Autor hat keine deklariert.
Auf unserem CME-Portal www.med-etraining.de können Sie ab dem 18.3.2015 diesen Beitrag bearbeiten und bekommen bei Erfolg Ihre Punkte sofort gutgeschrieben.
Erschienen in: Der Allgemeinarzt, 2015; 37 (22) Seite 12-18