Die heute geforderte möglichst frühe Erkennung und Behandlung von entzündlich-rheumatischen Erkrankungen stellen den Hausarzt vor eine große Herausforderung. Es gilt, die wenigen Patienten mit einer entzündlich-rheumatischen Erkrankung aus den vielen Patienten mit degenerativ oder fehlstatisch-myalgisch bedingten Beschwerden herauszufiltern. In diesem Artikel sollen daher häufige entzündlich-rheumatische Erkrankungen des Erwachsenen bezüglich Epidemiologie und typischer Erstsymptome vorgestellt und zudem praktische Vorschläge zu einer sinnvollen Diagnostik und einer adäquaten Akuttherapie in der Hausarztpraxis gemacht werden.
Degenerativ bedingte Gelenkerkrankungen stellen nicht nur bei Patienten im hohen Alter ein sehr häufiges Problem dar. Nach Angaben der Deutschen Gesellschaft für Rheumatologie (Stand 2008) leiden ca. 10 % der über 20-jährigen Menschen in Deutschland an einer Arthrose der Kniegelenke und ca. 6 % an einer Arthrose der Handgelenke [2]. Frauen sind 1,5-mal häufiger als Männer betroffen, oft kommt es bereits zwischen dem 30. und 40. Lebensjahr zu den ersten Symptomen, die Prävalenz nimmt aber mit zunehmendem Alter natürlich deutlich zu. Aktuell werden pro 100 000 Einwohner jährlich ca. 100 Hand-, 90 Hüft- und 240 Kniegelenksarthrosen erstmals diagnostiziert [2].
Demgegenüber besteht für die klassischen entzündlich-rheumatischen Erkrankungen eine niedrigere Prävalenz. So leiden ca. 440 000 (0,65 %) der erwachsenen Menschen in Deutschland an einer rheumatoiden Arthritis (RA) und weitere 0,1 % an einer undifferenzierten (noch nicht klassifizierbaren) Arthritis. Weitere 340 000 Patienten (0,5 %) sind an einer Spondylitis ankylosans (M. Bechterew) erkrankt, 136 000 (0,2 %) an einer Psoriasisarthritis und 272 000 (0,4 %) an einer undifferenzierten Spondyloarthritis. Weitaus häufiger ist die Gichtarthritis, für die in Deutschland von einer Prävalenz von 1,4 % derzeit ausgegangen wird [8]. Die aufgrund der häufig zusätzlich bestehenden Beteiligung innerer Organe in ihrer Prognose gravierenderen Krankheitsbilder der Kollagenosen und Vaskulitiden zeigen jedoch eine relativ niedrige Prävalenz mit nur 0,1 % der erwachsenen Bevölkerung [2].
Arthrose vs. Arthritis
Durch eine zielgerichtete Anamnese und körperliche Untersuchung kann der Hausarzt in der primären Evaluation bereits oft zwischen degenerativen und entzündlich bedingten Gelenkbeschwerden unterscheiden. Hier sollte nicht nur genau die Anzahl und Lokalisation der betroffenen Gelenke bzw. Gelenkregionen erfragt und dokumentiert werden, sondern auch der zeitliche Verlauf (kontinuierlich vs. in Schüben, Tageszeit) der Symptome. Eine zentrale Rolle kommt hier der typischerweise bei entzündlichen Gelenkerkrankungen vorliegenden Morgensteifigkeit zu. Diese hält bei Patienten mit einer schon länger bestehenden, aber noch unbehandelten entzündlichen Gelenkerkrankung oft mehrere Stunden an. Im Vergleich hierzu berichten Patienten mit einer Arthrose zwar auch über eine sie belastende Morgensteifigkeit, die sich jedoch fast immer rasch bessert (< 15 min).
Bei den häufigeren entzündlich-rheumatischen Erkrankungen sind bisher keine durch einen einzelnen Gendefekt bedingte klassischen Erbkrankheiten bekannt. Dennoch kommt der Erhebung der Familienanamnese große Bedeutung zu, da die Fähigkeit des Immunsystems zu einer autoimmunen Reaktion stark durch den genetischen Hintergrund des Individuums mitbestimmt wird. So sollte z. B. die Information, dass mehrere Geschwister an einer Psoriasis vulgaris erkrankt sind, bei einem Patienten bereits frühzeitig an eine Psoriasisarthritis denken lassen.
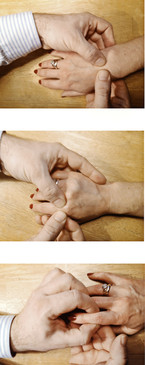
Bei der körperlichen Untersuchung gilt es, klassische Entzündungszeichen (Schmerz bei passiver Bewegung, Schwellung, Überwärmung und Rötung) von Gelenken zu erfassen sowie eine eventuelle Druckschmerzhaftigkeit (Abb. 1a – 1c). Hierfür sollte initial sehr vorsichtig, bei fehlender Schmerzreaktion dann aber auch relativ kräftig Druck auf das zu untersuchende Gelenk ausgeübt werden. Bei einem gesunden Gelenk wird selbst starker Druck vom Patienten im Allgemeinen ohne Schmerzreaktion gut toleriert. Eine Unterscheidung zwischen einer Arthrose und einer Arthritis kann aber allein durch die Druckschmerzhaftigkeit nicht getroffen werden.
Die Entscheidung, ob ein Gelenk geschwollen ist oder nicht, sollte möglichst unabhängig von der Selbsteinschätzung des Patienten erfolgen. Vorsicht: Klassische Zeichen einer Fingerpolyarthrose wie die durch Osteophyten bedingten Auftreibungen der Fingerendgelenke könnten als Gelenkschwellung fehlinterpretiert werden. Größere Gelenkergüsse können in der körperlichen Untersuchung durch eine entsprechende Fluktuation erfasst werden. Ein fehlender Nachweis von Gelenkschwellungen und Gelenkergüssen ermöglicht jedoch leider nicht den Ausschluss eines entzündlich-rheumatischen Krankheitsbildes.
Differentialdiagnose einer Arthritis
Bei eindeutigem Nachweis oder berechtigtem Verdacht auf eine Arthritis durch Anamnese und körperliche Untersuchung sollte deren Ätiologie bereits möglichst durch den Hausarzt weiter eingegrenzt werden. Zunächst sind Anzahl und Lokalisation der betroffenen Gelenke zu erfassen. Hierbei sind die Differentialdiagnosen einer viele Gelenke betreffenden Erkrankung im Vergleich zu einer Oligoarthritis oder zu einer Monarthritis eher begrenzt (vgl. Tabelle 1).
Zur weiteren Eingrenzung der Diagnose sind aber meist neben der Anamnese und körperlichen Untersuchung auch laborchemische und bildgebende Verfahren wichtig, deren Art und Ausmaß durch die zu erwartenden Differentialdiagnosen bedingt und die meist stufenweise durchgeführt werden.
Rheumatoide Arthritis
Die rheumatoide Arthritis (RA), früher als primäre chronische Polyarthritis bezeichnet, stellt bei einer symmetrischen Polyarthritis die häufigste Differentialdiagnose dar. Hierbei ist in den ersten Wochen und Monaten die Symptomatik aber sehr variabel, so dass nicht immer von Anfang an das Vollbild der hand-betonten symmetrischen Polyarthritis besteht.
Pathogenetisch steht eine fehlgeleitete Immunantwort gegen Synovialzellen im Vordergrund. Im weiteren Verlauf führt die durch den Autoimmunprozess getriggerte entzündliche Proliferation des synovialen Gewebes zu einer lokalen Zerstörung von Knorpel, Knochen und Gelenkkapsel sowie von Sehnen und Sehnenscheiden. Es kommen im weiteren Verlauf dann zusätzlich zur direkten autoimmun vermittelten Zerstörung arthrotische Schädigungen durch die mechanische Fehlbelastung der Gelenke hinzu.
Bei der Erhebung der Anamnese von Patienten, die erste Symptome einer RA entwickeln, zeigen sich diese oft sehr verwundert über den raschen Wechsel der durch Arthralgien betroffenen Gelenkregionen. Hier lässt sich oft eine Morgensteifigkeit von deutlich über 30 Minuten Dauer im Bereich der Hände erfragen. In der körperlichen Untersuchung (Abb. 1a – 1c) zeigen sich insbesondere die Handgelenke und Fingergrund- wie auch Fingermittelgelenke druckschmerzhaft oder sogar bereits leicht geschwollen.
In der Labordiagnostik sind bei einem Befall großer Gelenke meist auch eine erhöhte Blutsenkungsgeschwindigkeit (BSG) und C-reaktives Protein (CRP) auffällig, diese können jedoch bei einem isolierten arthritischen Befall kleiner Gelenke trotz hoher klinischer Aktivität auch im Normbereich liegen. Bei ca. 75 % der Patienten mit einer RA können Rheumafaktoren (RF) und/oder anti-citrullinierte Peptid-Antikörper (ACPA), zu denen auch die derzeit geläufigen anti-CCP-AK gerechnet werden, nachgewiesen werden. Hierbei ist die Spezifität und somit auch der positive Vorhersagewert von ACPA deutlich höher als von RF.
Seit 2010 bestehen für die RA neue Klassifikationskriterien, die gemeinsam von den US-amerikanischen (ACR) und europäischen (EULAR) rheumatologischen Fachgesellschaften erarbeitet wurden (Kasten 1) [1]. Diese Kriterien ermöglichen bei klassischer Klinik (symmetrische Polyarthritis mit Beteiligung von mehr als zehn Gelenken, 5 Punkte) und einer Erkrankungsdauer von mehr als sechs Wochen (1 Punkt) bereits die sichere Klassifikation der Arthritis als eine RA, ohne dass zusätzlich Laborwerte auffällig sein müssen. Bei einer nicht ganz klassischen Klinik kann die Klassifikation als RA aber bei typischen Laborparametern (erhöhte Entzündungsparameter und zusätzlich auffälliger RF und/oder ACPA) ebenfalls schon bei sehr kurzer Erkrankungsdauer gestellt werden. Somit kann anhand der neuen Klassifikationskriterien bei typischen Befunden bereits durch den Hausarzt oft die definitive Diagnose einer RA gestellt werden.
Ist die Diagnose einer RA gesichert, besteht entsprechend den aktuellen Behandlungsrichtlinien die direkte Indikation zur Einleitung einer immunsuppressiven Basistherapie [6]. Hierfür wird meist die einmal wöchentliche Gabe von Methotrexat gewählt, da dieses Medikament eine gute Wirksamkeit bei überschaubaren Risiken bietet. Da hier erst nach sechs bis acht Wochen die volle Wirkung eintritt, werden überbrückend Kortikosteroide und nicht-steroidale Antirheumatika (NSAR) eingesetzt. Hier sind initial tägliche Dosen von 15 bis 30 mg Prednisolonäquivalent meist für eine adäquate Erkrankungskontrolle ausreichend. Bei einem guten Ansprechen der RA kann dann die Dosis wochenweise, z. B. um 2,5 mg/die, reduziert werden. Sollte für Methotrexat eine Kontraindikation oder Unverträglichkeit bestehen, können weitere Basismedikamente wie Sulfasalazin, Hydroxychloroquin und Leflunomid zum Einsatz kommen. Der Einsatz neuerer Immunsuppressiva (Biologika) ist jedoch in der initialen Therapie der RA nur besonders schweren Fällen vorbehalten, z. B. jungen Patienten, die trotz sehr kurzer Erkrankungsdauer bereits deutliche Erosionen der Gelenke aufweisen.
Psoriasisarthritis
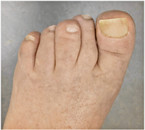
Bei der Psoriasisarthritis (PsA) handelt es sich um ein sehr heterogenes Krankheitsbild [4]. Die PsA kann sich klinisch sowohl als Mon-, Oligo- wie auch Polyarthritis manifestieren, des Weiteren können Enthesitiden (Entzündungen im Bereich von Sehnenansätzen) sowohl im Bereich der Wirbelsäule wie auch der peripheren Gelenke auftreten und es kommt auch zur Ausbildung von Daktylitiden (Schwellung eines gesamten Fingers oder Zehs durch eine Peritendinitis, Abb. 2).
Meist geht die Manifestation einer Psoriasis vulgaris der Haut der PsA um viele Jahre voraus. Die Erkrankung wird jedoch auch immer wieder bei Patienten ohne Hautbefall oder mit nur sehr diskreten Hautläsionen, die dem Patienten oft noch gar nicht selbst aufgefallen sind, diagnostiziert. Deshalb sollte bei ätiologisch unklaren Arthritiden immer eine sorgfältige Inspektion der gesamten Haut, aber insbesondere auch der retroaurikulären Region, des Bauchnabels, der Analfalte sowie der palmaren und plantaren Haut erfolgen.
Bisher konnte noch kein immunserologischer Laborparameter zur Diagnosesicherung einer PsA gefunden werden. Während floride Arthritiden im Bereich großer Gelenke zu deutlich erhöhten Entzündungsparametern (BSG und CRP) führen, können selbst bei multilokulären hochfloriden Enthesitiden diese Parameter im Normbereich liegen. Während die initiale Behandlung von PsA-Patienten mit Arthritiden der peripheren Gelenke ähnlich wie bei einer RA erfolgt, müssen Patienten mit führender axialer Manifestation der PsA eher wie eine Spondyloarthritis behandelt werden.
Spondyloarthritiden
Die Gruppe der Spondyloarthritiden (SpA) enthält neben der Maximalvariante der Spondylitis ankylosans (AS, auch M. Bechterew genannt) auch Krankheitsbilder wie die reaktive Arthritis (meist oligoartikulärer selbstlimitierender Verlauf einer Arthritis mit Beginn wenige Wochen nach einem bakteriellen Infekt) oder die enteropathische SpA (SpA bei Patienten mit einer chronisch-entzündlichen Darmerkrankung).
Anders wie bei der RA stehen hier in der Pathogenese nicht Synovitiden, sondern Enthesitiden im Vordergrund, bei Erstmanifestationen häufig in Form einer Sakroiliitis. Die Patienten berichten hier über insbesondere in der zweiten Nachthälfte auftretende Schmerzen im Bereich der Iliosakralgelenke mit einer langandauernden Morgensteifigkeit. Bei V. a. eine SpA sollte man insbesondere nach dem Symptomenkomplex des „entzündlichen Rückenschmerzes“ fragen (Kasten 2). Während die bis 2009 gängigen Klassifikationskriterien für SpA auf das Krankheitsbild der AS ausgerichtet waren und sich auf im konventionellen Röntgen gewonnene Befunde stützten, kann in den nun durch die internationale Fachgesellschaft ASAS etablierten neuen Klassifikationskriterien für die axiale SpA auch rein klinisch oder bei MR-tomographisch nachgewiesenen Veränderungen die Diagnose frühzeitig gestellt werden (Kasten 3).
In der initialen Therapie der SpA steht der Einsatz von NSAR im Vordergrund, da diese nicht nur symptomatisch, sondern auch krankheitsaufhaltend wirken. Sollten diese nicht ausreichen, muss bei schweren Verläufen aufgrund der fehlenden Wirksamkeit von klassischen Basismedikamenten (Sulfasalazin, Methotrexat oder Leflunomid) auf axiale SpA-Manifestationen dann jedoch direkt eine Therapie mit einem TNF-Inhibitor (Infliximab, Adalimumab, Etanercept, Golimumab oder Certolizumab) erwogen werden.
Polymyalgia rheumatica
Eine Polymyalgia rheumatica (PMR) manifestiert sich meistens zwischen dem 65. und 75. Lebensjahr. Charakteristisch sind hier ein relativ plötzlicher Krankheitsbeginn mit starken Schmerzen und Morgensteifigkeit im Bereich der Schulter- und/oder der Hüftmuskulatur. Zusätzlich treten oft Nachtschweiß, starke Müdigkeit und Abgeschlagenheit und depressive Verstimmungen auf. Da für die PMR bisher kein die Erkrankung beweisender Laborparameter zur Verfügung steht, ist auch bei klassischer Klinik eine sorgfältige differentialdiagnostische Abklärung notwendig, die zumindest neben einem Röntgenthorax in zwei Ebenen und einer Abdomensonographie auch eine sorgfältige klinische Evaluation bzgl. Symptomen einer Riesenzellarteriitis (M. Horton) umfassen sollte. Diese Erkrankung liegt bei ca. 15 % der PMR-Patienten zusätzlich vor und bedarf dann einer intensiveren immunsuppressiven Therapie. Für die initiale Therapie der PMR sollte Prednisolon in einer Dosierung von 15 mg/die gewählt werden [3], spricht die Symptomatik hierauf nicht in wenigen Tagen deutlich an, sollte die Diagnose der PMR kritisch hinterfragt werden.
Lyme-Arthritis
Eine Infektion mit Borrelien kann zu einer infektiösen Arthritis führen, die sich fast immer als Mon- oder Oligoarthritis großer Gelenke (insbesondere der Knie- und Ellbogengelenke) manifestiert [5]. Da die Lyme-Arthritis ohne eine adäquate antibiotische Behandlung meist einen chronisch-rezidivierenden Verlauf hat, wird hier oft zuerst an eine rheumatische Erkrankung gedacht. Der zur Borrelieninfektion führende Zeckenstich kann bei Erstmanifestation der Arthritis wenige Wochen bis viele Monate zurückliegen, bis zu 50 % der Patienten mit einer Lyme-Arthritis haben nie einen Zeckenstich bemerkt.
Da aufgrund der chronischen Infektion bei einer Lyme-Arthritis sich praktisch immer eine positive Borrelien-Serologie zeigt, ist bei für IgG- und IgM-Antikörper negativem Borrelien-ELISA-Test die Diagnose einer Lyme-Arthritis praktisch ausgeschlossen [5]. Aufgrund der langen Latenz zwischen Infektion und Manifestation weisen die Patienten jedoch meist keine IgM-AK gegen Borrelien mehr bei der Erstmanifestation der Arthritis auf. Bestehen die Symptome einer Lyme-Arthritis erst kurz, zeigt sich oft ein rasches und dauerhaftes Ansprechen auf eine für eine Borreliose adäquate antibiotische Therapie mit Doxycyclin oder Ceftriaxon.
Gichtarthritis
Bei der klassischen Symptomatik einer Podagra (plötzlich einsetzende Arthritis des Grundgelenkes der großen Zehe mit starker Rötung und Schwellung) ist es nicht schwer, an eine Gicht zu denken. Die Podagra stellt aber nur bei den ersten Gichtanfällen die häufigste Gelenkmanifestation dar, im Verlauf können praktisch alle Gelenke und selbst gelenkferne Weichteilregionen durch eine Gicht betroffen werden [8]. In der Laboruntersuchung zeigen sich während eines akuten Gichtanfalls oft hohe Entzündungsparameter, die Serumharnsäure liegt aber bei bis zu 40 % der Patienten im Normbereich. Ist zur akuten Entlastung eines Ergusses eine Punktion des betroffenen Gelenkes notwendig, sollte unbedingt eine direkte Mikroskopie der Synovia auf intrazelluläre Harnsäurekristalle zur Diagnosesicherung neben der evtl. zusätzlich differentialdiagnostisch notwendigen mikrobiologischen Diagnostik veranlasst werden.
Hausärztliche Diagnostik
Aufgrund der oft relativ langen Wartezeit bis zu einem Erstvorstellungstermin bei einem niedergelassenen internistischen Rheumatologen ist eine hausärztliche Primärdiagnostik und die Einleitung einer überbrückenden Therapie bei Patienten mit Verdacht auf eine entzündlich-rheumatische Erkrankung meist unumgänglich.
Da durch die Einleitung einer Therapie mit Kortikosteroiden aber nicht nur rasch die klinischen Symptome abklingen, sondern auch auffällige Laborwerte und Befunde der Bildgebung, sollte vor jeder Kortikoidtherapie eine sorgfältige Dokumentation der Beschwerden, der Befunde der körperlichen Untersuchung sowie unbedingt eine Laboruntersuchung inklusive Bestimmung der Entzündungsparameter BSG und CRP durchgeführt werden.
Bei V. a. eine Arthritis sollten im Labor zusätzlich zu den internistischen Routineparametern auch die Serumharnsäure und die Rheumafaktoren bestimmt und ein Test auf ACPA (anti-CCP-AK) veranlasst werden. Bei V. a. eine Kollagenose (z. B. bei Raynaud-Syndrom) sollten antinukleäre Antikörper (ANA) und bei Symptomen einer Vaskulitis (z. B. bei einer Purpura) auch Anti-Neutrophilen-Antikörper (ANCA) bestimmt werden. Bei einer mit einer starken Ergussbildung einhergehenden Monarthritis des Kniegelenkes sollte auch ohne Zeckenstich-Anamnese eine Borrelien-Serologie veranlasst werden. Der Patient sollte aufgefordert werden, den zeitlichen Verlauf und die Art seiner Beschwerden schriftlich zu dokumentieren, bei sichtbaren Schwellungen oder Hautveränderungen ist eine Fotodokumentation mittels Digitalkamera/Smartphone hilfreich.
Bei einer für die entsprechende Erkrankung typischen Erstmanifestation kann der Hausarzt bereits durch diese Maßnahmen oft anhand von Klassifikationskriterien die Diagnose einer entzündlich-rheumatischen Erkrankung definitiv stellen und dann selbstverständlich – bei entsprechender Erfahrung – auch schon vor der rheumatologischen Erstvorstellung eine immunsuppressive Basistherapie entsprechend den aktuellen Therapieempfehlungen einleiten.
Bei für den Hausarzt unklarer Symptom-/Befundkonstellation und starken Beschwerden empfiehlt sich jedoch eine direkte telefonische Kontaktaufnahme mit einem rheumatologischen Kollegen, um das weitere Vorgehen zu besprechen. Aufgrund der oft notwendigen komplexen Abklärung sowie Aufklärung und Schulung des Patienten bei Erstdiagnose einer entzündlich-rheumatischen Erkrankung ist hier auch primär eine stationäre Abklärung in einer rheumatologischen Fachklinik zu erwägen.
Bildgebung: Immer ein MRT notwendig?
Da viele entzündliche Veränderungen bei rheumatischen Erkrankungen sich nicht in klinisch fassbaren Schwellungen oder erhöhten Entzündungsparametern niederschlagen müssen, ist der Einsatz von bildgebenden Verfahren in der rheumatologischen Diagnostik oft nicht verzichtbar. Bei der Wahl der richtigen Methode wie auch einer optimalen Durchführung und Interpretation der erzielten Befunde bedarf es aber viel Erfahrung. So kann ein in der Gelenksonographie geübter Rheumatologe bei der überwiegenden Mehrheit der Patienten mit einer RA bereits mit dem Ultraschall entzündliche Gelenkveränderungen eindeutig feststellen, so dass hier keine MRT-Untersuchungen notwendig werden.
In der rheumatologischen Erfahrung ist die Qualität von angefertigten Röntgen-, MRT- und Szintigraphie-Untersuchungen und insbesondere die Interpretation durch den Radiologen/Nuklearmediziner bei Patienten mit V. a. eine rheumatische Erkrankung sehr wechselhaft. Somit ist es für den Rheumatologen bei einer Erstvorstellung oft einfacher, die notwendige Bildgebung bei geeigneten Kooperationspartnern selbst zu veranlassen, als durch aufwendige Nachbefundung von externen Untersuchungen zu versuchen, sich ein adäquates Bild von dem Patienten machen zu können.
Interessenkonflikte: Der Autor gibt an, von folgenden Firmen und Verbänden in den letzten drei Jahren Honorare für Vorträge erhalten zu haben: Abbott, Chugai, Medac, Mundipharma, MSD, Pfizer, Roche, Berlin-Chemie, Bayerischer Hausärzteverband e.V., DSAI e.V.
Auf unserem CME-Portal www.med-etraining.de können Sie ab dem 7.5.2014 diesen Beitrag bearbeiten und bekommen bei Erfolg Ihre Punkte sofort gutgeschrieben.
Erschienen in: Der Allgemeinarzt, 2014; 36 (8) Seite 14-19